|
Гипермаркет знаний>>Химия>>Химия 10 класс>> Химия: Карбоновые кислоты
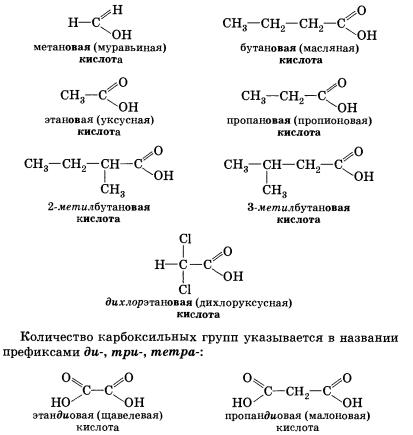
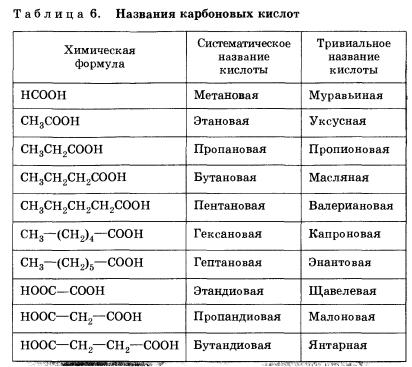
СтроениеВещества, содержащие в молекуле одну или несколько карбоксильных групп, называются карбоновыми кислотами. // OH Карбоновые кислоты, содержащие две карбоксильные группы, называются двухосновными. К ним относятся, например, щавелевая и янтарная кислоты. Существуют и многоосновные карбоновые кислоты, содержащие более двух карбоксильных групп. К ним относится, например, трехосновная лимонная кислота. В зависимости от природы углеводородного радикала карбоновые кислоты делятся на предельные, непредельные, ароматические. Предельными, или насыщенными, карбоновыми кислотами являются, например, пропановая (пропионовая) кислота или уже знакомая нам янтарная кислота. Очевидно, что предельные карбоновые кислоты не содержат п-связей в углеводородном радикале. В молекулах непредельных карбоновых кислот карбоксильная группа связана с ненасыщенным, непредельным углеводородным радикалом, например в молекулах акриловой (пропеновой) СН2=СН—СООН или олеиновой СН3—(СН2)7—СН= СН—(СН2)7—СООН и других кислот. Как видно из формулы бензойной кислоты, она является ароматической, так как содержит в молекуле ароматическое (бензольное) кольцо. Номенклатура и изомерияОбщие принципы образования названий карбоновых кислот, как и других органических соединений, мы уже рассматривали. Остановимся подробнее на номенклатуре одно- и двухосновных карбоновых кислот. Название карбоновой кислоты образуется от названия соответствующего алкана (алкана с тем же числом атомов углерода в молекуле) с добавлением суффикса -ов, окончания -ая и слова кислота. Нумерация атомов углерода начинается с карбоксильной группы. Например:
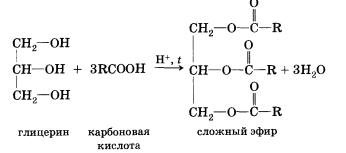
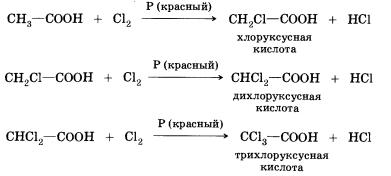
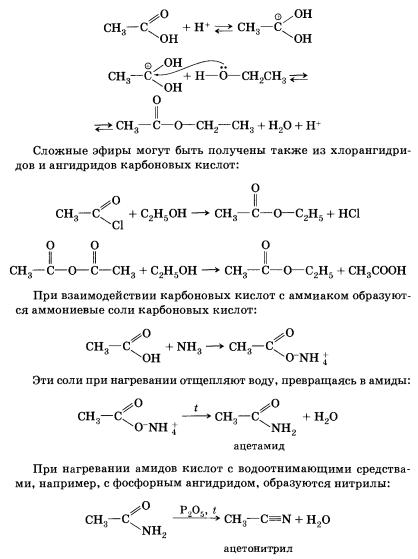
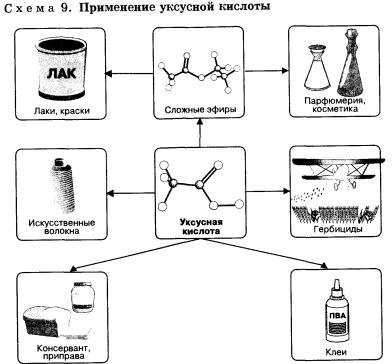
После первого знакомства с многообразным и интересным миром органических кислот рассмотрим более подробно предельные одноосновные карбоновые кислоты. Понятно, что состав этих кислот будет отражаться общей формулой СnН2nO2, или СnН2n+1 CООН, или RСООН. Физические свойства предельных одноосновных карбоновых кислотНизшие кислоты, т. е. кислоты с относительно небольшой молекулярной массой, содержащие в молекуле до четырех атомов углерода, — жидкости с характерным резким запахом (вспомните запах уксусной кислоты). Кислоты, содержащие от 4 до 9 атомов углерода, — вязкие маслянистые жидкости с неприятным запахом; содержащие более 9 атомов углерода в молекуле — твердые вещества, которые не растворяются в воде. Температуры кипения предельных одноосновных карбоно-вых кислот увеличиваются с ростом числа атомов углерода в молекуле и, следовательно, с ростом относительной молекулярной массы. Так, например, температура кипения муравьиной кислоты равна 101 °С, уксусной — 118 °С, пропионовой — 141 °С. Простейшая карбоновая кислота — муравьиная НСООН, имея небольшую относительную молекулярную массу (46), при обычных условиях является жидкостью с температурой кипения 100,8 °С. В то же время бутан (МR(С4Н10) = 58) в тех же условиях газообразен и имеет температуру кипения -0,5 °С. Это несоответствие температур кипения и относительных молекулярных масс объясняется образованием димеров карбоновых кислот, в которых две молекулы кислоты связаны двумя водородными связями. Возникновение водородных связей становится понятным при рассмотрении строения молекул карбоновых кислот. Молекулы предельных одноосновных карбоновых кислот содержат полярную группу атомов — карбоксил (подумайте, чем вызвана полярность этой функциональной группы) и практически неполярный углеводородный радикал. Карбоксильная группа притягивается молекулами воды, образуя с ними водородные связи. Муравьиная и уксусная кислоты растворимы в воде неограниченно. Очевидно, что с увеличением числа атомов в углеводородном радикале растворимость карбоновых кислот снижается. Зная состав и строение молекул карбоновых кислот, нам будет нетрудно понять и объяснить химические свойства этих веществ. Химические свойстваОбщие свойства, характерные для класса кислот (как органических, так и неорганических), обусловлены наличием в молекулах гидроксильной группы, содержащей сильно полярную связь между атомами водорода и кислорода. Эти свойства вам хорошо известны. Рассмотрим их еще раз на примере растворимых в воде органических кислот. 1. Диссоциация с образованием катионов водорода и анионов кислотного остатка. Более точно этот процесс описывает уравнение, учитывающее участие в нем молекул воды. Равновесие диссоциации карбоновых кислот смещено влево, подавляющее большинство их — слабые электролиты. Тем не менее кислый вкус, например, муравьиной и уксусной кислот объясняется диссоциацией на катионы водорода и анионы кислотных остатков. Очевидно, что присутствием в молекулах карбоновых кислот «кислого» водорода, т. е. водорода карбоксильной группы, обусловлены и другие характерные свойства. 2. Взаимодействие с металлами, стоящими в электрохимическом ряду напряжений до водорода. Так, железо восстанавливает водород из уксусной кислоты: 3. Взаимодействие с основными оксидами с образованием соли и воды: 4. Взаимодействие с гидроксидами металлов с образованием соли и воды (реакция нейтрализации): 5. Взаимодействие с солями более слабых кислот, с образованием последних. Так, уксусная кислота вытесняет стеариновую из стеарата натрия и угольную из карбоната калия. 6. Взаимодействие карбоновых кислот со спиртами с образованием сложных эфиров — уже известная вам реакция эте-рификации (одна из наиболее важных реакций, характерных для карбоновых кислот). Взаимодействие карбоновых кислот со спиртами катализируется катионами водорода. Реакция этерификации обратима. Равновесие смещается в сторону образования сложного эфира в присутствии водоотни-мающих средств и удалении эфира из реакционной смеси. В реакции, обратной этерификации, которая называется гидролизом сложного эфира (взаимодействие сложного эфира с водой), образуются кислота и спирт. Очевидно, что реагировать с карбоновыми кислотами, т. е. вступать в реакцию этерификации, могут и многоатомные спирты, например глицерин: Dсе карбоновые кислоты (кроме муравьиной) наряду с карбоксильной группой содержат в молекулах углеводородный остаток. Безусловно, это не может не сказаться на свойствах кислот, которые определяются характером углеводородного остатка. 7. Реакции присоединения по кратной связи — в них вступают непредельные карбоновые кислоты; например, реакция присоединения водорода — гидрирование. При гидрировании олеиновой кислоты образуется предельная стеариновая кислота. Непредельные карбоновые кислоты, как и другие ненасыщенные соединения, присоединяют галогены по двойной связи. Так, например, акриловая кислота обесцвечивает бромную воду. 8. Реакции замещения (с галогенами) — в нее способны вступать предельные карбоновые кислоты; например, при взаимодействии уксусной кислоты с хлором могут быть получены различные хлорпроизводные кислоты: При галогенировании карбоновых кислот, содержащих более одного атома углерода в углеводородном остатке, возможно образование продуктов с различным положением галогена в молекуле. При протекании реакции по свободнорадикальному механизму могут замещаться любые атомы водорода в углеводородном остатке. Если же реакцию проводить в присутствии небольших количеств красного фосфора, то она идет селективно — водород замещается лишь в а-положении (у ближайшего к функциональной группе атома углерода) в молекуле кислоты. Причины такой селективности вы узнаете при изучении химии в высшем учебном заведении. Карбоновые кислоты образуют различные функциональные производные при замещении гидроксильной группы. При гидролизе этих производных из них вновь образуется карбоновая кислота. Хлорангидрид карбоновой кислоты можно получить действием на кислоту хлорида фосфора(ІІІ) или тионилхлорида (SОСl2). Ангидриды карбоновых кислот получают взаимодействием хлор-ангидридов с солями карбоновых кислот. Сложные эфиры образуются в результате этерификации карбоновых кислот спиртами. Этерификация катализируется неорганическими кислотами. Эту реакцию инициирует протонирование карбоксильной группы — взаимодействие катиона водорода (протона) с неподеленной электронной парой атома кислорода. Протонирование карбоксильной группы влечет за собой увеличение положительного заряда на атоме углерода в ней: Способы полученияКарбоновые кислоты могут быть получены окислением первичных спиртов и альдегидов. Ароматические карбоновые кислоты образуются при окислении гомологов бензола. Гидролиз различных производных карбоновых кислот также приводит к получению кислот. Так, при гидролизе сложного эфира образуются спирт и карбоновая кислота. Как уже говорилось выше, реакции этерификации и гидролиза, катарилизируемые кислотой, обратимы. Гидролиз сложного эфира под действием водного раствора щелочи протекает необратимо, в этом случае из сложного эфира образуется не кислота, а ее соль. При гидролизе нитрилов сначала образуются амиды, которые затем превращаются в кислоты. Карбоновые кислоты образуются при взаимодействии магний-органических соединений с оксидом углерода(IV). Отдельные представители карбоновых кислот и их значениеМуравьиная (метановая) кислота НСООН — жидкость с резким запахом и температурой кипения 100,8 °С, хорошо растворима в воде. Муравьиная кислота ядовита, при попадании на кожу вызывает ожоги! Жалящая жидкость, выделяемая муравьями, содержит эту кислоту. Муравьиная кислота обладает дезинфицирующим свойством и поэтому находит свое применение в пищевой, кожевенной и фармацевтической промышленности, медицине. Она также используется при крашении тканей и бумаги. Уксусная (этановая) кислота СН3СООН — бесцветная жидкость с характерным резким запахом, смешивается с водой в любых отношениях. Водные растворы уксусной кислоты поступают в продажу под названием уксуса (3—5%-ный раствор) и уксусной эссенции (70—80%-ный раствор) и широко используются в пищевой промышленности. Уксусная кислота — хороший растворитель многих органических веществ и поэтому используется при крашении, в кожевенном производстве, в лакокрасочной промышленности. Кроме этого, уксусная кислота является сырьем для получения многих важных в техническом отношении органических соединений: например, на ее основе получают вещества, используемые для борьбы с сорняками, — гербициды.
Уксусная кислота является основным компонентом винного уксуса, характерный запах которого обусловлен именно ей. Она продукт окисления этанола и образуется из него при хранении вина на воздухе. Важнейшими представителями высших предельных одноосновных кислот являются пальмитиновая С15Н31СООН и стеариновая С17Н35СООН кислоты. В отличие от низших кислот эти вещества твердые, плохо растворимые в воде. Однако их соли — стеараты и пальмитаты — хорошо растворимы и обладают моющим действием, поэтому их еще называют мылами. Понятно, что эти вещества производят в больших масштабах. Из непредельных высших карбоновых кислот наибольшее значение имеет олеиновая кислота С17Н33СООН, или (СН2)7СООН. Это маслоподоб-ная жидкость без вкуса и запаха. Широкое применение в технике находят ее соли. Простейшим представителем двухосновных карбоновых кислот является щавелевая (этандиовая) кислота НООС—СООН, соли которой встречаются во многих растениях, например в щавеле и кислице. Щавелевая кислота — это бесцветное кристаллическое вещество, хорошо растворяется в воде. Она применяется при полировке металлов, в деревообрабатывающей и кожевенной промышленности. 1. Непредельная элаидиновая кислота С17Н33СООН является транс-изомером олеиновой кислоты. Составьте структурную формулу этого вещества. 2. Составьте уравнение реакции гидрирования олеиновой кислоты. Назовите продукт этой реакции. 3. Составьте уравнение реакции горения стеариновой кислоты. Какой объем кислорода и воздуха (н. у.) потребуется для сжигания 568 г стеариновой кислоты? 4. Смесь твердых жирных кислот — пальмитиновой и стеариновой — называют стеарином (именно из него изготавливают стеариновые свечи). Какой объем воздуха (н. у.) потребуется для сжигания двухсотграммовой стеариновой свечи, если стеарин содержит равные массы пальмитиновой и стеариновой кислот? Какой объем углекислого газа (н. у.) и масса воды образуются при этом? 5. Решите предыдущую задачу при условии, что свеча содержит равные количества (одинаковое число молей) стеариновой и пальмитиновой кислот. 6. Для удаления пятен ржавчины их обрабатывают раствором уксусной кислоты. Составьте молекулярные и ионные уравнения происходящих при этом реакций, учитывая, что ржавчина содержит оксид и гидроксид железа(III) — Fе2O3 и Fе(ОН)3. Почему такие пятна не удаляются водой? Почему они исчезают при обработке раствором кислоты? 7. Добавляемую в бездрожжевое тесто пищевую (питьевую) соду МаНС03 предварительно «гасят» уксусной кислотой. Проделайте дома эту реакцию и составьте ее уравнение, зная, что угольная кислота слабее уксусной. Объясните образование пены. 8. Зная, что хлор более электроотрицателен, чем углерод, расположите следующие кислоты: уксусную, пропионо-вую, хлоруксусную, дихлоруксусную и трихлоруксусную кислоты в порядке усиления кислотных свойств. Обоснуйте свой результат. 9. Чем можно объяснить, что муравьиная кислота вступает в реакцию «серебряного зеркала»? Составьте уравнение этой реакции. Какой газ может выделяться при этом? 10. При взаимодействии 3 г предельной одноосновной карбо-новой кислоты с избытком магния выделилось 560 мл (н. у.) водорода. Определите формулу кислоты. 11. Приведите уравнения реакции, с помощью которых можно описать химические свойства уксусной кислоты. Назовите продукты этих реакций. 12. Предложите несложный лабораторный способ, с помощью которого можно распознать пропановую и акриловую кислоты. 13. Составьте уравнение реакции получения метилформиата — сложного эфира метанола и муравьиной кислоты. В каких условиях следует проводить эту реакцию? 14. Составьте структурные формулы веществ, имеющих состав С3Н602. К каким классам веществ их можно отнести? Приведите уравнения реакций, характерных для каждого из них. 15. Вещество А — изомер уксусной кислоты — не растворяется в воде, однако может подвергаться гидролизу. Какова структурная формула вещества А? Назовите продукты его гидролиза. 16. Составьте структурные формулы следующих веществ: а) метилацетат; 17*. Образец предельной одноосновной органической кислоты массой 3,7 г нейтрализовали водным раствором гидрокарбоната натрия. При пропускании выделившегося газа через известковую воду было получено 5,0 г осадка. Какая кислота была взята и каков объем выделившегося газа? Карбоновые кислоты в природеКарбоновые кислоты очень часто встречается в природе. Они содержится в фруктах и растениях. Они присутствуют в хвое, поте, моче и соке крапивы. Вы знаете, оказывается, что основная масса кислот образуют сложные эфиры, которые обладают запахами. Так запах молочной кислоты, которая содержится в поте человека, привлекает комаров, они ее чувствуют на довольно-таки значительном расстоянии. Поэтому, сколько бы вы не пытались отогнать назойливого комара, он все равно хорошо чувствует свою жертву. Кроме человеческого пота, молочная кислота содержится в соленых огурцах и квашеной капусте. А самки обезьян, чтобы привлечь к себе самца, выделяет уксусную и пропионовую кислоту. Чувствительный, собачий нос способен услышать запах масляной кислоты, которая имеет концентрацию 10–18 г/см3. Многие виды растений способны выделять выделяют уксусную и масляную кислоту. А некоторые сорные растения этим пользуются и выделяя вещества, устраняют своих конкурентов, подавляя их рост, а иногда и вызывая их гибель. Кислотой пользовались и индейцы. Чтобы уничтожить врага, они смачивали стрелы смертельным ядом, который оказался производным от уксусной кислоты. И тут возникает закономерный вопрос, представляют ли кислоты опасность для здоровья человека? Ведь широко распространенная в природе щавелевая кислота, которая содержится в щавеле, апельсинах, смородине и малине, почему-то не нашла применения в пищевой промышленности. Оказывается, щавелевая кислота в двести раз сильнее уксусной кислоты, и способна даже разъедать посуду, а ее соли, накапливаясь в организме человека, образовывать камни. Многие насекомые используют кислоту, таким образом, общаясь друг с другом. Муравьи выделяют ее в момент опасности, оповещая своих сородичей о нападении хищников. Пользу в муравьиной кислоте находят и другие животные. Так, например, с ее помощью медведи избавляются от паразитов. Они ложиться на муравейник, а те защищаясь, впрыскивают муравьиную кислоту и сами того не ведая, являются для медведя спасителями. Где можно использовать карбоновые кислотыКислоты нашли широкое применение во всех сферах человеческой жизни. Их применяют в медицине, косметологии, пищевой промышленности, сельском хозяйстве и используют для бытовых нужд. В медицинских целях используются такие органические кислоты, как молочная, винная, аскорбиновая. Наверное, каждый из вас употреблял для укрепления организма витамин С – это как раз и есть аскорбиновая кислота. Она не только помогает укрепить иммунитет, но и обладает способностью выводить из организма канцерогены и токсины. Молочную кислоту используют для прижигания, так как она обладает высокой гигроскопичностью. А вот винная кислота действует, как легкое слабительное, как противоядие при отравлениях щелочами и как компонент, необходимый для приготовления плазмы при переливании крови. А вот поклонникам косметических процедур, следует знать, что содержащиеся в цитрусовых фруктах, фруктовые кислоты, благоприятно влияют на кожу, так, как проникая вглубь, они способны ускорять процесс обновления кожи. Кроме этого, запах цитрусовых имеет тонизирующее влияние на нервную систему. Замечали ли вы, что такие ягоды, как клюква и брусника долго хранятся и остаются свежими. А знаете почему? Оказывается, в них содержится бензойная кислота, которая является прекрасным консервантом. А вот в сельском хозяйстве широкое применение нашла янтарная кислота, так как с ее помощью можно повысить урожайность культурных растений. Также она способна стимулировать рост растений и ускорять их развитие. презентация урока химии 10 класса, словарик основных терминов, методические рекомендации для учителей химии |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: