|
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Хімія: Метанол, етанол, їхні молекулярні, електронні та структурні формули, фізичні властивості. Хімічні властивості
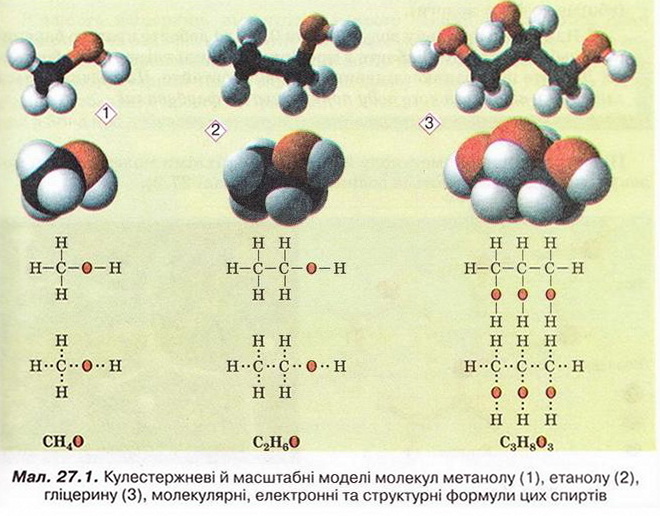
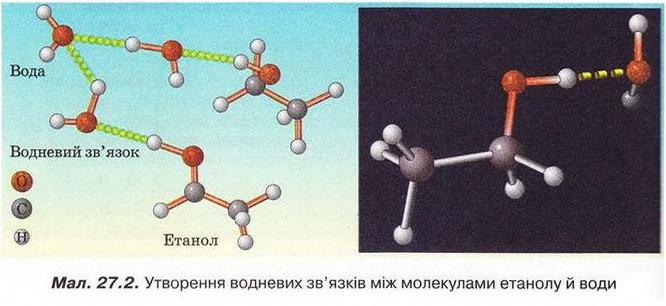
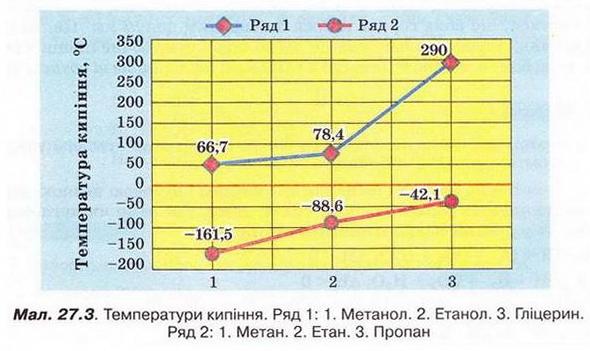
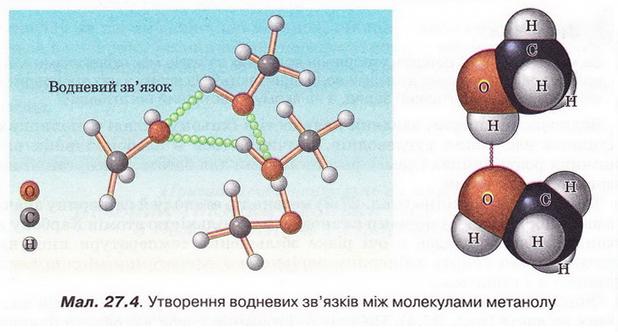
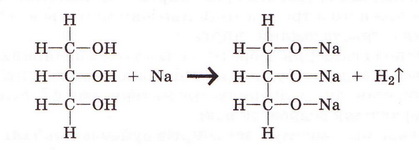
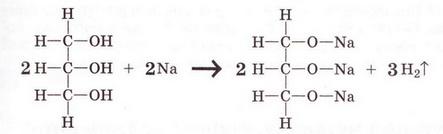
Метанол, етанол, гліцерин Після опрацювання § 27 ви зможете: складати й пояснювати молекулярні, електронні та структурні формули метанолу, етанолу, гліцерину; збирати моделі їхніх молекул; характеризувати склад, структуру, фізичні та хімічні властивості цих сполук; ілюструвати властивості метанолу, етанолу, гліцерину рівняннями хімічних реакцій розрізняти спирти за функціональними ознаками. На шляху до успіху пригадаємо з вивчених курсів хімії, біології, основ здоров'я: які хімічні елементи, окрім Карбону, є органогенами; яка валентність Карбону й Оксигену в органічних сполуках; який склад гідроксильної групи, у яких неорганічних сполуках вона трапляється; що таке електронегативність і як утворюється ковалентний полярний зв'язок; що таке водневий зв'язок і як він позначається на властивостях речовин; як і чому змінюється характер горіння вуглеводнів залежно від умісту Карбону; що таке гідрати; які продукту згоряння вуглеводнів і як їх виявляють; як вода реагує з активними металами. Ви, звичайно, пам'ятаєте (див. § 18), що до складу органічних сполук, окрім Карбону й Гідрогену, може входити також Оксиген. Зокрема, до оксигеновмісних органічних сполук належать спирти - метанол, етанол, гліцерин (у сучасній науковій хімічній літературі вам траплятиметься й інша назва гліцерину - гліцерол). Ви, напевно, звернули увагу на суфікс -ол у назвах цих речовин. Що він означає, на які особливості хімічного складу і будови молекул спиртів вказує? Аби з'ясувати це, розгляньмо моделі, за допомогою яких унаочнюють склад і будову молекул спиртів. • Молекулярні, електронні та структурні формули метанолу, етанолу, й гліцерину наведені на малюнку 27.1. Наявність однієї (чи кількох) груп атомів -ОН є очевидною спільною рисою структур метанолу, етанолу й гліцеролу. Ці речовини можна розглядати як похідні алканів. Приміром, якщо у структурній формулі метану один з чотирьох атомів Гідрогену замінити на гідроксильну групу, дістанемо структурну формулу метанолу. Внаслідок аналогічної дії зі структурною формулою етану одержимо структурну формулу етанолу. Аби зобразити структурну формулу гліцерину, достатньо у структурній формулі пропану замінити на групу -ОН атом Гідрогену біля кожного з трьох атомів Карбону. Метанол і етанол - похідні насичених вуглеводнів, їхні молекули містять по одній гідроксильній групі. Тому ці спирти називають насиченими одноатомними спиртами. Гліцерол - насичений трьохатомний спирт (поясніть, чому). Групу - Н називають функціональною групою спиртів - адже вона зумовлює їхні хімічні властивості - здатність вступати в хімічні реакції. • Фізичні властивості метанолу, етанолу й гліцерину З огляду на це, не дивно, що метанол, етанол і гліцерин добре розчиняються в полярних розчинниках, передусім воді. З нею вони змішуються в будь-яких співвідношеннях (пригадайте, про це йшлося в § 4-6). Під час розчинення метанолу й етанолу між їхніми молекулами й молекулами води утворюються водневі зв'язки (мал. 27.2). Завдання За малюнком 27.2 опишіть утворення водневих зв'язків між молекулами етанолу й води. Між якими атомами вони виникають? На якому з них зосереджений частковий позитивний заряд, а на якому - частковий негативний? Водночас ці спирти, завдяки наявності в їхньому складі неполярних залишків насичених вуглеводнів, розчиняються в слабополярних органічних розчинниках і самі є розчинниками для багатьох неорганічних і органічних речовин. Температури кипіння (мал. 27.3) метанолу, етанолу й гліцерину значно вищі порівняно з алканами з такою самою кількістю атомів Карбону в ланцюзі. Також впадає в очі різке збільшення температури кипіння трьохатомного спирту гліцерину порівняно з одноатомними спиртами метанолом і етанолом. Описані явища пов'язані з утворенням між молекулами спиртів водневих зв'язків (мал. 27.4). На їхнє руйнування треба витратити значну кількість енергії, аби спирт перейшов з рідкого стану в газуватий. Зрозуміло, що між молекулами гліцерину утворюється значно більша кількість водневих зв'язків порівняно з метанолом і етанолом. Тож і температура кипіння гліцерину істотно вища. Завдання За малюнком 27.4 опишіть утворення водневих зв'язків між молекулами метанолу. Між якими атомами виникають водневі зв'язки? На якому з атомів зосереджений частковий позитивний заряд, а на якому - частковий негативний? В'язкість гліцерину, відсутність у нього запаху та солодкий смак (грецьке glicos означає солодкий) також пов'язані з наявністю в його молекулі трьох гідроксильних груп. Натомість метанол й етанол - леткі речовини з характерним «алкогольним» запахом і «пекучим» смаком. Усі ці рідини безбарвні й прозорі. (Про те, як було відкрито гліцерин ви дізнаєтеся з § 30, а про добування етанолу з природної сировини йтиметься в § 33.) • Хімічні властивості метанолу, етанолу й гліцерину також зумовлені наявністю в їхньому складі залишку насиченого вуглеводню й функціональної гідроксильної групи. Спирти беруть участь у найрізноманітніших хімічних перетвореннях, з якими ви матимете нагоду ознайомитися під час вивчення хімії в старшій школі. Розгляньмо дві важливі реакції за участю спиртів і встановімо, чим зумовлений їхній перебіг. Приклад реакції повного окиснення спиртів ви неодноразово спостерігали під час горіння етанолу в спиртовому пальнику й, напевно, звернули увагу на характерний колір полум'я. Варто пам'ятати, що етанол - легкозаймиста речовина й потребує особливо обережного поводження - адже його пара спалахує за 13 °С. Полум'я метанолу, так саме як і етанолу, некіптяве. Який характер горіння гліцерину? Можна припустити, що світність його полум'я має бути більшою порівняно з метанолом й етанолом - адже в молекулі гліцерину міститься три атоми Карбону. Експериментальна перевірка спростовує наші припущення. Якщо в тигельку нагріти кипіння гліцерин об'ємом 1 мл й підпалити його пару, можна пересвідчитися, що вона горить майже безбарвним полум'ям. Це, на перший погляд, парадоксальне явище легко пояснити, обчисливши масові частки Карбону в метанолі, етанолі й гліцерині {викопайте ці обчислення). Завдання Аби гліцерин зайнявся, його треба нагріти до значно вищої температури, ніж приміром, етанол. Поясніть, чому. Отже, метанол, етанол і гліцерин за складом і будовою певною мірою подібні до алканів (поясніть, чим саме), тому, так само як вуглеводні. СН3ОН + 02 → С02 + Н20; ΔН < 0 С2Н5ОН + 02 → С02 + Н20; ΔН < 0 НОСН2 - СНОН - СН2ОН + 02 → С02 + Н20; ΔН < 0 (скорочено С3Н803 + 02 → С02 + Н2 Завдання Перетворіть схеми реакцій повного окиснення спиртів на хімічні рівняння. Визначте, ендо- чи екзотермічними є ці процеси. Наявністю гідроксильної групи й здатністю утворювати водневі зв'язки спирти подібні до води. Тож можна припустити, що, як і вода, вони реагуватимуть з активними металами - калієм, натрієм тощо. Завдання Пригадайте, до якого типу належить реакція води з активними металами. Помістімо в маленьку пробірку з абсолютованим (безводним) спиртом кілька шматочків натрію завбільшки із сірникову головку (поясніть, чому спирт не повинен містити домішок води). Спостерігатимемо розігрівання реагуючої суміші, виділення бульбашок безбарвного газу. Це водень, який після перевірки на чистоту, можна підпалити. Після охолодження пробірки можна побачити утворення білого осаду натрій етилату: 2С2Н5ОН + 2Na → 2С2Н5ONa + Н2↑ Однак реакція з етанолом відбувається не так активно, як взаємодія натрію з водою. Завдання Порівняйте склад і будову молекули води і молекули етанолу. Що, на вашу думку, може бути причиною того, що реакція цих сполук з натрієм відбувається з різною інтенсивністю, адже змін в обох випадках зазнає група -ОН? Аналогічно до етанолу відбувається реакція метанолу з натрієм (перетворіть її схему на хімічне рівняння): СН30H + Nа → СН3ONa + Н2↑ За об'ємом водню - одного з продуктів реакції - було зроблено висновок, що в молекулах метанолу й етанолу лише один атом Гідрогену заміщується на атом Натрію, а в молекулі гліцерину таких атомів - три: Завдання Перетворіть схему реакції гліцерину з натрієм на хімічне рівняння. Отже, атоми Гідрогену, зв'язані в молекулах спиртів з атомами Оксигену, виявляють вищу хімічну активність порівняно з атомами Гідрогену, безпосередньо сполученими з атомами Карбону. Стисло про головне Метанол, етанол, гліцерол (гліцерин) - оксигеновмісні органічні сполуки. Суфікс —ол у назвах цих речовин вказує на наявність однієї (чи кількох) груп атомів —ОН. Метанол, етанол, гліцерин - похідні насичених вуглеводнів, тому їх називають насиченими спиртами. Молекули метанолу й етанолу містять по одній гідроксильній групі, отже, ці спирти - одноатомні. У молекулі гліцерину біля кожного з трьох атомів Карбону міститься гідроксильна група. Гліцерин - трьохатомний спирт. Метанол, етанол і гліцерин добре розчиняються в полярних розчинниках, змішуються з водою в будь-яких співвідношеннях. Під час розчинення метанолу, етанолу й гліцерину між молекулами спиртів й молекулами води утворюються водневі зв'язки. Водневі зв'язки між молекулами спиртів зумовлюють їхні аномально високі порівняно з вуглеводнями температури кипіння. Між молекулами гліцерину утворюється значно більша кількість водневих зв'язків порівняно з метанолом і етанолом, тому температура кипіння гліцерину істотно вища. В'язкість гліцерину, відсутність у нього запаху та солодкий смак також пов'язані з наявністю в його молекулі трьох гідроксильних груп. Метанол і етанол - леткі речовини з характерним «алкогольним» запахом і «пекучим» смаком. Усі ці рідини безбарвні й прозорі. Хімічні властивості метанолу, етанолу й гліцерину також зумовлені наявністю в їхньому складі залишку насиченого вуглеводню й функціональної гідроксильної групи. Спирти вступають у реакції повного окиснення (горіння): 2СН3ОН + 302 → 2С02 + 4Н20; ΔН < 0 С2Н5ОН + 302 → 2С02 + ЗН20; ΔН < 0 2НОСН2 - СНОН - СН2ОН + 702 → 6С02 + 8Н20; ΔН < 0 (скорочено 2С3Н803 + 702 → 6С02 + 8Н20; ΔН < 0 Метанол й етанол - легкозаймисті речовини й потребують особливо обережного поводження. Метанол, етанол, гліцерин горять майже безбарвним некіптявим полум'ям. Реакції повного окиснення спиртів екзотермічні. Як і вода, спирти реагують з активними металами - калієм, натрієм тощо: 2СН3ОН + 2Na → 2CH3ONa + H2↑ 2С2Н5ОН + 2Na → 2C2H5ONa + H2↑ Атоми Гідрогену, зв'язані в молекулах спиртів з атомами Оксигену, виявляють вищу хімічну активність порівняно з атомами Гідрогену, безпосередньо сполученими з атомами Карбону. Якісна реакція на гліцерин пов'язана з наявністю у складі його молекули трьох функціональних груп —ОН. Унаслідок взаємодії гліцерину із свіжодобутим блакитним осадом купрум(ІІ) гідроксиду утворюється яскраво-синій розчин. Застосуйте свої знання й уміння 1. Виберіть кількість спільних електронних пар у молекулі етанолу: 2. Виберіть кількість функціональних груп у молекулі гліцерину: 3. Розташуйте сполуки за зменшенням їхньої температури кипіння: 4. Виберіть сполуки, між молекулами яких утворюються водневі зв'язки: 5. Виберіть сполуки з характерним запахом: 6. Виберіть солодку на смак сполуку: 7. Виберіть характеристики реакції повного окиснення метанолу. 8. Поясніть, окисником чи відновником є натрій у реакції з етанолом. 9. Абсолютизацію (зневоднення) етанолу здійснюють за допомогою безводного купрум(ІІ) сульфату. Опишіть зовнішні ефекти, які, на вашу думку, мають супроводжувати цей процес. За потреби зверніться до малюнка 5.3. 10. Виберіть характеристики реакції гліцерину з натрієм; 11. Виберіть реактиви для проведення якісної реакції на гліцерин: 12. Виберіть зовнішній ефект якісної реакції на гліцерин:
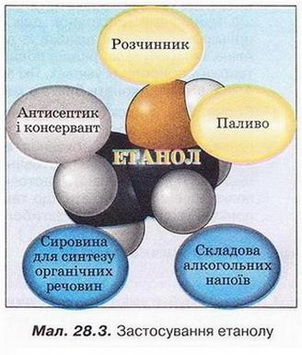
Застосування метанолу, етанолу та гліцерину. Отруйність спиртів, їхня згубна дія на організм людини Після опрацювання § 28 ви зможете: наводити приклади застосування метанолу, етанолу, гліцерину; встановлювати причинно-наслідкові зв'язки між складом, будовою, властивостями та біологічними функціями і застосуванням цих сполук; обґрунтовувати застосування метанолу, етанолу, гліцерину їхніми властивостями. На шляху до успіху пригадаємо з вивчених курсів хімії, фізики й основ здоров'я: що таке полімери; чому випаровування рідин супроводжується зниженням температури; що таке заломлення світла; чому треба охороняти земноводних і плазунів; як запобігти захворюванням шкіри дівчат і хлопців підліткового віку; як впливають на здоров'я підлітків алкоголь, наркотичні й токсичні речовини; що таке Е-коди. • Застосування метанолу, етанолу та гліцерину зумовлене їхніми властивостями. Метанол і етанол - сировина для добування різноманітних органічних речовин, наприклад оцтової кислоти (про неї йтиметься в наступному параграфі). На основі продуктів переробки цих спиртів виготовляють синтетичні каучуки й гуму, полімери й пластмаси, розчинники й лікарські препарати. Завдання Пригадайте, яку речовину добувають у шкільній лабораторії дегідратацією етанолу (за потреби зверніться до § 24). Ви, звичайно, пам'ятаєте, що продуктами взаємодії метанолу й етанолу з натрієм є відповідні алкоголяти. Ці речовини, так само як і вихідні спирти, використовують для виготовлення з різноманітних олій (про них йтиметься в §30) біодизельного пального. У різних країнах існують державні програми застосування метанолу й етанолу на транспорті. Це й ідивідуальне моторне пальне, і добавки до біодизелю й бензину. Реакцію горіння етанолу використовують і в побуті. Наразі модним і функціональним елементом інтер'єру стає камін, що працює на етиловому спирті. З етанолу добувають і горезвісний тетраетилсвинець Рb(СН3СН2)4. Використання цієї речовини поліпшує якість автомобільного бензину. Водночас вона - чи не найпотужніше джерело забруднення довкілля Плюмбумом, що особливо небезпечно для дітей і підлітків. Також етанол є компонентом антифризу та рідин для миття скла, зокрема в автомобілях. Завдання Поміркуйте й висловіть припущення, на яких властивостях етанолу ґрунтується його застосування у складі засобів догляду за автомобілем. Окрім того, етанол - добрий розчинник багатьох речовин і водночас консервант, тому входить до складу різноманітних спиртових розчинів, настоянок, екстрактів з рослинної сировини. Ви, звичайно, пам'ятаєте, що етиловий спирт - летка речовина й легко випаровується. Тож водний розчин етанолу використовують для розтирання під час лихоманки, аби знизити температуру тіла недужого. Ці ж властивості етилового спирту використовують для виготовлення одеколонів, лосьйонів, дезодорантів тощо. Етанол - ефективний консервант не лише для рослинної сировини, у ньому зберігають найрізноманітніші біологічні препарати. Як консервант біологічних препаратів використовують і гліцерин. Ця речовина дуже гігроскопічна, тож, глибоко проникаючи всередину тканин, гліцерин запобігає їхньому висиханню. Показник заломлення гліцерину такий, що біологічні препарати виглядають дуже прозорими - це поліпшує наочність зразків (мал.28.1). Прозорість властива й тим сортам туалетного мила, в яких масова частка гліцерину становить 8-15 % . Таке мило та інші косметичні препарати з гліцерином добре зволожують шкіру. Побутує думка, що через гігроскопічність гліцерин може спричинити зневоднення і висушування шкірного покриву. Однак це стосується лише препаратів з масовою часткою гліцерину понад 40 %. Гліцерин є важливою складовою зубних паст, медичних і парфумерних мазей, гелів, кремів для взуття тощо - він запобігає їхньому висиханню. Здатність гліцерину розчиняти різноманітні речовини дуже важлива. Його використовують для виготовлення висококонцентрованих медичних розчинів, вибавляння плям від чаю, кави, молока, чорнила. Не злічити всіх галузей застосування гліцерину та продуктів його хімічної переробки. Виробництво паперу, пакувальних матеріалів, пластмас, ліків і вибухівки потребує величезних кількостей гліцерину. Зокрема, з гліцерину виробляють нітрогліцерин. Це і засіб невідкладно: допомоги під час нападу стенокардії, і основа для виготовлення динаміту - вибухівки. Нетоксичність, солодкий смак (пригадайте, що означає грецьке слово (glicos), висока в'язкість, здатність утримувати вологу зумовили використання гліцерину у виробництві лікерів, шоколаду, морозива, желе, гірчиці, хлібобулочних і макаронних виробів, екстрактів кави, чаю. імбиру тощо. • Отруйність спиртів, їхня згубна дія на організм людини вам відома з курсу основ здоров'я. Розгляньмо це питання докладніше. Метанол (так званий деревний спирт) - надзвичайно отруйна речовина. Недарма місткості з метанолом маркують міжнародним застережним знаком (мал. 28.2). Смертельна доза метанолу в разі потрапляння всередину організму становить З0 г, проте важке отруєння, що супроводжується сліпотою, може спричинити метанол масою 5-10 г. Його пара подразнює слизові оболонки очей, верхніх дихальних шляхів, спричиняє головний біль, дзенькіт у вухах, тремтіння кінцівок, неврити, розлади зору. Метанол може проникати в організм навіть крізь неушкоджену шкіру. Висока отруйність метанолу стала однією з причин того, що з 2007 р. у гоночних болідах паль¬не на основі метанолу замінили етанолом. Ці два сусідніх члени гомологічного ряду спиртів дуже схожі за фізичними властивостями, їх неможливо розрізнити за зовнішнім виглядом, смаком, запахом тощо. Смертельна доза етанолу значно вища порівняно з метанолом становить від 4 до 12 г на кілограм маси тіла людини. Проте небезпечність уживання етанолу, алкогольних напоїв і їхніх сурогатів важко переоцінити. Унаслідок гострої алкогольної інтоксикації пригнічується діяльність центральної нервової системи (ви вивчатимете це в курсі біології), зокрема дихального центру. Хронічне отруєння організму алкоголем, ефект звикання до цього наркотику - складна медична й соціальна проблема. В організмі людини немає жодного органа, який би не потерпав від алкогольної інтоксикації, однак найсильніше етанол уражає мозок. Зламані долі, зруйновані родини, деградація особистості, соціальне сирітство, смерті й каліцтва в автомобільних аваріях та на виробництві, вроджені вади розвитку в дітей... Сумний перелік наслідків уживання алкогольних напоїв задовгий для одного параграфа підручника. Кожен з вас не лише має усвідомити негайний вплив уживання як міцних, так і слабоалкогольних напоїв на здоров'я людини. Найголовніше - знайти в собі сили, виявити характер, аби рішуче відмовитися від небезпечних пропозицій, не спокуситися скуштувати алкогольні напої. Варто зробити свідомий вибір на користь здорового способу життя, міцної родини, здорового й щасливого сьогодення - майбуття. На прикладі метанолу й етанолу ви пересвідчилися, що корисність чи дохідливість речовин залежить насамперед від того, для чого й у який од осіб їх використовує людина. Підтвердження цього ви зможете знайти наступних параграфах підручника. Стисло про головне Застосування метанолу, етанолу та гліцерину зумовлене їхніми властивостями. На малюнку 28.3 представлено застосування етанолу. Використання метанолу подібне до етанолу, однак обмежене токсичністю цього спирту. Унікальний комплекс фізичних і хімічних властивостей гліцерину мовив його широке застосування в медицині, харчовій промисловості, органічному синтезі, виробництві полімерів, побуті. Гліцерин - розчинник, консервант, зволожувач, зм'якшувач, антифриз, засіб для вибавляння плям тощо. Метанол - надзвичайно отруйна речовина, залежно від дози спричиняє сліпоту або смерть. Смертельна доза етанолу значно вища зрівняно з метанолом. Проте небезпечність уживання етанолу, алкогольних напоїв і їхніх сурогатів дуже висока, бо етанол спричиняє наркотичну залежність. Кожен має усвідомити негативний вплив уживання як міцних, так і слабоалкогольних напоїв на здоров'я людини. Варто зробити свідомий вибір на користь здорового способу життя. Корисність чи шкідливість речовин залежить насамперед від того, для чого й у який спосіб їх використовує людина. Застосуйте свої знання й уміння 1. Наведіть приклади застосування метанолу, етанолу, гліцерину. 2. Обґрунтуйте застосування етанолу в медицині його властивостями. 3. Поясніть, які властивості гліцерину зумовили його використання як компонента косметичних засобів. 4 Дарина розповіла однокласниці Наталці, що карамель «Малібу» містить гліцерин. Та не йняла їй віри. Чи вважаєте ви, що Даринчина інформація заслуговує на довіру? Чому? 5. Дев'ятикласник Роман стверджував, що етанол - один з продуктів обміну речовин в організмі людини, а тому ця речовина нешкідлива. Чи згодні ви з ним? Обґрунтуйте свою позицію. 6. Використовуючи різноманітні джерела інформації, дізнайтеся, яку харчову добавку позначають кодом Е 422. 7. З віком уміст вологи в епідермісі зменшується. Природна мінеральна вода «Юзя» з трускавецького курорту містить гліцерин. Як ви вважаєте, чи мають підстави легенди про «омолоджувальну» дію цієї води? Чому? 8. Постановою № 41 від 27.12.2007 р. Міністерства охорони здоров'я України заборонено виробництво та реалізацію населенню засобів догляду за автотранспортом, які містять метанол. Оцініть доцільність такого припису - адже метиловий спирт дуже добре змиває бруд, не залишаючи розводів на склі. 9. Сергій розповів однокласникам, що один зі світових лідерів у галузі електроніки пропонує споживачеві новітню модель практично повністю прозорого стільникового телефону з великим сенсорним екраном на основі органічних рідких кристалів. Єдина непрозора частина телефону - блок, що містить GSM модуль, мікросхему й динаміку металевій оболонці. Усередині корпусу - підфарбована рідина на основі метанолу. Телефон можна зарядити, а змінювати кольори дуже зручно - досить лише залити паливо з іншого флакончика. Чи хотіли б ви мати такий телефон чи подарувати його, приміром, молодшому братові або сестрі? Поясніть свою позицію. 10. Батько Олега й Аліни - біолог, вивчає плазунів. Підлітки не змогли дійти згоди, що саме подарувати татові на день народження. Олег стверджував, що найліпший подарунок для справжнього чоловіка - міцний напій, приміром сувенірна пляшка із заспиртованою змією або саламандрою. Аліна заперечувала: радше подарувати фотоальбом із зображеннями цих тварин у природних умовах. Які аргументи, на вашу думку, мала б навести Аліна, аби переконати брата в хибності його пропозиції? 11. Прочитайте уривок з літературного твору: «На військовому кладовищі на одному з білих хрестів є напис: "Ласло Гаргань". Там спить вічним сном гонвед, який під час грабування гімназійних колекцій випив увесь денатурат з посудини, де були заспиртовані різні плазуни. Світова війна винищувала людське покоління навіть настоянкою з гадів» (Я. Гашек. Пригоди бравого вояка Швейка). Поясніть, що таке денатурат. Назвіть причини, які могли призвести до безславної загибелі піхотинця угорської армії. Скарбничка досвіду 1. Проаналізуйте зміст етикеток лікарських препаратів, косметичних засобів, побутових хімікатів, харчових продуктів. Визначте, які з них містять етанол або гліцерин. 2. Знайдіть інформацію про використання гліцерину для: а) вибавляння плям; б) збереження композицій з рослинного матеріалу й перевірте її експери-ментально. 3. Етанол - це шкідлива чи корисна речовина? Розробіть рекламу й антирекламу цього насиченого одноатомного спирту. За результатами виконаного дослідження підготуйте презентацію.
Зміст уроку
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум. |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: