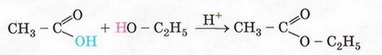|
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Хімія: Оцтова кислота, її молекулярна та структурна формули, фізичні властивості. Функціональна карбоксильна група. Хімічні властивості
ОЦТОВА КИСЛОТА, ЇЇ МОЛЕКУЛЯРНА ТА СТРУКТУРНА ФОРМУЛИ, ФІЗИЧНІ ВЛАСТИВОСТІ. ФУНКЦІОНАЛЬНА КАРБОКСИЛЬНА ГРУПА. ХІМІЧНІ ВЛАСТИВОСТІ: ЕЛЕКТРОЛІТИЧНА ДИСОЦІАЦІЯ, ВЗАЄМОДІЯ З ІНДИКАТОРАМИ, МЕТАЛАМИ, ЛУГАМИ, СОЛЯМИ, СПИРТАМИ. ЗАСТОСУВАННЯ
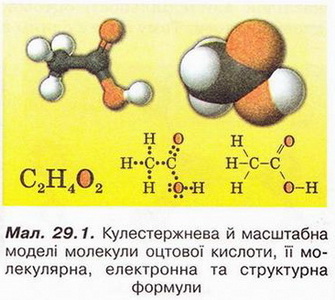
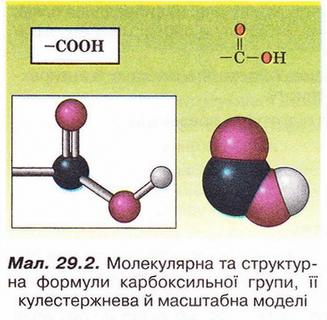
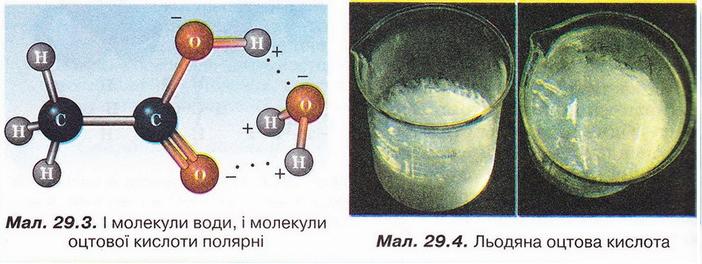
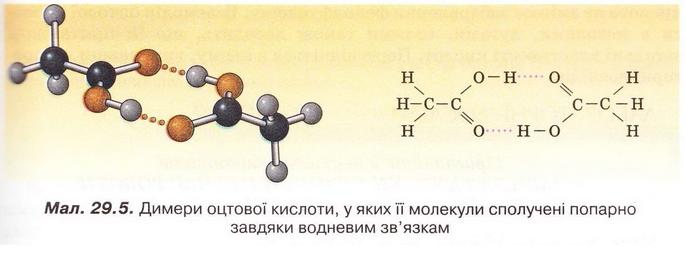
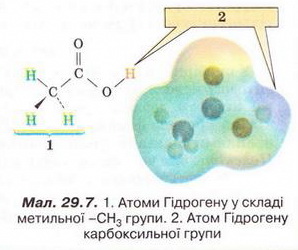
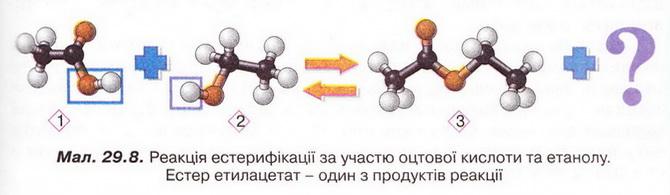
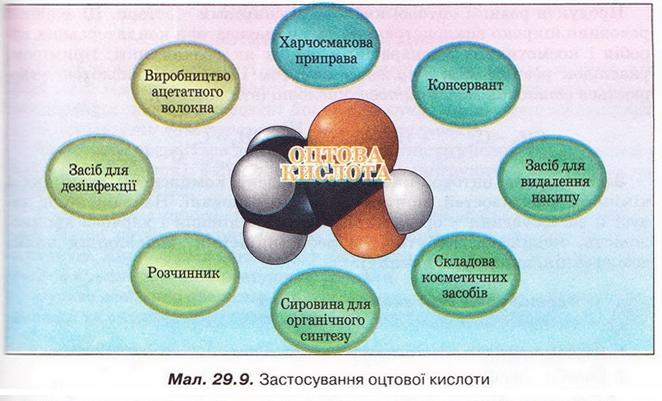
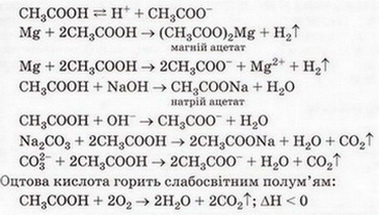
Оцтова кислота Після опрацювання § 29 ви зможете: складати й пояснювати молекулярні, електронні та структурні формули оцтової кислоти; збирати моделі її молекули; характеризувати склад, структуру, фізичні та хімічні властивості оцтової кислоти; ілюструвати властивості оцтової кислоти рівняннями хімічних реакцій; розрізняти карбонові кислоти за функціональними ознаками; наводити приклади застосування оцтової кислоти; встановлювати причинно-наслідкові зв'язки між складом, будовою, властивостями та біологічними функціями і застосуванням цієї сполуки; обґрунтовувати застосування оцтової кислоти її властивостями. На шляху до успіху пригадаємо з вивчених курсів хімії, біології та основ здоров'я: які органічні сполуки називають оксигеновмісними; що таке гомологічний ряд і функціональна група; для чого використовують бактерії в господарстві; чим чисті речовини відрізняються від сумішей; яке значення перших синтезів органічних сполук; що таке водневий зв'язок і як він позначається на властивостях речовин; які речовини називають кислотами і як їх виявляють у розчині; як класифікують кислоти за різними ознаками; з якими речовинами реагують кислоти і які речовини утворюються внаслідок цього; чим зумовлена світність полум'я; які правила безпечного поводження з побутовими хімікатами. • Карбонові кислоти, так само як і спирти, містять Оксиген, тобто належать до оксигеновмісних органічних сполук. Розгляньмо докладно властивості оцтової кислоти - другого члена гомологічного ряду (згадайте схему 22.1) одноосновних карбонових кислот (у сучасній науковій хімічній літературі вам траплятиметься й інша назва цієї речовини - етанова кислота). Ця речовина добре відома вам з повсякденного життя як складова харчосмакової приправи - оцту. • Молекулярна, електронна та структурна формули оцтової кислоти наведені на малюнку 29.1. До складу молекули оцтової кислоти входять два атоми Оксигену. Один з них міститься в гідроксильній групі. Другий атом Оксигену сполучений подвійним зв'язком з тим самим атомом Карбону, до якого приєднана й гідроксильна група. Групу атомів C=O називають карбонільною групою. Поєднавши фрагменти слів карбонільна і гідроксильна, дістанемо назву функціональної групи карбонових кислот. Склад і будову карбоксильної групи наведено на малюнку 29.2. Завдання Запишіть електронну формулу карбоксильної групи. • Фізичні властивості оцтової кислоти повною мірою науковці змогли дослідити лише після того, як виокремили цю речовину з її водного розчину (поясніть, чому). Дослідники з'ясували, що оцтова кислота - безбарвна прозора гігроскопічна рідина, яка необмежено розчиняється у воді. Оцтова кислота змішується з багатьма розчинниками, у ній розчиняється чимало органічних речовин. Завдання Роздивіться малюнок 29.3 і поясніть, які зв'язки виникають між молекулами води и оцтової кислоти. Чи розчинятимуться в оцтовій кислоті леткі сполуки галогенів з Гідрогеном? Обґрунтуйте свою думку. Температура плавлення оцтової кислоти становить 16,6 °С, замерзла вона нагадує лід, тому її кристали називають льодяною оцтовою кислотою (мал. 29.4). Вперше її добув російський хімік і фармацевт Товій Ловіц, виокремивши з водного розчину виморожуванням. Густина оцтової кислоти за температури 20 °С становить 1,05гсм3 Температура кипіння цієї сполуки сягає 118,1 °С - адже між молекулами оцтової кислоти утворюються водневі зв'язки (мал. 29.5). Натомість характерний кислий смак і різкий запах оцтової кислоти відомі з сивої давнини. Етиловий спирт, який міститься в пиві чи вині внаслідок життєдіяльності оцтовокислих бактерій перетворюється на оцтову кислоту. Тому оцет є одним з найдавніших продуктів мікробіологічного синтезу. Приміром, у Давньому Вавилоні за 5000 років до н. е. оцет виготовляли з фініків, а в Китаї він відомий з III ст. до н. е. 1864 р. участь бактерій у перетворенні спирту на оцет довів Луї Пастер (мал. 29.6). Нині в країнах Євросоюзу харчовим є лише той оцет, який добуто методом мікробіологічного синтезу з харчової спиртовмісної сировини. • Хімічні властивості оцтової кислоти зумовлені складом і будовою цієї речовини. Оцтова кислота одноосновна, тобто в її молекулі лише один атом Гідрогену (за малюнком 29.7 визначте, який саме) здатен заміщуватися на атоми металічних елементів і відщеплюватися під час електролітичної дисоціації. Оцтова кислота - слабкий електроліт, лише незначна частка її молекул розпадається на катіони Гідрогену й ацетат-аніони: СН3СООН ⇔ Н+ + СН3СОО-. У рівняннях реакцій хімічну формулу оцтової кислоти записують у молекулярній формі - адже її водному розчині переважно містяться молекули цієї речовини. Тим не менш катіонів Гідрогену у водному розчині оцтової кислоти достатньо, аби під їхньою дією змінилося забарвлення індикаторів. Метиловий оранжевий, фіолетовий лакмус й універсальний індикаторний папір набувають відтінків світло-червоного кольору. Як і неорганічні кислоти, оцтова кислота не змінює забарвлення фенолфталеїну. Взаємодія оцтової кислоти з металами, лугами, солями також доводить, що їй притаманні загальні властивості кислот. Пересвідчіться в цьому, виконавши лабораторні досліди. ЛАБОРАТОРНІ ДОСЛІДИ Пригадайте й неухильно виконуйте ПРАВИЛА ТЕХНІКИ БЕЗПЕКИ ПІД ЧАС РОБОТИ З ОБЛАДНАННЯМ І РЕАКТИВАМИ № 9. Дія оцтової кислоти на індикатори Завдання Дослідіть і порівняйте дію оцтової та хлоридної кислот на індикатори. Обладнання: штатив з пробірками (або пластина із заглибинами). Реактиви: столовий оцет; хлоридна кислота; розчини індикаторів (метилового оранжевого, фенолфталеїну, лакмусу; універсальний індикаторний папір). Інструкція У пробірки (або заглибини пластини) внесіть по 5 крапель розчину оцтової кислоти і добавте по 1-2 краплі розчинів індикаторів. Краплю оцтової кислоти нанесіть на універсальний індикаторний папір. Те саме проробіть з хлоридною кислотою. Чи однаково діють ці кислоти на індикатори? Яка з них є сильним електролітом, а яка - слабким? № 10. Взаємодія оцтової кислоти З металами, лугами, солями Завдання Дослідіть і порівняйте взаємодію оцтової і хлоридної кислот з магнієм, натрій гідроксидом у розчині, натрій карбонатом (кальцій карбонатом, натрій гідрогенкарбонатом). Обладнання: штатив з пробірками або пластина із заглибинами. Реактиви: столовий оцет; хлоридна кислота; магній (порошок або ошурки); кристалічний натрій карбонат (кальцій карбонат, натрій гідрогенкарбонат); розчини фенолфталеїну та натрій гідроксиду. Інструкція У пробірки (або заглибини пластини) внесіть по 5 крапель розчину оцтової кислоти. До першої пробірки (або заглибини) з розчином оцтової кислоти добавте трохи магнію (10-12 крупинок), до другої - кілька крапель фенолфталеїну. Далі до другої пробірки (заглибини) краплями додавайте розчин натрій гідроксиду до зміни забарвлення. Поясніть, для чого до кислоти попередньо було добавлено фенолфталеїн. До третьої пробірки добавте трохи кристалічного натрій карбонату (або кальцій карбонату, натрій гідрогенкарбонату). Те саме проробіть з хлоридною кислотою. Завдання Перетворіть схеми пророблених реакцій за участю оцтової кислоти на хімічні рівняння, запишіть їх у йонній формі: Мg + СН3СООН → (СН3СОО)2Мg + Н2↑ СН3СОО +NaОН → СН3СООNа + Н20 NaCO3 + СН3ООН → СН3СООNa + Н20 + С02↑ Виконавши лабораторні досліди, ви пересвідчилися, що оцтовій кислоті притаманні ті самі загальні властивості, що й відомим вам неорганічним кислотам. Однак слід пам'ятати: оцтова кислота - органічна речовина, тому ця неї характерна реакція горіння (повного окиснення). Наллємо в пробірку трохи чистої оцтової кислоти й нагріємо її (пригадайте, за якої температури кипить оцтова кислота). Не припиняючи нагрівання, підпалімо палаючою скіпкою пару оцтової кислоти. Вона горить слабосвітним полум'ям. Завдання 1. Запишіть рівняння реакції горіння оцтової кислоти. 2. Обчисліть масову частку Карбону в оцтовій кислоті й поясніть характер її горіння. • Взаємодія зі спиртами - реакція, яка вкотре переконає вас у тому, по хімічні властивості оцтової кислоти, метанолу та етанолу (і багатьох інших сполук) зумовлені функціональними групами цих речовин. У пробірку наллємо концентровану оцтову кислоту (есенцію) об'ємом 0,5 мл і таку саму порцію етанолу. Навіть за нагрівання не можна виявити змін, які свідчили б про перебіг реакції. Якщо в пробірку добавити концентровану сульфатну кислоту об'ємом 0,5-1 мл, відчуємо приємний фруктовий запах, який посилюється під час подальшого нагрівання реакційної суміші. Цей запах властивий одному з продуктів реакції - етиловому естеру оцтової кислоти (етилацетату) (мал. 29.8,3): Який другий продукт реакції естерифікації? Висновок про це можна легко зробити, пригадавши, що під час складання хімічних рівнянь використовують закон збереження маси. З огляду на це за схемою, наведеною на малюнку 29.8, легко визначити, що, окрім естеру, утворюється вода. Реакцію естерифікації можна провести, використавши як каталізатор безводний купрум(ІІ) сульфат. Поясніть, чому поступово внаслідок перебігу реакції з'являється синє забарвлення. За потреби зверніться до § 5. Подібно до розглянутої реакції відбувається реакція естерифікації за участю оцтової кислоти та метанолу: СН3СООН + НО – СН3 ⇔ СН3СООСН3 + Н20. Продукт взаємодії - метилацетат - також має приємний фруктовий запах. Реакцію оцтової кислоти зі спиртами важливо було вивчити не лише тому, що її продукти - естери - широко використовують як розчинники та ароматизатори у складі парфумів і харчових продуктів. Здобуті знання допоможуть вам зрозуміти, як відбувається перетравлювання і синтез жирів у живих організмах. Про це йтиметься в наступному параграфі. • Застосування оцтової кислоти зумовлене комплексом фізичних і хімічних властивостей, притаманних цій речовині. Завдання Проаналізуйте пункт цього параграфа, у якому описано фізичні властивості оцтової кислоти. Назвіть властивості, які, на вашу думку, використовують: а) у побуті; б) у промисловості й органічному синтезі. Досліджені вами хімічні властивості оцтової кислоти люди здавна застосовують у повсякденному житті. Досвідчені господині добавляють оцет до страв зі столового буряка й червонокачанної капусти не лише для того, аби надати страві гостроти, а й задля привабливого червоного кольору. Завдання Пригадайте досліди з природними індикаторами й поясніть обґрунтованість дій господинь. Висловіть припущення, чому дієтологи радять використовувати у харчуванні оцет не синтетичного, а природного походження або лимонний сік. У разі потрапляння на шкіру розчину лугу його змивають великою кількістю води й промивають уражене місце розбавленим водним розчином оцтової кислоти. Слід пам'ятати, що льодяна та концентрована оцтова кислота (есенція) самі можуть спричинити хімічні опіки, пара оцтової кислоти сильно подразнює слизові оболонки, дихальні шляхи. Для полегшення стану потерпілого використовують розчин питної соди. «Гасіння» питної соди оцтом потрібне й для розпушування тіста. Видалення за допомогою оцту накипу зі стінок посуду ґрунтується на реакції оцтової кислоти з кальцій карбонатом. Цікаво? У Стародавньому Римі дію оцтової кислоти на свинець використовували для виготовлення солодкого густого напою. Скисле вино наливали у свинцеві горнятка й витримували певний час. Римські аристократи істотно вкорочували собі життя, ласуючи цим трунком. Адже солодкого смаку йому надавав так званий свинцевий цукор - отруйний плюмбум(ІІ) ацетат, який утворювався внаслідок реакції. Галузі застосування оцтової кислоти наведено на малюнку 29.9. Стисло про головне Карбонові кислоти належать до оксигеновмісних органічних сполук. Функціональною групою карбонових кислот є карбоксильна група - СООН. Оцтова кислота - безбарвна прозора гігроскопічна рідина з характерним кислим смаком і різким запахом. Вона необмежено розчиняється у воді, між її молекулами й молекулами води утворюються водневі зв'язки. Оцтова кислота змішується з багатьма розчинниками, у ній розчиняється чимало органічних речовин. Температура плавлення оцтової кислоти 16,6 °С, густина за температури 20 °С - 1,05 г/см3, температура кипіння становить 118,1 °С. Між молекулами оцтової кислоти утворюються водневі зв'язки. Хімічні властивості оцтової кислоти зумовлені її складом і будовою. Вона - одноосновна кислота, слабкий електроліт. Оцтова кислота діє на індикатори, реагує з металами, лугами, солями подібно до неорганічних кислот: Продукти реакції оцтової кислоти зі спиртами - естери. Ці запашні речовини широко використовують як ароматизатори кондитерських виробів і косметичних препаратів, а також як розчинники. Приміром, унаслідок реакції між етиловим спиртом і оцтовою кислотою утворюється етиловий естер оцтової кислоти (етилацетат): Застосування оцтової кислоти зумовлене комплексом фізичних і хімічних властивостей, притаманних цій речовині. Найважливіші галузі її застосування - органічний синтез, кулінарія і харчова промисловість, медицина, побутові потреби (чищення, вибавляння плям, дезінфекція, видалення накипу). Застосуйте свої знання й уміння 1. Назвіть функціональну групу карбонових кислот. 2. Виберіть характеристики оцтової кислоти: А Слабкий електроліт; Б Має різкий запах; В Малорозчинна у воді; Г Негорюча речовина; Д Взаємодіє з калій гідроксидом. 3. Назвіть аніон у складі солей оцтової кислоти. 4. Запишіть рівняння реакції між оцтовою кислотою та метанолом. 5. Дев'ятикласник Сергій чув, що за допомогою оцтової кислоти вибавляють плями. На його магнієвій стругачці для олівців з'явилися темні плямки. Хлопець налив у пластиковий стаканчик оцту й поклав туди стругачку, аби надати їй первісного вигляду. Наступного дня Сергій зазирнув до стаканчика й дуже здивувався... Висловіть припущення, що так вразило хлопця. Як би ви пояснили Сергію його помилку? 6. Тимофій насипав на дно високого хімічного стакана шар питної соди і поставив на нього запалену свічку. Далі він почав обережно наливати у стакан невеликі порції оцту. Висловіть припущення щодо явищ, які відбулися внаслідок Тимофієвих дій, опишіть і поясніть їх. 7. Оленчина мама, аби прочистити злив умивальника, заливала в його отвір рідкий засіб «Кріт». Раптом частина їдкої рідини хлюпнула на руку. Жінка швидко змила її водою. Але далі завагалася: чим промити уражену ділянку - розчином питної соди чи розбавленим водою оцтом? А що порадите ви? Чому? 8.*Головні компоненти сплаву, з якого виготовляють деякі монети, - мідь цинк. Недосвідчені нумізмати намагаються за допомогою оцту очистити старі монети від нашарувань оксидів і карбонатів. Вони спостерігають не лише видалення цих сполук, а й появу осаду чистої міді на поверхні монети Поясніть явища, які відбуваються. За потреби зверніться до ряду активності металів (с. 105, мал. 14.4). Скарбничка досвіду 1. Дізнайтеся про різновиди оцту та його використання. З'ясуйте, де у світі є музеї оцту, які мистецькі твори присвячені цій харчосмаковій приправі. 2. Зніміть міні-фільм або створіть слайд-шоу «Як моя родина використовує оцет» За результатами досліджень підготуйте презентацію. Г. А. Лашевська, Геометрія, 9 клас
Зміст уроку
Если у вас есть исправления или предложения к данному уроку, напишите нам. Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум. |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: