|
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Фтор и хлор получают электролизом расплавов или растворов их солей. Например, процесс элек-| тролиза расплава хлорида натрия можно отразить уравнением:

Но если водород можно получить другими, более удобными и дешевыми способами, например из природного газа, то гидроксид натрия получают почти исключительно электролизом раствора поваренной соли, как и хлор.
Бром и иод получают в промышленности по реакции вытеснения их соответственно из бромидов и иодидов.
Биологическое значение галогенов. Их применение. Вы не могли не обратить внимание, что на этикетках многих марок зубных паст указывается на содержание в них фтора — конечно, не свободного, а его соединений. Благодаря этому важному компоненту, участвующему в построении зубной эмали и костей, предотвращается такое заболевание, как кариес зубов. Кроме того, фтор является необходимым элементом в процессах обмена веществ в железах, мышцах и нервных клетках.
Важное значение имеет фтор и в промышленном производстве, где основные потребители его — ядерная промышленность и электротехника. Его соединение Nа3АlF6 (как оно называется?) используется для производства алюминия. А в быту все более широкое применение находит тефлоновая посуда, название которой дано по фторсодержащей пластмассе — тефлону.
Хлор — один из химических элементов, без которых немыслимо существование живых организмов. Основная форма его. поступления в организм — это хлорид натрия. Он стимулирует обмен веществ, рост волос, придает бодрость и силу. Больше всего NаСl содержится в плазме крови.
Особую роль в пищеварении играет соляная кислота НС1, которая входит в состав желудочного сока. Без 0,2%-ной НСl практически прекращается процесс переваривания пищи. И хотя почти все пищевые продукты содержат некоторое количество поваренной соли, человек вынужден добавлять к пище ежедневно около 20 г соли.
По масштабам промышленного применения хлор намного превосходит все галогены. Хлор и его соединения необходимы для отбеливания льняных и хлопчатобумажных тканей, бумаги и т. д. Особенно много его расходуется в органическом синтезе для производства пластмасс, каучуков, красителей и растворителей (рис. 20).
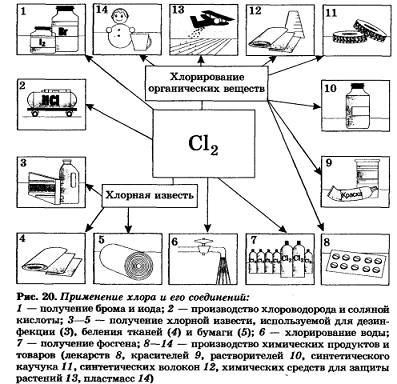
Многие хлорсодержащие соединения используют для борьбы с вредителями сельского хозяйства. В больших количествах хлор потребляется для обеззараживания питьевой воды, правда, далеко не без отрицательных последствий (какое вещество безопаснее применять для этой цели?). В цветной металлургии методом хлорирования руд извлекают из них некоторые металлы (титан, ниобий, тантал). Хлор нашел применение и в военных целях в качестве боевого отравляющего средства. Позднее он был заменен другими, более эффективными хлорсодержащими отравляющими веществами, например фосгеном СОСl2.
Хлор содержится в очень опасном для жизни и здоровья веществе — диоксине. Соединения хлора — одна из причин разрушения озонового слоя Земли.
Еще один галоген — бром также весьма важен для организма человека. Соединения этого элемента регулируют процессы возбуждения и торможения центральной нервной системы, поэтому для лечения нервных болезней (бессонницы, истерии, неврастении и т. д.) врачи прописывают «бром» — бромсодер-жащие препараты.
Бром активно накапливают некоторые растения, и в том числе морские водоросли. Именно в море сосредоточена большая часть брома на нашей планете, и море служит главным поставщиком брома. Подсчитано, что ежегодно вместе с морской водой в воздух переходит около 4 млн т брома. Понятно, что содержание его в воздухе приморских районов всегда больше, чем в районах, далеких от моря. Это одна из причин, почему так полезно дышать морским воздухом.
Не менее важную роль бром, а точнее, бромид серебра АgВr играет в фотографии. Те, кто занимается фотографией, вероятно, сразу же вспомнят названия сортов фотобумаги — «Уни-бром», «Бромпортрет» и др. Фотобумага содержит нанесенный на нее с помощью желатина слой бромида серебра, который легко разлагается под действием света:
2АgВr = 2Ag + Br2
И наконец, последний из рассматриваемых нами галогенов — иод — это тот элемент, без которого человек не может жить: недостаток его в воде и пище снижает выработку гормона щитовидной железы и приводит к заболеванию эндемическим зобом. Под регулирующим действием гормона щитовидной железы находятся мускульное возбуждение, биение сердца, аппетит, пищеварение, работа мозга и темперамент человека. Иод попадает в организм вместе с пищей: хлебом, яйцами, молоком, водой, морской капустой и с воздухом (особенно морским) при дыхании.
Спиртовой раствор иода (5—10% -ный), называемый йодной настойкой, применяется для обработки ран. Иод входит в состав многих лекарств.
Главными потребителями иода являются фармацевтичеcкая и химическая промышленность, а также производство светочувствительных фотоматериалов.
1. Получение галогенов электролизом расплавов и растворов солей.
2. Биологическое значение галогенов.
3. Применение хлора и соединений фтора, хлора и иода.
Какой объем хлора (н. у.) и какую массу натрия можно получить при электролизе 585 г хлорида натрия, содержащего 2% примесей?
Рассчитайте, сколько граммов 40%-ного раствора щелочи можно получить из натрия, массу которого вы определили в предыдущей задаче.
Французский химик Шееле получил хлор по реакции оксида марганца(IV) с соляной кислотой. В результате этой реакции образуются также хлорид марганца( II) и вода. Составьте уравнение этой реакции, рассмотрите окислительно-восстановительные процессы и рассчитайте массу оксида марганца(IV) и количество хлороводорода, необходимых для получения 100 л хлора (н. у.), если выход его составляет 95% от теоретически возможного.
Подготовьте сообщение о положительном и отрицательном значении галогенов в жизни человека.
Извечная заповедь медицины: «Малые дозы — лекарства, а большие — яд». Докажите ее на примерах из химии галогенов.
Английский поэт Уилфред Оуэн, погибший в сражениях Первой мировой войны, оставил такие строки:
Газ! Газ! Скорей! — неловкие движенья,
Напяливание масок в едкой мгле!
Один замешкался, давясь и спотыкаясь,
Барахтаясь, как в огненной смоле,
В просветах мутного зеленого тумана.
Бессильный как во сне, вмешаться и помочь,
Я видел только — вот он зашатался,
Рванулся и поник — бороться уж невмочь.
Какое событие описывает поэт? Какой галоген выступает в страшной роли убийцы? Какие его свойства упоминаются в стихотворении?
Используя свои знания по химии галогенов, напишите сочинение на тему «Художественный образ вещества или процесса». Для того чтобы иметь представление, как это делают другие ученики, прочитайте сочинение ученика 9 класса 531-й школы г. Москвы (1990) Ильи Горшкова «Самый сильный окислитель».
Жил-был Кислород. И был он таким сильным, что, с кем ни встретится, сразу окислит. И назвали Кислород окислителем, а вещества, получающиеся в реакции с кислородом, — оксидами, сам процесс — окислением. Ходит Кислород по таблице Менделеева и со всеми в реакцию вступает. Стал он хвастливым, заносчивым и решил, будто в химическом мире нет никого сильнее него. И воаже кислород ошибся. Как-то раз встретил он в таблице фтор. Решил Кислород окислить фтор. Позвал он на помощь водород и, образовав в соединении с ним воду, пошел в наступление на фтор. И произошло чудо. Вода, которой тушат пожары, сама загорелась во фторе. Кислород, считавшийся окислителем, в этой реакции стал восстановителем. Так фтор превзошел Кислород и оказался самым сильным из окислителей.
Какие химические понятия осветил Илья в своем сочинении? Выпишите их и дайте их определения.
опорный каркас урока химии 9 класса, шпаргалки по химии, рефераты по всем предметам
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|













