|
Гипермаркет знаний>>Химия>>Химия 7 класс>> Простые и сложные вещества. Типы простых веществ: металлы и неметаллы
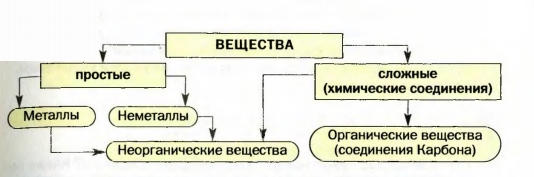
> различать простые и сложные вещества, органические и неорганические вещества; Вещество, образованное одним химическим элементом, называется простым, а вещество, образованное несколькими элементами, — сложным, или химическим соединением. Простые вещества делят на металлы и неметаллы. Такую классификацию простых веществ предложил выдающийся французский ученый A.Л. Лавуазье в конце XVIII в. Химические элементы, от которых происходят металлы, называют металлическими, а те, которые образуют неметаллы, — Простые вещества 13 элементов — Au, Ag, Cu, Hg, Pb, Fe, Sn, Pt, S, С, Zn, Sb и As были известны еще в древности. Каждый из вас может, не задумываясь, назвать несколько металлов (рис. 36). Они отличаются от остальных веществ особым «металлическим» блеском. Эти вещества имеют много общих свойств.
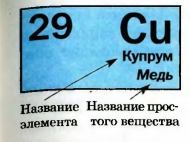
Благодаря своим свойствам металлы уверенно вошли в жизнь людей. Об их огромном значении свидетельствуют названия исторических эпох: медный век, бронзовый1 век, железный век. Сходство металлов обусловлено их внутренним строением. Строение металлов. Металлы — кристаллические вещества. Кристаллы в металлах намного мельче, чем кристаллы сахара или поваренной соли, и увидеть их невооруженным глазом невозможно. Атомы в металле «упакованы» очень плотно, поэтому часть электронов постоянно переходит от одних атомов к другим. Именно благодаря этим «свободным» электронам металлы проводят электрический ток. Атомы, которые теряют электроны, превращаются в положительно заряженные частицы — ионы (рис. 37). Простых веществ этого типа значительно меньше. К неметаллам относятся азот и кислород (компоненты воздуха), графит (стержни карандашей, материал электрических контактов), алмаз, сера и др. (рис. 38). Рис. 38. Неметаллы Внешне неметаллы отличаются от металлов прежде всего отсутствием металлического блеска. Только графит и иод имеют слабый блеск. Неметаллы не проводят электрический ток (исключение — графит). В обычных условиях половина неметаллов находится в газообразном состоянии, другие являются твердыми веществами и только бром — жидкостью. Ни одного металла-газа не существует. Неметаллы заметно отличаются друг от друга. Строение неметаллов. Часть неметаллов состоит из атомов. В алмазе, графите, красном фосфоре все атомы соединены друг с другом, а в инертных газах — гелии, неоне, аргоне, криптоне, ксеноне и радоне — разъединены. Другие неметаллы образованы молекулами 1. Молекула — электронейтральная частица, состоящая из двух или большего числа соединенных атомов. В каждой молекуле атомы соединены между собой достаточно прочно, а молекулы друг с другом в веществе — очень слабо. Поэтому вещества молекулярного строения имеют невысокие температуры плавления и кипения. Кислород и озон являются молекулярными веществами. Это простые вещества Оксигена. Молекула кислорода содержит два атома Оксигена, а молекула озона — три (рис. 39). Рис. 39. Модели молекул Большинство простых веществ называют так, как и соответствующие элементы. Если названия разные, то они приведены в периодической системе, причем название простого вещества расположено ниже названия ► Назовите простые вещества элементов Гидргена, Лития, Магния, Нитрогена. 1 Термин «молекула» происходит от латинского слова moles (масса), уменьшительного суффикса cula и в переводе означает «маленькая масса».
Соединение атомов разных химических элементов порождает множество сложных веществ (их в десятки тысяч раз больше, чем простых). Существуют сложные вещества с молекулярным, атомным и ионным строением. Поэтому их свойства очень разные. Молекулярные соединения в основном летучи, нередко имеют запах. Температуры их плавления и кипения значительно ниже, чем соединений с атомным или ионным строением. Молекулярным веществом является вода. Молекула воды состоит из двух атомов Гидрогена и одного атома Оксигена (рис. 41).
Некоторые соединения имеют атомное строение. Одним из них является минерал кварц, главная составляющая песка. В нем содержатся атомы Силиция и Оксигена (рис. 42).
В молекулах органических соединений, кроме атомов Карбона, содержатся, как правило, атомы Гидрогена, нередко — атомы Оксигена, иногда — некоторых других элементов. Взаимное притяжение многих противоположно заряженных ионов обуславливает существование ионных соединений. Ион, образовавшийся из одного атома, называют простым, а ион, который образовался из нескольких атомов, — сложным. Положительно заряженные простые ионы существуют для металлических элементов, а отрицательно заряженные — для неметаллических элементов. В учебнике до сих пор приводились технические или бытовые названия сложных веществ. Кроме того, вещества имеют и химические названия. Например, химическое название поваренной соли — натрий хлорид, а мела — кальций карбонат. Каждое такое название состоит из двух слов. Первым словом является название одного из элементов, которыми образовано вещество (оно пишется с маленькой буквы), а второе происходит от названия другого элемента. Раньше органическими веществами называли те вещества, которые содержатся в живых организмах. Это белки, жиры, сахар, крахмал, витамины, соединения, придающие цвет, запах, вкус овощам и фруктам, и др. Co временем ученые начали получать в лабораториях подобные по составу и свойствам вещества, которых нет в природе. Сейчас органическими веществами называют соединения Карбона (за исключением угарного и углекислого газов, мела, соды, некоторых других). Большинство органических соединений способны гореть, а при нагревании в отсутствие воздуха обугливаются (уголь почти полностью состоит из атомов Карбона). К неорганическим веществам принадлежат остальные сложные вещества, а также все простые. Они составляют основу минерального мира, т. е. содержатся в почве, минералах, горных породах, воздухе, природной воде. Кроме того, неорганические вещества есть и в живых организмах. Вам выданы такие вещества (вариант укажет учитель): вариант I — сахар, кальций карбонат (мел), графит, медь; Вещества находятся в банках с этикетками. Внимательно рассмотрите вещества, обратите внимание на их названия. Определите среди них простые (металлы, неметаллы) и сложные вещества, а также органические и неорганические. Внесите в таблицу название каждого вещества и укажите его тип, записав в соответствующих столбцах знак «+».
Вещества бывают простыми и сложными, органическими и неорганическими. Простые вещества делят на металлы и неметаллы, а химические элементы — на металлические и неметаллические. Металлы имеют немало общих свойств благодаря сходству их внутреннего строения. Неметаллы состоят из атомов или молекул и по своим свойствам отличаются от металлов. Сложные вещества (химические соединения) имеют атомное, молекулярное или ионное строение. Почти все соединения Карбона принадлежат к органическим веществам, а остальные соединения и простые вещества — к неорганическим веществам. 57. По каким физическим свойствам металл можно отличить от неметалла? 58. Дайте определение молекулы. Чем отличается молекула простого вещества от молекулы сложного вещества? 60. Заполните пропуски, вставив слова «элемент», «атом» или «молекула» в соответствующем падеже и числе: 61. Какими элементами образованы простые вещества фтор, цинк, фосфор, ртуть? Какие из названных элементов являются металлическими, а какие — неметаллическими? 62. Назовите простые вещества элементов, символы которых — Pb, Ca, He, Ag, В. 63. Какая ошибка допущена в выражении «В яблоках есть железо»? Предложите свой вариант, правильный относительно названий элементов и простых веществ. 64. Какие из веществ являются органическими, а какие — неорганическими: алмаз, вода, крахмал, витамин С (аскорбиновая кислота), халькозин (медная руда)? 65. Какими элементами образованы сложные вещества с такими химическими названиями: алюминий оксид, силиций нитрид, натрий гидрогенсульфид?
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. — К.: ВЦ «Академія», 2008. — 136 с.: іл. Содержание урока Если у вас есть исправления или предложения к данному уроку, напишите нам. Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|
||||||||||||||
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: