|
Гипермаркет знаний>>Химия>>Химия 10 класс>> Химия: Химическая связь
Учение о химической связи составляет основу всей теоретической химии.
Под химической связью понимают такое взаимо действие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы.
Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную.
Ионная химическая связь
Ионная химическая связь — это связь, образовавшаяся за счет электростатического притяжения катионов к анионам.
Как вы знаете, наиболее устойчивой является такая электронная конфигурация атомов, при которой на внешнем электронном уровне, подобно атомам благородных газов, будет находиться 8 электронов (или для первого энергетического уровня — 2). При химических взаимодействиях атомы стремятся приобрести именно такую устойчивую электронную конфигурацию и часто достигают этого или в результате присоединения валентных электронов от других атомов (процесса восстановления), или в результате отдачи своих валентных электронов (процесса окисления). Атомы, присоединившие «чужие» электроны, превращаются в отрицательные ионы, или анионы. Атомы, отдавшие свои электроны, превращаются в положительные ионы, или катионы. Понятно, что между анионами и катионами возникают силы электростатического притяжения, которые и будут удерживать их друг около друга, осуществляя тем самым ионную химическую связь.
Так как катионы образуют в основном атомы металлов, а анионы — атомы неметаллов, логично сделать вывод, что этот тип связи характерен для соединений типичных металлов (элементы главных подгрупп I и II групп, кроме магния и бериллия Ве) с типичными неметаллами (элементы главной подгруппы VII группы). Классическим примером является образование галогенидов щелочных металлов (фторидов, хлоридов и др.). Например, рассмотрим схему образования ионной связи в хлориде натрия:
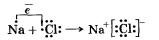
Два разноименно заряженных иона, связанные силами притяжения, не теряют способности взаимодействовать с противоположно заряженными ионами, вследствие чего образуются соединения с ионной кристаллической решеткой. Ионные соединения представляют собой твердые, прочные, тугоплавкие вещества с высокой температурой плавления.
Растворы и расплавы большинства ионных соединений — электролиты. Такой тип связи характерен для гидроксидов типичных металлов и многих солей кислородсодержащих кислот. Однако при образовании ионной связи не происходит идеального (полного) перехода электронов. Ионная связь является крайним случаем ковалентной полярной связи.
В ионном соединении ионы представлены как бы в виде электрических зарядов со сферической симметрией электрического поля, одинаково убывающего с увеличением расстояния от Центра заряда (иона) в любом направлении. Поэтому взаимодействие ионов не зависит от направления, то есть ионная связь, в отличие от ковалентной, будет ненаправленной.
Ионная связь существует также в солях аммония, где нет атомов металлов (их роль играет катион аммония).
Ковалентная химическая связь
Ковалентная химическая связь — это связь, возникаю щая между атомами за счет образования общих электронных пар.
В основе ее описания также лежит представление о приобретении атомами химических элементов энергетически выгодной и устойчивой электронной конфигурации из восьми электронов (для атома водорода из двух). Такую конфигурацию атомы получают не путем отдачи или присоединения электронов, как в случае ионной связи, а посредством образования общих электронных пар. Механизм образования такой связи может быть обменный или донорно-акцепторный.
Обменный механизм действует, когда атомы образуют общие электронные пары за счет объединения неспаренных электронов. Например:
1) Н2 — водород:
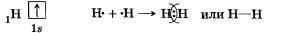
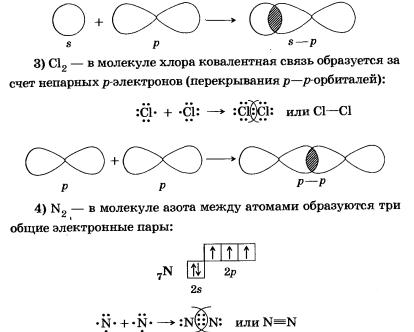
Связь возникает благодаря образованию общей электронной пары s-электронами атомов водорода (перекрыванию s-орбиталей):
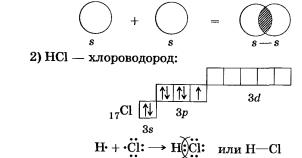
Связь возникает за счет образования общей электронной пары из s- и р-электронов (перекрывания s—р-орбиталей):
Донорно-акцепторный механизм образования ковалентной связи рассмотрим на классическом примере образования иона аммония NH4+:
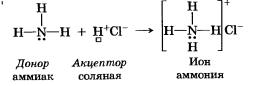
Донор имеет электронную пару, акцептор — свободную орбитальную, которую эта пара может занять. В ионе аммония все четыре связи с атомами водорода ковалентные: три образовались благодаря созданию общих электронных пар атомом азота и атомами водорода по обменному механизму, одна образовалась по донорно-акцепторному механизму. Все четыре связи N—Н в катионе аммония равноценны.
Аналогично образуется донорно-акцепторная связь в ионе метиламмония [СН3NH3]+.
Ковалентные связи классифицируют не только по механизму образования общих электронных пар, соединяющих атомы, но и по способу перекрывания электронных орбита-лей, по числу общих электронных пар, а также по смещению их к одному из связанных атомов.
По способу перекрывания электронных орбиталей различают ковалентные связи сигма- и пи.
В молекуле азота одна общая электронная пара образуется за счет сигма-связи (электронная плотность находится в одной области, расположенной на линии, соединяющей ядра атомов; связь прочная).
Две другие общие электронные пары образуются за счет я-связей, то есть бокового перекрывания р-орбиталей в двух областях; пи-связь менее прочна, чем сигма-связь.
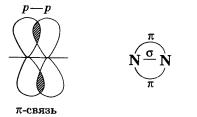
В молекуле азота между атомами существует одна сигма-связь и две пи-связи, которые находятся во взаимно перпендикулярных плоскостях (так как взаимодействуют 3 неспаренных р-электрона каждого атома).
Следовательно, о-связи могут образовываться за счет перекрывания электронных орбиталей:
s—s (Н2),
s-р (НСl),
р-р (Сl2),
а также за счет перекрывания «чистых» и гибридных орбиталей:
s-sр3 (СН4)
sр2—sр2 (С2Н4) и т. д.
По числу общих электронных пар, связывающих атомы, то есть по кратности, различают ковалентные связи:
1) одинарные:
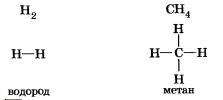
2) двойные:
СО,
о=с=о
оксид углерода (IV)
3) тройные:
С2Н2
НС=-СН ацетилен
По степени смещенности общих электронных пар к одному из связанных ими атомов ковалентная связь может быть неполярной и полярной. При неполярной ковалентной связи общие электронные пары не смещены ни к одному из атомов, так как эти атомы имеют одинаковую электроотрицательность (ЭО) — свойство оттягивать к себе валентные электроны от других атомов.
Ковалентную химическую связь, образующуюся между атомами с одинаковой электроотрицательностью, называют неполярной.
Посредством ковалентной неполярной связи образованы молекулы простых веществ-неметаллов.
Значения относительной электроотрицательности фосфора и водорода практически одинаковы: ЭО (Н) = 2,1; ЭО (Р) = = 2,1, поэтому в молекуле фосфина РН3 связи между атомом фосфора и атомами водорода ковалентные неполярные.
Ковалентную химическую связь между атомами элементов, электроотрицательности которых различаются, называют полярной
Например:
NH3
аммиак
Азот — более электроотрицательный элемент, чем водород, поэтому общие электронные пары смещаются к его атому.
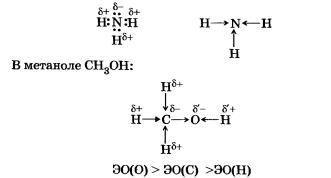
Следует различать полярность молекулы и полярность связи. Полярность связи зависит от значений электроотрицательности связанных атомов, а полярность молекулы зависит и от полярности связи, и от геометрии молекулы. Например, связи в молекуле углекислого газа С02 будут полярными, а молекула не будет полярной, так как имеет линейное строение.
Молекула воды Н20 полярна, так как образована с помощью двух ковалентных полярных связей Н—> 0 и имеет угловую форму. Валентный угол НОН составляет 104,5°, поэтому у атома кислорода с частичным отрицательным зарядом 6-и двумя неподеленными электронными парами формируется отрицательный полюс молекулы, а у атомов водорода с зарядом 6+ — положительный. Молекула воды — диполь.
Вещества с ковалентной связью характеризуются кристаллической решеткой двух типов:
атомной — очень прочной (алмаз, графит, кварц); молекулярной — в обычных условиях это газы, легколетучие жидкости и твердые, но легкоплавкие или возгоняющиеся вещества (Сl2, Н20, иод I2, «сухой лед» С02 и др.).
Внутримолекулярная ковалентная связь прочная, но межмолекулярное взаимодействие очень слабое, вследствие чего молекулярная кристаллическая решетка непрочная.
Металлическая связь
Связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке, называют металлической.
Такая связь ненаправленная, ненасыщенная, характеризуется небольшим числом валентных электронов и большим числом свободных орбиталей, что характерно для атомов металлов. Схема образования металлической связи (М — металл):
_
М0 — nе <-> Мn+
Наличием металлической связи обусловлены физические свойства металлов и сплавов: твердость, электрическая проводимость и теплопроводность, ковкость, пластичность, металлический блеск. Вещества с металлической связью имеют металлическую кристаллическую решетку. В ее узлах находятся ионы или атомы металла, между которыми свободно (в пределах кристалла) перемещаются электроны («электронный газ»).
Водородная связь
Химическую связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов, имеющих неподеленные электронные пары другой молекулы (или ее части), называют водородной.
Механизм образования водородной связи имеет частично электростатический, частично донорно-акцепторный характер. При наличии такой связи даже низкомолекулярные вещества могут быть при обычных условиях жидкостями (спирт, вода) или легко сжижающимися газами (аммиак, фтороводо-род).
В биополимерах — белках (вторичная структура) имеется внутримолекулярная водородная связь между карбонильным кислородом и водородом аминогруппы.
Молекулы полинуклеотидов — ДНК (дезоксирибонуклеиновая кислота) представляют собой двойные спирали, в которых две цепи нуклеотидов связаны друг с другом водородными связями. При этом действует принцип комплементарности, то есть эти связи образуются между определенными парами, состоящими из пуринового и пиримидинового оснований: против аденинового нуклеотида (А) располагается тиминовый (Т), а против гуанинового (Г) — цитозиновый (Ц).
Вещества с водородной связью имеют молекулярные кристаллические решетки.
Единая природа химической связи
Деление химических связей на типы носит условный характер, так как все они характеризуются определенным единством.
Ионную связь можно рассматривать как предельный случай ковалентной полярной связи.
Металлическая связь совмещает ковалентное взаимодействие атомов с помощью обобществленных электронов и электростатическое притяжение между этими электронами и ионами металлов.
В веществах часто отсутствуют предельные случаи химической связи (или «чистые» химические связи).
Например, фторид лития 1лК относят к ионным соединениям. Фактически же в нем связь на 80% ионная и на 20% ковалентная. Правильнее поэтому, очевидно, говорить о степени полярности (ионности) химической связи.
В ряду галогеноводородов НF — НСl — НВг — HI — НАt степень полярности связи уменьшается, ибо уменьшается разность в значениях электроотрицательности атомов галогена и водорода, и в астатоводороде связь становится почти неполярной (ЭО(Н) = 2,1; ЭО(Аг) = 2,2).
Различные типы связей могут содержаться в одних и тех же веществах, например:
1) в основаниях — между атомами кислорода и водорода в гидроксогруппах связь ковалентная полярная, а между металлом и гидроксогруппой — ионная;
2) в солях кислородсодержащих кислот — между атомами неметалла и кислородом кислотного остатка — ковалентная полярная, а между металлом и кислотным остатком — ионная;
3) в солях аммония, метиламмония и т. д. — между атомами азота и водорода — ковалентная полярная, а между иона-ми аммония или метиламмония и кислотным остатком — ионная;
4) в пероксидах металлов (например, Nа2O2) — связь между атомами кислорода ковалентная неполярная, а между металлом и кислородом — ионная и т. д.
Различные типы связей могут переходить одна в другую:
• при электролитической диссоциации в воде ковалент-ных соединений ковалентная полярная связь переходит в ионную;
• при испарении металлов металлическая связь превращается в ковалентную неполярную и т. д.
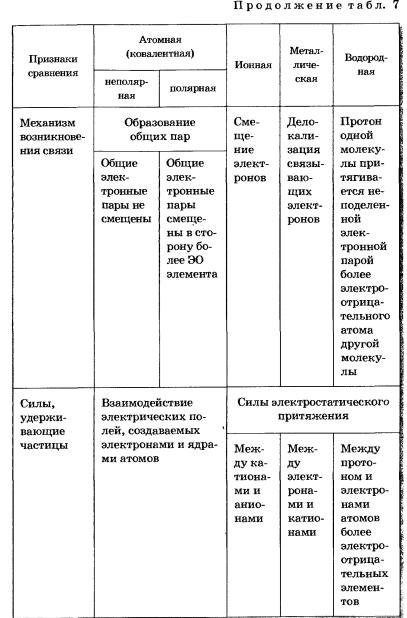
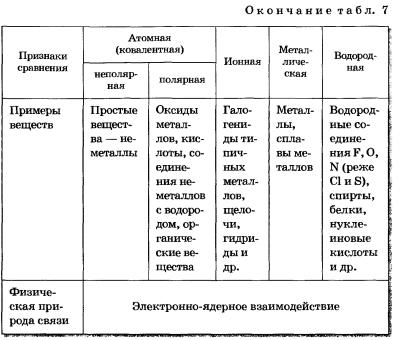
Причиной единства всех типов и видов химических связей служит их одинаковая физическая природа — электронно-ядерное взаимодействие. Образование химической связи в любом случае представляет собой результат электронно-ядерного взаимодействия атомов, сопровождающегося выделением энергии (табл. 7).
Таблица 7 Типы химической связи

1. Часто встречается выражение: «Молекулы благородных газов одноатомны». Насколько оно соответствует истине?
2. Почему, в отличие от большинства элементов-неметаллов, самые яркие представители их — галогены — не образуют аллотропных модификаций?
3. Дайте наиболее полную характеристику химической связи в молекуле азота, используя следующие признаки: ЭО связанных атомов, механизм образования, способ перекрывания электронных орбиталей, кратность связи.
4. Определите тип химической связи и рассмотрите схемы ее образования в веществах, имеющих формулы: Са, СаF2, F2, ОF2.
5. Напишите структурные формулы веществ: СО, СаС2, СS2, FеS2. Определите степени окисления элементов и их валентности (в возможных случаях) в этих веществах.
6. Докажите, что все типы химической связи имеют общую природу.
7. Почему молекулы N2, СО и С2Н2 называют изоэлектронными?
учебники основные и дополнительные по химии, обновление фрагмента в учебнике химии 11 класса, сборник конспектов уроков
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|