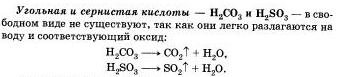|
Гипермаркет знаний>>Химия>>Химия 8 класс>> Химия: Кислоты С одним из представителей веществ этого класса вы уже познакомились, когда рассматривали летучие водородные соединения на примере хлороводорода HCl. Раствор его в воде и представляет собой соляную кислоту. Они имеет ту же формулу HCl. Аналогично при растворении в воде другого летучего водородного соединения — сероводорода H2S образуется раствор слабой сероводородной кислоты с формулой H2S.
Молекулы этих кислот состоят из двух элементов, то есть онн являются бинарными соединениями. Одннко к классу кислот относят также и соединения, состоящие из большего числи химических элементов. Кик привило, третьим элементом, входящим в состив кислоты, является кислород. Поэтому такие кислоты называют кислородсодержащими в отличие от HCl и H2S, которые называются бескислородными. Перечислим некоторые кислородсодержащие кислоты.
Обратите внимание, что все кислоты (н кислородсодержащие, и бескислородные) обязательно содержат водород, который в формуле записывается ня первом месте. Вся остальная часть формулы называется кислотным остатком. Например, у HCl кислотным остатком является Сl-.
Кислотами называются сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков.
Как правило, кислотные остатки образуют элементы-неметаллы.
По формулам кислот можно определить степени окисления атомов химических элементов, образующих кислоты.
Для бинарных кислот это сделать просто. Так как у водорода степень окисления +1. то в соединении H+1Cl-1 у хлора степень окисления -1, а в соединении H2+1S-2 у серы степень окисления -2.
Несложно будет рассчитать и степени окисления атомов элементов неметаллов, образующих кислотные остатки кислородсодержащих кислот. Нужно только помнить, что суммарная степень окисления атомов всех элементов в соединении равна нулю, а степени окисления водорода +1 и кислорода -2.
Зная степень окисления элемента-неметалла, образующего кислотный остаток кислородсодержащей кислоты, можно определить, какой оксид ей соответствует. Например, серной кислоте HgSO, в которой у серы степень окисления равна +6, соответствует оксид серы (VI) S03; азотной кислоте HN03, в которой у азота степень окисления равна +5, соответствует оксиl азота (V) NzOu.
По формулам кислот можно также определить и общий заряд, который имеют кислотные остатки. Заряд кислотного остатка всегда отрицателен и равен числу атомов водорода в кислоте. Число атомов водорода в кислоте называется основно стью. Для одноосновных кислот, содержащих один атом водорода, например HCl и HN08, заряды кислотных остатков равны 1-. Для двухосновных кислот, например H2SO4 и H2S, заряды кислотных остатков равны 2-, то есть
SO4 2- и S 2-.
В природе встречается много кислот: лимонная кислота в лимонах, яблочная кислота в яблоках, щавелевая кислота в листьях щавеля. Муравьи защищаются от врагов, разбрызгивая едкие капельки муравьиной кислоты. Она же содержится в пчелином яде и в жгучих волосках крапивы.
При скисании виноградного сока получается уксусная кислота, а при скисании молока — молочная кислота. Та же самая молочная кислота образуется при квашении капусты и при силосовании кормов для скота. Нам хорошо известны часто применяемые в быту лимонная и уксусная кислоты. Употребляемый в пищу уксус и представляет собой раствор уксусной кислоты.
Многие кислоты нужны в народном хозяйстве в огромных количествах, производство этих веществ называется многотоннажным. К их числу относятся серная и соляная кислоты.
Серная кислота S2SO4 — бесцветная жидкость, вязкая, как масло, не имеющая запаха, почти вдвое тяжелее воды. Серная кислота поглощает влагу из воздуха и других газов. Это свойство серной кислоты используют для осушения некоторых газов.
При смешивании серной кислоты с водой выделяется большое количество теплоты. Если воду вливать в серную кислоту, то вода, не успев смешаться с кислотой, может закипеть и выбросить брызги серной кислоты на лицо и руки работающего. Чтобы этого не случилось, при растворении серной кислоты нужно вливать ее тонкой струей в воду и перемешивать.
Серная кислота обугливает древесину, кожу, ткани. Если в пробирку с серной кислотой опустить лучинку, то происходит химическая реакция — лучинка обугливается. Теперь понятно, как опасно попадание брызг серной кислоты на кожу человека и одежду.
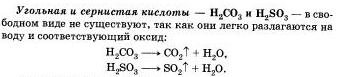
Растворы всех кислот кислые, но распознавать концентрированные кислоты на вкус не решится ни один химик — это опасно. Есть более эффективные и безопасные способы обнаружения кислот. Их так же, как и щелочи, распознают с помощью индикаторов.
Прильем к растворам кислот по нескольку капелек раствора лакмуса фиолетового цвета. Лакмус окрасится в красный цвет. Метиловый оранжевый при действии кислот меняет оранжевый цвет на красно-розовый.
А вот кремниевую кислоту, поскольку она нерастворима в воде, так распознавать нельзя.
1. Кислоты кислородсодержащие и бескислородные.
2. Кислотные остатки и основность кислот.
3. Сложные и простые ионы.
4. Соляная, сероводородная, серная, сернистая, угольная, азотная, азотистая, фосфорная и кремниевая кислоты.
5. Непрочные кислоты: утольивв и сернистая.
6. Индикаторы.
Дайте характеристику фосфорной кислоты по плану: а) формула; й) наличие кислорода; в) основность; г) растворимость; д)степени окисления элементов, образующих кислоту: е) заряд иона, образуемого киглотным остатком; ж) соответствующий оксид.
Почему нельзя лить воду в серную кислоту для ее разбавления?

конспект урока химии 8 класса, задачи по всем предметам, учебники химии
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|