|
Хімія — наука, котра вивчає речовини, їх будову, властивості, застосування і перетворення речовин. Дана наука досліджує молекулярно-атомні перетворення речовин, тобто, при яких молекули одних речовин руйнуються, а на їх місці утворюються молекули інших речовин з новими властивостями. Сьогодні не можна назвати жодної сфери виробництва, де б людина не стикалася з хімією. Практично все життя суспільства пов'язані з численними речовинами, що нас оточують, і хімічними процесами, що відбуваються навколо нас і всередині нас. Хімічними знаннями повинна володіти кожна цивілізована людина. Без них неможливаекологічно грамотна поведінка в побуті, в природі, на виробництві.
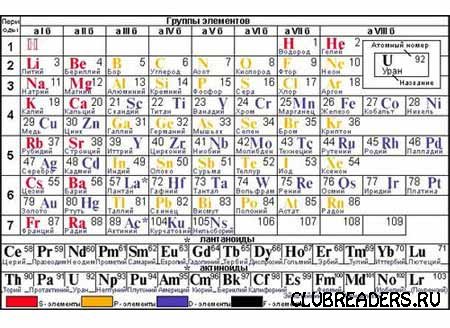
Завдання хімії - досліджувати властивості елементів і хімічних сполук, вивчати залежності властивостей речовин від їх складу й будови, вивчати умови перетворення одних речовин в інші, поширення хімічних речовин у природі, технологій їх одержання, механізмів взаємодії хімічних сполук, а також практичне використання хімічних реакцій. Назва хімія походить від араб. کيمياء. Це арабське слово пішло від єгипетського Chemi чи Kimi (стародавня назва Єгипту), що означало "чорний". Виділяють такі основні розділи: загальна хімія; неорганічна хімія; органічна хімія; аналітична хімія; фізична хімія: електрохімія, радіохімія, колоїдна хімія, механохімія; біологічна хімія , біоорганічна хімія, фармацевтична хімія , клінічна біохімія токсикологічна хімія , теоретична хімія , квантова хімія, комп'ютерна хімія, математична хімія, обчислювальна хімія, хемоінформатика, молекулярна динаміка, молекулярна механіка, радіохімія, геохімія. Поняття атому є базовим у хімії. Атом - це найменша частинка хімічного елемента, яка зберігає всі його хімічні властивості. Він складається з щільного ядра з позитивно заряджених протонів та електрично нейтральних нейтронів, яке оточене набагато більшою хмарою негативно заряджених електронів. Якщо число протонів відповідає числу електронів - атом електрично нейтральний; в іншому випадку це - іон, з певним зарядом. Атоми систематизують відповідно до числа протонів та нейтронів: число протонів визначає хімічний елемент, а число нейтронів визначає нуклід елементу. Періодична система елементів: Хімічний елемент — тип атомів з однаковим зарядом атомних ядер і певною сукупністю властивостей. Молекула—найменша частинка простої або складної речовини, котра здатна до самостійного існування й має її основні хімічні властивості, які визначаються її складом та будовою. Молекула складається з атомів. Хімічні властивості — властивості, які проявляються в ході хімічної реакції: здатність реагувати з іншими речовинами, а також схильність до розкладу Хімічна реакція — це перетворення речовин, коли молекули одних речовин руйнуються і на їхньому місці утворюються молекули інших речовин з іншим атомним складом. Хімічні реакції зображують у вигляді хімічних рівнянь. Реакції супроводжуються розривом старих та утворенням нових хімічних зв'язків
Історія хімії Хімія почалася з відкриття людиною здатності вогню змінювати природні матеріали. Виплавлялась мідь і бронзу, обпалювались глиняні вироби, люди почали отримувати скло ще за 4000 років до н. е. З 7 ст. до н. е. В Єгипті і Месопотамії утворився центр виробництва барвників, в чистому вигляді золото, срібло і інші метали. Приблизно з 1500 до 350 до н. е. для виробництва барвників використовували перегонку, а метали виплавляли з руд, змішуючи їх з деревним вугіллям і продуваючи через суміш, що горить — повітря. Самим процедурам перетворення природних матеріалів давали містичне значення. Аристотель Фалес Мілетський зводив все різноманіття явищ і речей до єдиної першостихії — води. Саме через нього хімічні ідеї проникли в Грецію. Проте грецькі філософи цікавились не способом отримання речовин і їх практичним використанням, суттю виникаючих в світі процесів. Древньогрецький філософ Анаксімен (585—525 до н. е.) вважав першоосновою Всесвіту повітря, що при розрідженні повітря перетворюється у вогонь, а по мірі згущення стає водою, потім землею і, нарешті, каменем. Геракліт Ефесський (кінець 6 початок 5 віків. до н. е.) намагався пояснити явища природи й визначив вогонь п'ятим елементом. В натурфілософії Емпедокла з Агрігента (490—430 до н. е.), котра володарювала більш двох тисячоліть. Згідно Емпедоклу, всі матеріальні об'єкти утворюються при з'єднанні вічних і незмінних елементів-стихій: води, повітря, землі і вогню під дією космічних сил любові (тяжіння) і ненависті (відштовхування). Цю теорію розвинули Платон й Аристотель. Згідно вченню Аристотеля, елементи-стихії - це не матеріальні субстанції, вони є носіями певних якостей: тепла, холоду, сухості і вогкості. Це вчення трансформувалося в ідею чотирьох «соків» Галена і побутувало в науці аж до 17 ст. Важливим в той час було питання про подільність матерії. Щодо нього виникли вчення Левкіппа та Демокріта, Епікура, які вважали, що існують тільки пустота і атоми — неподільні матеріальні елементи, незруйновані, вічні, непроникні, котрі відрізняються формою, положенням в просторі і величиною. Ця теорія дістала назву «атомістичної» й була непопулярною протягом двох тисячоліть після Демокріта, але не зникла повністю. Древньогрецький поет Тіт Лукрецій Кар розкрив її в поемі «Про природу речей» (De Rerum Natura). 3-7 ст. – період алхімії, мистецтва вдосконалення речовини через перетворення металів в золото і вдосконалення людини шляхом створення еліксиру життя. Алхіміки розв'язали багато практичних задач, відкрили багато нових процесів, спостерігали різноманітні реакції, сприяючи становленню нової науки хімії. Саме у 7-9 ст. з'явилися перші хіміки. Найбільш талановитим і прославленим арабським алхіміком був Джабір ібн Хайян (кінець 8 ст.), пізніше він здобув популярність та повагу в Європі під іменем Гебер. Він був переконаним, що сірка і ртуть є двома протилежними початками, з яких утворюються сім інших металів; важче від усього утворюється золото: для цього потрібна особлива речовина, яку греки називали xerion «сухий», а араби змінили на al-iksir (так з'явилося слово «еліксир»). Еліксир повинен був мати чудодійними властивостями: виліковувати від всіх хвороб і давати безсмертя. Наукові досягнення арабів досягли Середньовічної Європи у 12 ст. через Північну Африку, Сицилію і Іспанію. Роботи арабських алхіміків перекладені латинською й іншими європейськими мовами. Англійський філософ і дослідник, чернець — францисканець Роджер Бекон став важливою персоною хімії 13 століття, він передбачив багато подальших відкриттів: вивчав властивості селітри і багатьох інших речовин, знайшов спосіб виготовлення чорного пороху. Відомими алхіміками були й Арнальдо да Вілланов, Раймонда Луллій, Василь Валентин. В Західній Європі 12-13 ст. відбувався значний виток розвитку науки і промисловості. Рецепти алхіміків використовувалися в таких технологічних процесах, як обробка металів. В цей час починаються систематичні пошуки способів отримання і ідентифікації нових речовин, з'являються рецепти виробництва спирту і удосконалення процесу його перегонки. Важливим досягненням того часу - відкриття сильних кислот сірчаної, азотної. Було здійснено багато нових реакцій і отримано такі речовини, як солі азотної кислоти, купорос, солі сірчаної і соляної кислот. До кінця 14 ст. інтерес алхіміків до трансформація одних речовин в інші став менш популярним, адже збільшувався інтерес до виробництва міді, латуні, оцту, оливкового масла і різних ліків. В кінці середніх віків популярною стала ятрохімія, суть якої полягала у тому, що медицина - це справа хімії, і все залежить від здатності лікаря виділяти чисті речовини з нечистих субстанцій, всі функції організму зводяться до хімічних процесів, алхімік повинен знайти і приготувати хімічні речовини для медичних потреб. Основні представники ятрохімічного напряму: Ян Гельмонт; Франциск Сильвій; Андреас Лібавій. В 17 столітті вчені повернулись до найдавніших поглядів. Однин з найвидніших вчених авторів нової теорії філософ і математик Рене Декарт , який вважав, що всі тіла «складаються з численних дрібних часток різної форми і розмірів,… які не настільки точно прилягають один до одного, щоб навколо них не залишалося проміжків; ці проміжки не пусті, а наповнені… розрідженою матерією». Апротивником декарта був Гассенді, вчення - по суті переказ вчення Епікура, проте цей вчений визнавав створення атомів Богом; він вважав, що Бог створив певне число неподільних і непроникних атомів, з яких і складаються всі тіла; між атомами повинна бути абсолютна пустота. В 17 ст. ірландський вчений Роберт Бойль застосовував експериментальний підхід до визначення хімічних елементів (який зрештою і був прийнятий), описав сконструйований ним повітряний насос і досліди з визначення пружності повітря за допомогою U-подібної трубки. Внаслідок цього було сформульовано відомий закон про зворотну пропорційність об'єму і тиску повітря. У 1668 Бойль став дійсним членом щойно організованого Лондонського королівського товариства, а в 1680 був обраний його президентом. Протягом 16 ст. з розширенням споживання спиртних напоїв удосконалюються методи перегонки, конструюються нові перегінні апарати, з'явились численні виробничі лабораторії, передусім металургійні. Визначні хіміки-технологи — Ванноччо Бірінгуччо, Ґеорґ Аґріколо, Йогана Глаубер. У 18 столітті хімію почали викладати в начальних закладах. У 1675 був виданий підручник Ніколя Лемері (1645—1715) «Курс хімії. У 18 ст. в Європі утворюються наукові хімічні товариства і велика кількість наукових інститутів. Дослідження, що проводяться в них тісно пов'язані з соціальними і економічними потребами суспільства. З'явлись хіміки-практики, котрі займались виготовленням приладів і отриманням речовин для промисловості. Виникає теорія флогістону. Йоган Йоахим Бехер спробував дати раціоналістичне пояснення горючості. Він передбачив, що тверді речовини складаються з трьох видів «землі», і один з видів, названий ним «жирною землею», прийняв на себе «можливість горючості». Георг Ернст Шталь трансформував цю концепцію «жирної землі» в узагальнену доктрину флогістона — «початку горючості». Флогістон - це деяка субстанція, що міститься у всіх горючих речовинах і що вивільняється при горінні. Згідно вченню хіміка, корозія металів подібна до горіння дерева. Метали містять флогістон, а іржа вже не містить флогістону. Це даво зрозуміле пояснення процесу перетворення руд в метали: руда, вміст флогістону в якій незначне, нагрівається на деревному вугіллі, багатому флогістоном, і останній переходить в руду. Важливу роль у розвитку хімії 18-го століття відіграв Михайло Ломоносов , який провів знамениті досліди з випалювання металів в закритій посудині, що дало незаперечний доказ збереження речовини при хімічних реакціях і ролі повітря в процесах горіння: збільшення ваги, що при цьому спостерігається він пояснював з'єднанням їх з повітрям. Пружність газів хімік пояснив рухом часток. Такі поняття як «корпускула» (молекула) і «елемент» (атом) Михайло Ломоносов розмежовував, це отримало загальне визнання лише в середині 19 ст. Також хімік сформулював принцип збереження матерії і руху, заклав основи фізичної хімії , виключив флогістон з числа хімічних елементів. Великих успіхів у виділенні газів і вивченні їх властивостей досяг Джозеф Прістлі , котрий виявив, що гази можуть розчинятися у воді, і спробував збирати їх не над водою, а над ртуттю. Великий французький хімік Антуан Лоран Лавуазьє стверджував, що повітря –це не проста речовина, а суміш двох газів, одне з них «дефлогістроване повітря». Протягом 1780-х років Лавуазье в співпраці з іншими французькими хіміками Антуаном Франсуа де Фуркруа, Гітоном де Морво і Клодом Луї Бертолле розробив логічну систему хімічної номенклатури; в ній було описано більше 30 простих речовин з вказівкою їх властивостей. Цю працю, «Метод хімічної номенклатури», було опубліковано в 1787. Процеси 18 сталіття називають хімічною революцією. 19 століття Англійський хімік Джон Дальтон виявив, що два елементи можуть сполучатися один з одним в різних співвідношеннях і кожна нова комбінація елементів дає нове з'єднання й у 1808 він детально виклав свою атомну теорію. В той же час французький хімік Жозеф Луї Люссак опублікував припущення про те, що об'єми газів, вступаючих в реакцію один з одним, відносяться між собою як прості кратні числа. На жаль, Дальтон не зумів побачити користі у відкритті Люссака, крім перешкоди для розробки своєї теорії, хоч ці висновки могли б стати дуже плідними у визначенні відносної атомної ваги. Протягом 17 ст. хіміки наслідували ідеї Бехера і Шталя, котрі класифікували всі речовини відповідно до їх здатності реагувати зі специфічними кислотами. На початку 19 ст. з відкриттям нового аналітичного методу виникли нові ідеї: Гемфрі Деві пропустив електричний струм, що отримувався від батареї з 250 металевих пластин, через розплавлений карбонат калію і отримав маленькі кульки металу, згодом названого калієм, а потім таким же способом виділив з соди натрій. Деві передбачив, що хімічна спорідненість зводиться до електризації атомів при контакті. Шведський хімік Йонс Якоб Берцеліус розвинув уявлення про атом і електричну спорідненість, а також те, що, якщо солі в розчині під дією електричного струму розкладаються на негативні і позитивні компоненти, то всі з'єднання повинні складатися з позитивних і негативних частин радикалів. У 1860 відбувся перший Міжнародний хімічний конгрес в Карлсруе , де італійський хімік Станіслао Канніццаро знову повернув до життя забуту гіпотезу про те, що виходячи з відкриття Люссаком закону об'ємних відношень, передбачив, що рівні об'єми газів містять однакове число молекул. Дмитро Менделєєв опублікував свою періодичну таблицю. Всі відомі елементи він розташував відповідно до збільшення їх атомної ваги і розбив на періоди і групи, що відповідають зміні валентності. У таблиці були залишені пусті місця для ще невідкритих елементів. Точність періодичного закону була підтверджена відкриттями галію у 1875, ідентичного за своїми властивостями екаалюмінію, скандію (екабору) в 1879 і германію (екакремнію) в 1886. У 18 столітті питання про хімічні взаємовідносини організмів і речовин виходило із вчення, що розглядало життя як особливе явище, що підкоряється не законам світобудови, а впливу особливих життєвих сил. У 1828 німецький хімік Фрідріх Велер отримав сечовину — продукт життєдіяльності людини і тварин. У 1845 Адольф Кольбе, учень Велера, синтезував оцтову кислоту з початкових елементів вуглецю, водню і кисню. П'єр Бертло вів систематичну роботу з синтезу органічних сполук і отримав метиловий і етиловий спирти, метан, бензол, ацетилен. Фрідріх Август Кекуле у 1867 визначив органічну хімію як хімію сполук вуглецю. Юстус Лібіх узагальнив ці знання й разом з французьким хіміком Жаном Батистом Дюма уточнив уявлення про радикал як про специфічну незмінну групу атомів, що входить до складу багатьох органічних сполук (приклад радикал CH3). Стало зрозуміло, що визначити будову великих молекул можна, лише встановивши будову певного числа радикалів. У 1853 вчені зробили спробу класифікувати всі органічні сполуки. Шарль Фредерік Жерар узагальнив «теорію типів» й виділив чотири основних типи атомних груп, з яких, на його думку, і складаються як органічні, так і неорганічні сполуки. У 1857 Кекуле передбачив, що вуглець чотиривалентний і тому може сполучатися з чотирма іншими атомами, утворюючи довгі ланцюги прямі або розгалужені. Тому органічні молекули стали зображати не у вигляді комбінацій радикалів, а у вигляді структурних формул атомів і зв'язків між ними. До 1860-го року працями Кекуле і Бутлерова було закладено основу структурної хімії, це дозволяло пояснювати властивості речовин. До кінця 19 ст. ідеї структурної хімії були підкріплені даними, отриманими спектроскопічними методами. До 1900 концепція об'ємної організації молекул складних органічних і неорганічних сполук була прийнята практично всіма вченими. У 20 столітті виникли нові уявлення про будову матерії. У 1896 Антуан Анрі Беккерель відкрив явище радіоактивності внаслідок виявлення спонтанного випускання солями урану субатомних часток, а через два роки П'єр Кюрі і Марія Кюрі виділили два радіоактивні елементи: полоній і радій. Важливим було відкриття Фредеріка Содді, яке показало, що при радіоактивному розпаді відбувається перетворення одних речовин в інші, дало нове значення тому, що древні називали трансмутація. У 1897 Джозеф Джон Томсон) відкрив електрон. У 1911р. Ернест Резерфорд , виходячи з електронної концепції Томсона, запропонував модель атома: в центрі атома знаходиться позитивно заряджене ядро, а навколо нього обертаються негативно заряджені електрони. У 1913 Нільс Бор довів, що електрони можуть знаходитися не на будь-яких, а на суворо визначених орбітах. Вальтер Коссель спрогнозував , що хімічні властивості атома визначаються числом електронів на його зовнішній оболонці, а утворення хімічних зв'язків зумовлюється в основному силами електростатичної взаємодії. Американські вчені Ірвінг Ленгмюр й Гілберт Ньютон Льюїс визначили електронну теорію хімічного зв'язку, згідно з якою молекули неорганічних солей стабілізуються електростатичними взаємодіями між іонами, що входять до їх складу, які утворяться при переході електронів від одного елемента до іншого (іонний зв'язок). Важливим досягнення 20 століття Х-променів Іваном Пулюєм, що послужило основою для створення згодом методу рентгенівської кристалографії. За допомогою цього методу була розшифрована структура складних органічних сполук інсуліну, ДНК, гемоглобіну тощо. Зі створенням атомної теорії виникли нові потужні спектроскопічні методи, які можуть давати інформацію про будову атомів і молекул. Біохімія виділилася самостійну область в останньому десятиріччі 20 ст. Від[[|]]омі особистості в біохімії: Еміль Фішер , який синтезував такі речовини, як кофеїн, фенобарбітал, глюкозу, вніс великий внесок в науку про ферменти білкових каталізаторів; Теодор Сведберг , сконструював ультрацентрифугу і розробив новий метод визначення молекулярної маси макромолекул, головним чином білків; Арне Тізеліус , який створив метод електрофорезу досконаліший метод розділення гігантських молекул, заснований на відмінності в швидкості міграції заряджених молекул в електричному полі; Арчер Мартін і Річард Синг , котрі запропонували новий варіант методу: вони замінили трубку з адсорбентом на фільтрувальний папір. В кінці 1940-х початку 1950-х років вчені проаналізували суміші амінокислот, що виходять при розщепленні різних білків, і визначити склад білків, й було встановлено порядок розташування амінокислот в молекулі, а до 1964 цей білок вдалося синтезувати. Зараз методами біохімічного синтезу отримують багато гормонів лікарських засобів, вітамінів. Промислова хімія здобула свого основного розвитку на початку 20 ст. , коли ряд промислових корпорацій створили перші промислові дослідницькі лабораторії. Після відкриття і синтезу в 1940-х роках пеніциліну, а потім і інших антибіотиків з'явилися великі фармацевтичні фірми, в яких працювали професійні хіміки. Визначними у хімії слали дослідження в області хімії високомолекулярних сполук. Так, саме в цей час була розроблена теорія будови полімерів. Дослідження в цьому напрямі полімерів привели до синтезу поліетилену, а потім інших полімерів із заданими властивостями. Сьогодні виготовлення полімерів є найбільшою галуззю хімічної промисловості. Хімія в Україні Хімічні знання в Україні використовували давно: при з виготовленні і використанні металів, їхніх сплавів, емалей, пороху тощо. Значну роль у розвитку хімічних наук за нових часів в Україні мали наукові товариства природознавців, які існували в Харкові, Києві та Одесі. Перші наукові дослідження з хімії провадилися на початку 19 століття в Харківському університеті Василем Каразіним, Фердінандом Гізе. Визначні особистості української хімічної науки були Микола Бекетов , Микола Ізмайлов, Олександр Данилевський, Володимир Палладін , Олександр Ельтеков , Костянтин Красуський. Перший підручник фізіологічної хімії Олексія Ходнєва з Харківського університету вийшов 1847 року. У Київському університеті важливі досліди над дисоціацією молекул провадив у 1879—1884 роках Микола Миколайович Каяндер, також Я. Михайленко. Ілля Григорович Борщов, хімії Антон Володимирович Думанський, Петро Петрович Алексєєв , Микола Андрійович Бунге, Сергій Миколайович Реформатський – видатні науковці того часу. Володимир Олександрович Кістяковський працював у галузі біохімії над обміном вуглеводів, зокрема глікогену. У 1850—1860-их роках у Львівському університеті проводились досліди з органічної та аналітичної хімії . Тут працювали такі вчені як Л. Пебаль, С. Толлочко, Віктор Кемула , Е. Ліннеман. В кінці 19 — на початку 20 століття В Одеському університеті на ниві органічної хімії працювали Петро Григорович Мелікішвілі, Микола Дмитрович Зелінський Ф. Шведов, з О. Саханов, А. Рабинович , О. Фрумкін, Л. Писаржевський. Визначним українським біохіміком у Віденському університеті наприкінці 19 століття був І. Горбачевський. З радянського періоду більшість наукових праць почали проводитись в університетах та політехнічних інститутах. На цій ниві важливою ланкою стали інститути АН УРСР (нині АНУкраїни), які нині й репрезентують найвищий рівень хімічної науки в Україні. Сьогодні Академія Наук співпрацює з університетами, політехнічними інститутами та іншими дослідними цетрами, координуючи їх працю у визначених завданнях. Конспекти уроків, реферати та курсові роботи з Хімії, підручник хімія, уроки хімії, реферати з хімії, тести з хімії, відповіді на тести з хімії, хімія в школі, гдз з хімії, розробки уроків з хімії, домашні завдання хімія, хімія курс, план уроку по хімії, хімія відповіді, онлайн хімія, книги по хімії
|
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: