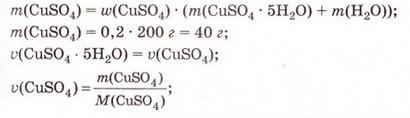|
|
|
| Строка 9: |
Строка 9: |
| | Виготовимо водний розчин масою 400 г із масовою часткою натрій хлориду 5 % . Спочатку обчислимо потрібні для цього масу солі та об'єм води: | | Виготовимо водний розчин масою 400 г із масовою часткою натрій хлориду 5 % . Спочатку обчислимо потрібні для цього масу солі та об'єм води: |
| | | | |
| - | [[Image:55_2_chemistry.jpg]]<br> | + | [[Image:55 2 chemistry.jpg]]<br> |
| | | | |
| | У колбу або склянку ємністю 500-700 мл помістимо наважку солі масою 20 г і невеликими порціями, обережно перемішуючи скляною паличкою або круговими рухами посудини, добавимо попередньо відміряну циліндром воду об'ємом 380 мл. Після повного розчинення солі переллємо розчин у посудину та закоркуємо її. На етикетці зазначимо дату виготовлення розчину та масову частку розчиненої речовини (поясніть, для чого).<br> | | У колбу або склянку ємністю 500-700 мл помістимо наважку солі масою 20 г і невеликими порціями, обережно перемішуючи скляною паличкою або круговими рухами посудини, добавимо попередньо відміряну циліндром воду об'ємом 380 мл. Після повного розчинення солі переллємо розчин у посудину та закоркуємо її. На етикетці зазначимо дату виготовлення розчину та масову частку розчиненої речовини (поясніть, для чого).<br> |
| Строка 17: |
Строка 17: |
| | Обчислимо масу купрум(ІІ) сульфату, пентагідрату та об'єм води, потрібні для виготовлення розчину масою 200 г із масовою часткою купрум(II) сульфату 20 %. | | Обчислимо масу купрум(ІІ) сульфату, пентагідрату та об'єм води, потрібні для виготовлення розчину масою 200 г із масовою часткою купрум(II) сульфату 20 %. |
| | | | |
| - | [[Image:55_3x_chemistry.jpg]]<br> | + | [[Image:55 3x chemistry.jpg]]<br> |
| | | | |
| - | [[Image:56_chemistry.jpg]] | + | [[Image:56 chemistry.jpg]] |
| | | | |
| | <u>''Застосуйте свої знання й уміння''</u><br>1. Виберіть реактиви та обладнання для виготовлення розчину певної маси із заданою масовою часткою калій нітрату:<br>А Ваги з важками; Б Газовідвідна трубка; В Шпатель; Г Дистильована вода; Д КN0<sub>2</sub>; Е Мірний циліндр; Ж Конічна колба; 3 Пластина для крапельного аналізу; И КN0<sub>3</sub>.<br> | | <u>''Застосуйте свої знання й уміння''</u><br>1. Виберіть реактиви та обладнання для виготовлення розчину певної маси із заданою масовою часткою калій нітрату:<br>А Ваги з важками; Б Газовідвідна трубка; В Шпатель; Г Дистильована вода; Д КN0<sub>2</sub>; Е Мірний циліндр; Ж Конічна колба; 3 Пластина для крапельного аналізу; И КN0<sub>3</sub>.<br> |
| Строка 37: |
Строка 37: |
| | <br> ''Г. А. Лашевська, Геометрія, 9 клас<br>Вислано читачами з інтернет-сайтів '' | | <br> ''Г. А. Лашевська, Геометрія, 9 клас<br>Вислано читачами з інтернет-сайтів '' |
| | | | |
| - | <br> <sub>Скачати підручники та книги онлайн, планування з хімії, курси та завдання з хімії для 9 класу</sub> <br> | + | <br> <sub>Скачати підручники та книги [[Гіпермаркет_Знань_-_перший_в_світі!|онлайн]], планування [[Хімія|з хімії]], курси та завдання [[Хімія_9_клас|з хімії для 9 класу]]</sub> [[Хімія_9_клас|<br>]] |
| | | | |
| | <br> | | <br> |
Версия 12:57, 19 марта 2010
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Хімія: Розв'язування розрахункових задач №2
РОЗВ'ЯЗУВАННЯ РОЗРАХУНКОВИХ ЗАДАЧ №2
Виготовлення розчинів потребує точності, акуратності й попереднього проведення правильних математичних розрахунків. Усі ці якості та вміння знадобляться вам не лише на одному з наступних уроків під час виконання Практпичної роботи № 1, а й у повсякденному житті. Докладно розглянемо послідовність виготовлення розчину на конкретному прикладі.
Виготовимо водний розчин масою 400 г із масовою часткою натрій хлориду 5 % . Спочатку обчислимо потрібні для цього масу солі та об'єм води:

У колбу або склянку ємністю 500-700 мл помістимо наважку солі масою 20 г і невеликими порціями, обережно перемішуючи скляною паличкою або круговими рухами посудини, добавимо попередньо відміряну циліндром воду об'ємом 380 мл. Після повного розчинення солі переллємо розчин у посудину та закоркуємо її. На етикетці зазначимо дату виготовлення розчину та масову частку розчиненої речовини (поясніть, для чого).
Пам'ятайте, у разі виготовлення розчину з кристалогідрату слід зважати на наявність у ньому кристалізаційної води.
Обчислимо масу купрум(ІІ) сульфату, пентагідрату та об'єм води, потрібні для виготовлення розчину масою 200 г із масовою часткою купрум(II) сульфату 20 %.
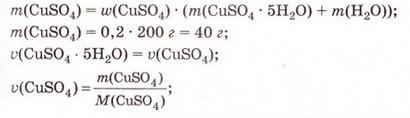

Застосуйте свої знання й уміння
1. Виберіть реактиви та обладнання для виготовлення розчину певної маси із заданою масовою часткою калій нітрату:
А Ваги з важками; Б Газовідвідна трубка; В Шпатель; Г Дистильована вода; Д КN02; Е Мірний циліндр; Ж Конічна колба; 3 Пластина для крапельного аналізу; И КN03.
2. Виберіть правильну послідовність операцій із виготовлення розчину з певною масовою часткою розчиненої речовини:
А Фільтрування розчину; Б Змішування розчинюваної речовини із розчинником; В Відмірювання порцій розчинюваної речовини й розчинника; Г Обчислення маси розчинюваної речовини та об'єму розчинника.
3. Обчисліть масу натрій хлориду і об'єм води для виготовлення розчину масою 150 г з масовою часткою солі 0,04.
4. Обчисліть масу цукру та об'єм води для виготовлення розчину масою 250 г з масовою часткою сахарози 0,2.
5. Обчисліть масу натрій карбонату та об'єм води для виготовлення розчину масою 80 г з масовою часткою солі 5 %.
6. Як дезінфікуючі засоби для полоскання ротової порожнини та горла використовують 3 %-ний розчин питної соди (натрій гідрогенкарбонату) або 5 %-ний розчин борної (боратної) кислоти. Обчисліть маси розчинюваних речовин і об'єми води для виготовлення цих розчинів об'ємом 200 мл кожний. Густини розчинів дорівнюють 1 гмл. Поясніть, чи потрібно знати хімічні формули розчинюваних речовин, аби виконати ці обчислення.
7. Схарактеризуйте значення розчинів у природі та житті людини.
Г. А. Лашевська, Геометрія, 9 клас
Вислано читачами з інтернет-сайтів
Скачати підручники та книги онлайн, планування з хімії, курси та завдання з хімії для 9 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|