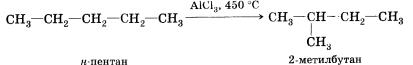|
|
|
| Строка 3: |
Строка 3: |
| | Реакции органических веществ можно формально разделить на четыре основных типа: замещения, присоединения, отщепления (элиминирования) и перегруппировки (изомеризации). Очевидно, что все многообразие реакций органических соединений невозможно свести в рамки предложенной классификации (например, реакции горения). Однако такая классификация поможет установить аналогии с уже знакомыми вам из курса неорганической химии классификациями реакций, протекающих между неорганическими веществами.<br><br>Как правило, основное органическое соединение, участвующее в реакции, называют субстратом, а другой компонент реакции условно рассматривают как реагент.<br><br>''Реакции замещения''<br><br>Реакции, в результате которых осуществляется замена одного атома или группы атомов в исходной молекуле (субстрате) на другие атомы или группы атомов, называются реакциями замещения.<br><br>В реакции замещения вступают предельные и ароматические соединения, такие, как, например, алканы, циклоалканы или арены.<br><br>Приведем примеры таких реакций.<br> | | Реакции органических веществ можно формально разделить на четыре основных типа: замещения, присоединения, отщепления (элиминирования) и перегруппировки (изомеризации). Очевидно, что все многообразие реакций органических соединений невозможно свести в рамки предложенной классификации (например, реакции горения). Однако такая классификация поможет установить аналогии с уже знакомыми вам из курса неорганической химии классификациями реакций, протекающих между неорганическими веществами.<br><br>Как правило, основное органическое соединение, участвующее в реакции, называют субстратом, а другой компонент реакции условно рассматривают как реагент.<br><br>''Реакции замещения''<br><br>Реакции, в результате которых осуществляется замена одного атома или группы атомов в исходной молекуле (субстрате) на другие атомы или группы атомов, называются реакциями замещения.<br><br>В реакции замещения вступают предельные и ароматические соединения, такие, как, например, алканы, циклоалканы или арены.<br><br>Приведем примеры таких реакций.<br> |
| | | | |
| - | Под действием света атомы водорода в молекуле метана способны замещаться на атомы галогена, например на атомы хлора:<br><br>СН4 + Сl2 —> СН3Сl + НСl<br><br>Другим примером замещения водорода на галоген является превращение бензола в бромбензол:<br>[[Image:Aahim10-32.jpg]] | + | Под действием света атомы [[Квантовые_постулаты_Бора._Модель_атома_водорода_по_Бору|водорода]] в молекуле метана способны замещаться на атомы галогена, например на атомы хлора:<br><br>СН4 + Сl2 —> СН3Сl + НСl<br><br>Другим примером замещения водорода на галоген является превращение бензола в бромбензол:<br>[[Image:Aahim10-32.jpg|Типы химических реакций в органической химии]] |
| | | | |
| | При этой форме записи реагенты, катализатор, условия проведения реакции записывают над стрелкой, а неорганические продукты реакции — под ней.<br><br>''Реакции присоединения''<br><br>Реакции, в результате которых две или более молекул реагирующих веществ соединяются в одну, называют реакциями присоединения.<br><br>В реакции присоединения вступают ненасыщенные соединения, такие, как, например, алкены или алкины. В зависимости от того, какая молекула выступает в качестве реагента, различают гидрирование (или восстановление), галогенирование, гидрогалогенирование, гидратацию и другие реакции присоединения. Каждая из них требует определенных условий.<br><br>1. Гидрирование — реакция присоединения молекулы водорода по кратной связи:<br><br>СН3—СН = СН2 + Н2 -> СН3—СН2—СН3 | | При этой форме записи реагенты, катализатор, условия проведения реакции записывают над стрелкой, а неорганические продукты реакции — под ней.<br><br>''Реакции присоединения''<br><br>Реакции, в результате которых две или более молекул реагирующих веществ соединяются в одну, называют реакциями присоединения.<br><br>В реакции присоединения вступают ненасыщенные соединения, такие, как, например, алкены или алкины. В зависимости от того, какая молекула выступает в качестве реагента, различают гидрирование (или восстановление), галогенирование, гидрогалогенирование, гидратацию и другие реакции присоединения. Каждая из них требует определенных условий.<br><br>1. Гидрирование — реакция присоединения молекулы водорода по кратной связи:<br><br>СН3—СН = СН2 + Н2 -> СН3—СН2—СН3 |
| Строка 9: |
Строка 9: |
| | пропен пропан | | пропен пропан |
| | | | |
| - | <br>2. Гидрогалогенирование — реакция присоединения гало-геноводорода (например, гидрохлорирование):<br><br>СН2=СН2 + НСl —> СН3—СН2—Сl<br> этен хлорэтан<br><br>3. Галогенирование — реакция присоединения галогена (например, хлорирование):<br><br>СН2=СН2 + Сl2 —> СН2Сl—СН2Сl<br> этен 1,2-дихлорэтан<br><br>4. Полимеризация — особый тип реакций присоединения, в ходе которых молекулы вещества с небольшой молекулярной массой соединяются друг с другом с образованием молекул вещества с очень высокой молекулярной массой — макромолекул.<br><br>Реакции полимеризации — это процессы соединения множества молекул низкомолекулярного вещества (мономера) в крупные молекулы (макромолекулы) полимера.<br><br>Примером реакции полимеризации может служить получение полиэтилена из этилена (этена) под действием ультрафиолетового излучения и радикального инициатора полимеризации R.<br>[[Image:Aahim10-33.jpg]] | + | <br>2. Гидрогалогенирование — реакция присоединения гало-геноводорода (например, гидрохлорирование):<br><br>СН2=СН2 + НСl —> СН3—СН2—Сl<br> этен хлорэтан<br><br>3. Галогенирование — реакция присоединения галогена (например, хлорирование):<br><br>СН2=СН2 + Сl2 —> СН2Сl—СН2Сl<br> этен 1,2-дихлорэтан<br><br>4. Полимеризация — особый тип реакций присоединения, в ходе которых молекулы вещества с небольшой молекулярной массой соединяются друг с другом с образованием [[Молекулы_и_атомы|молекул]] вещества с очень высокой молекулярной массой — макромолекул.<br><br>Реакции полимеризации — это процессы соединения множества молекул низкомолекулярного вещества (мономера) в крупные молекулы (макромолекулы) полимера.<br><br>Примером реакции полимеризации может служить получение полиэтилена из этилена (этена) под действием ультрафиолетового излучения и радикального инициатора полимеризации R.<br>[[Image:Aahim10-33.jpg|Типы химических реакций в органической химии]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | ''Реакции отщепления (элиминирования)''<br><br>Реакции, в результате которых из молекулы исходного соединения образуются молекулы нескольких новых веществ, называют реакциями отщепления или элиминирования.<br><br>Примерами таких реакций может служить получение этилена из различных органических веществ.<br> | + | ''Реакции отщепления (элиминирования)''<br><br>Реакции, в результате которых из молекулы исходного соединения образуются молекулы нескольких новых веществ, называют реакциями отщепления или элиминирования.<br><br>Примерами таких реакций может служить получение [[Непредельные_углеводороды._Этилен_и_его_гомологи|этилена]] из различных органических веществ.<br> |
| | | | |
| - | [[Image:Aahim10-34.jpg]] | + | [[Image:Aahim10-34.jpg|Типы химических реакций в органической химии]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | Особое значение среди реакций отщепления имеет реакция термического расщепления углеводородов, на котором основан крекинг (англ. to crack — расщеплять) алканов — важнейший технологический процесс:<br>[[Image:Aahim10-35.jpg]] | + | Особое значение среди реакций отщепления имеет реакция термического расщепления углеводородов, на котором основан крекинг (англ. to crack — расщеплять) алканов — важнейший технологический процесс:<br>[[Image:Aahim10-35.jpg|Типы химических реакций в органической химии]] |
| | | | |
| | <br> | | <br> |
| Строка 25: |
Строка 25: |
| | В большинстве случаев отщепление малой молекулы от молекулы исходного вещества приводит к образованию дополнительной ''п''-связи между атомами. Реакции элиминирования протекают в определенных условиях и с определенными реагентами. Приведенные уравнения отражают лишь конечный результат этих превращений.<br><br>''Реакции изомеризации''<br>Реакции, в результате которых из молекул одного вещества образуются молекулы, других веществ того же качественного и количественного состава, т. е. с той же молекулярной формулой, называют реакциями изомеризации. | | В большинстве случаев отщепление малой молекулы от молекулы исходного вещества приводит к образованию дополнительной ''п''-связи между атомами. Реакции элиминирования протекают в определенных условиях и с определенными реагентами. Приведенные уравнения отражают лишь конечный результат этих превращений.<br><br>''Реакции изомеризации''<br>Реакции, в результате которых из молекул одного вещества образуются молекулы, других веществ того же качественного и количественного состава, т. е. с той же молекулярной формулой, называют реакциями изомеризации. |
| | | | |
| - | <br>Примером такой реакции является изомеризация углеродного скелета алканов линейного строения в разветвленные, которая происходит на хлориде алюминия при высокой температуре:<br>[[Image:Aahim10-36.jpg]] | + | <br>Примером такой реакции является изомеризация углеродного скелета алканов линейного строения в разветвленные, которая происходит на хлориде [[Конспект_уроку_з_теми:_Алюміній_як_хімічний_елемент_і_проста_речовина._Фізичні_та_хімічні_властивості_алюмінію|алюминия]] при высокой температуре:<br>[[Image:Aahim10-36.jpg|Типы химических реакций в органической химии]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | 1. К какому типу реакций относится:<br><br>а) получение хлорметана из метана;<br>б) получение бромбензола из бензола;<br>в) получение хлорэтана из этилена;<br>г) получение этилена из этанола;<br>д) превращение бутана в изобутан;<br>е) дегидрирование этана;<br>ж) превращение бромэтана в этанол?<br><br>2. Какие реакции характерны для: а) алканов; б) алкенов? Приведите примеры реакций.<br><br>3. В чем особенности реакций изомеризации? Что их объединяет с реакциями получения аллотропных модификаций одного химического элемента? Приведите примеры.<br><br>4. В каких реакциях (присоединение, замещение, элиминирование, изомеризация) молекулярная масса исходного соединения:<br><br>а) увеличивается;<br>б) уменьшается;<br>в) не изменяется;<br>г) в зависимости от реагента увеличивается или уменьшается?<br> | + | 1. К какому типу реакций относится:<br><br>а) получение хлорметана из метана;<br>б) получение бромбензола из бензола;<br>в) получение хлорэтана из [[Непредельные_углеводороды._Этилен_и_его_гомологи|этилена]];<br>г) получение этилена из этанола;<br>д) превращение бутана в изобутан;<br>е) дегидрирование этана;<br>ж) превращение бромэтана в этанол?<br><br>2. Какие реакции характерны для: а) алканов; б) алкенов? Приведите примеры реакций.<br><br>3. В чем особенности реакций изомеризации? Что их объединяет с реакциями получения аллотропных модификаций одного химического элемента? Приведите примеры.<br><br>4. В каких реакциях (присоединение, замещение, элиминирование, изомеризация) молекулярная масса исходного соединения:<br><br>а) увеличивается;<br>б) уменьшается;<br>в) не изменяется;<br>г) в зависимости от реагента увеличивается или уменьшается?<br> |
| | | | |
| | <br> <sub>риторические вопросы [[Химия|по химии]], кроссворды [[Химия 10 класс|для 10 класса]], [[Гипермаркет знаний - первый в мире!|цитаты и поговорки]]</sub> | | <br> <sub>риторические вопросы [[Химия|по химии]], кроссворды [[Химия 10 класс|для 10 класса]], [[Гипермаркет знаний - первый в мире!|цитаты и поговорки]]</sub> |
Текущая версия на 05:02, 2 июля 2012
Гипермаркет знаний>>Химия>>Химия 10 класс>> Химия: Типы химических реакций в органической химии
Реакции органических веществ можно формально разделить на четыре основных типа: замещения, присоединения, отщепления (элиминирования) и перегруппировки (изомеризации). Очевидно, что все многообразие реакций органических соединений невозможно свести в рамки предложенной классификации (например, реакции горения). Однако такая классификация поможет установить аналогии с уже знакомыми вам из курса неорганической химии классификациями реакций, протекающих между неорганическими веществами.
Как правило, основное органическое соединение, участвующее в реакции, называют субстратом, а другой компонент реакции условно рассматривают как реагент.
Реакции замещения
Реакции, в результате которых осуществляется замена одного атома или группы атомов в исходной молекуле (субстрате) на другие атомы или группы атомов, называются реакциями замещения.
В реакции замещения вступают предельные и ароматические соединения, такие, как, например, алканы, циклоалканы или арены.
Приведем примеры таких реакций.
Под действием света атомы водорода в молекуле метана способны замещаться на атомы галогена, например на атомы хлора:
СН4 + Сl2 —> СН3Сl + НСl
Другим примером замещения водорода на галоген является превращение бензола в бромбензол:
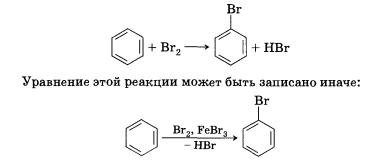
При этой форме записи реагенты, катализатор, условия проведения реакции записывают над стрелкой, а неорганические продукты реакции — под ней.
Реакции присоединения
Реакции, в результате которых две или более молекул реагирующих веществ соединяются в одну, называют реакциями присоединения.
В реакции присоединения вступают ненасыщенные соединения, такие, как, например, алкены или алкины. В зависимости от того, какая молекула выступает в качестве реагента, различают гидрирование (или восстановление), галогенирование, гидрогалогенирование, гидратацию и другие реакции присоединения. Каждая из них требует определенных условий.
1. Гидрирование — реакция присоединения молекулы водорода по кратной связи:
СН3—СН = СН2 + Н2 -> СН3—СН2—СН3
пропен пропан
2. Гидрогалогенирование — реакция присоединения гало-геноводорода (например, гидрохлорирование):
СН2=СН2 + НСl —> СН3—СН2—Сl
этен хлорэтан
3. Галогенирование — реакция присоединения галогена (например, хлорирование):
СН2=СН2 + Сl2 —> СН2Сl—СН2Сl
этен 1,2-дихлорэтан
4. Полимеризация — особый тип реакций присоединения, в ходе которых молекулы вещества с небольшой молекулярной массой соединяются друг с другом с образованием молекул вещества с очень высокой молекулярной массой — макромолекул.
Реакции полимеризации — это процессы соединения множества молекул низкомолекулярного вещества (мономера) в крупные молекулы (макромолекулы) полимера.
Примером реакции полимеризации может служить получение полиэтилена из этилена (этена) под действием ультрафиолетового излучения и радикального инициатора полимеризации R.
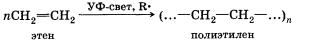
Реакции отщепления (элиминирования)
Реакции, в результате которых из молекулы исходного соединения образуются молекулы нескольких новых веществ, называют реакциями отщепления или элиминирования.
Примерами таких реакций может служить получение этилена из различных органических веществ.
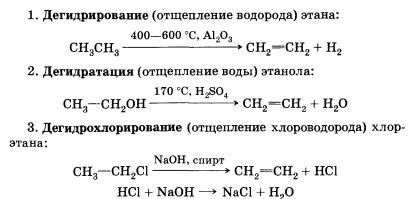
Особое значение среди реакций отщепления имеет реакция термического расщепления углеводородов, на котором основан крекинг (англ. to crack — расщеплять) алканов — важнейший технологический процесс:
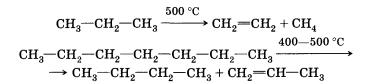
В большинстве случаев отщепление малой молекулы от молекулы исходного вещества приводит к образованию дополнительной п-связи между атомами. Реакции элиминирования протекают в определенных условиях и с определенными реагентами. Приведенные уравнения отражают лишь конечный результат этих превращений.
Реакции изомеризации
Реакции, в результате которых из молекул одного вещества образуются молекулы, других веществ того же качественного и количественного состава, т. е. с той же молекулярной формулой, называют реакциями изомеризации.
Примером такой реакции является изомеризация углеродного скелета алканов линейного строения в разветвленные, которая происходит на хлориде алюминия при высокой температуре:
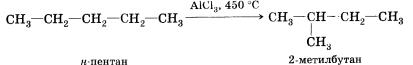
1. К какому типу реакций относится:
а) получение хлорметана из метана;
б) получение бромбензола из бензола;
в) получение хлорэтана из этилена;
г) получение этилена из этанола;
д) превращение бутана в изобутан;
е) дегидрирование этана;
ж) превращение бромэтана в этанол?
2. Какие реакции характерны для: а) алканов; б) алкенов? Приведите примеры реакций.
3. В чем особенности реакций изомеризации? Что их объединяет с реакциями получения аллотропных модификаций одного химического элемента? Приведите примеры.
4. В каких реакциях (присоединение, замещение, элиминирование, изомеризация) молекулярная масса исходного соединения:
а) увеличивается;
б) уменьшается;
в) не изменяется;
г) в зависимости от реагента увеличивается или уменьшается?
риторические вопросы по химии, кроссворды для 10 класса, цитаты и поговорки
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|