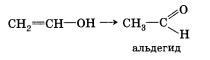|
Гипермаркет знаний>>Химия>>Химия 10 класс>> Химия: Алкины
Строение
Алкины — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, одну тройную связь между атомами углерода и соответствующие общей формуле СnН2n-2.
Атомы углерода, между которыми образована тройная связь, находятся в состоянии sр-гибридизации (рис. 15). Это означает, что в гибридизации участвует одна s- и одна р-орби-таль, а две р-орбитали остаются негибридизованными. Перекрывание гибридных орбиталей приводит к образованию Þ-связи, а за счет негибридизованных р-орбиталей соседних атомов углерода образуются две л-связи. Таким образом, тройная связь состоит из одной а- и двух л-связей.

Все гибридные орбитали атомов, между которыми образована двойная связь, а также заместители при них (в случае этина — атомы водорода) лежат на одной прямой, а плоскости п</span-связей перпендикулярны друг другу.
Тройная углерод-углеродная связь с длиной 0,120 нм короче двойной, энергия тройной связи больше, т. е. она является более прочной.
Гомологический ряд этина
Неразветвленные алкины составляют гомологический ряд этина (ацетилена):
С2Н2 — этин, С3Н4 — пропин, С4Н6 — бутин, С5Н8 — пентин, С6Н10 — гексин и т. д.
Изомерия и номенклатура
Для алкинов, так же как и для алкенов, характерна структурная изомерия: изомерия углеродного скелета и изомерия положения кратной связи. Простейший алкин, для которого характерны структурные изомеры положения кратной связи класса алкинов, — это бутин:
СН3—СН2—С=СН CH3—С=С—СН3
бутин-1 бутин-2
Изомерия углеродного скелета у алкинов возможна, начиная с пентина:
СН3—СН2—СН2—С=СН СН3—СН—С=СН
l
СН3
пентин-1 З-метилбутин-1
Так как тройная связь предполагает линейное строение углеродной цепи, геометрическая (цис транс-) изомерия в случае алкинов невозможна.
Наличие тройной связи в молекулах углеводородов этого класса отражается суффиксом -ин, а ее положение в цепи — номером атома углерода.
Получение
1. Метановый способ. Нагревание метана до температуры 1500 °С приводит к образованию ацетилена. Эта реакция эндо-термична. При высокой температуре происходит смещение равновесия в сторону образования ацетилена:
1500 °С
2СН4 -> С2Н2 + ЗН2
Продукты (газовую смесь) необходимо быстро охладить, чтобы предотвратить разложение образовавшегося ацетилена.
2. Карбидный способ. Давно известным и достаточно удобным способом получения этина является гидролиз (обменное взаимодействие веществ с водой) некоторых карбидов, например гидролиз карбида кальция:
СаС2 + 2Н20 —> Са(ОН)2 + С2Н2
Карбид кальция получают взаимодействием оксида кальция, образовавшегося при обжиге (термическом разложении) карбоната кальция, с углем:
СаСО3 -> СаО + С02
СаО + ЗС —> СаС2 + СО
3. Способ дегидрогалогенирования. При воздействии на ди-бромпроизводное, в котором атомы галогенов находятся при соседних атомах углерода (или при одном и том же атоме), спиртового раствора щелочи происходит отщепление двух молекул галогеноводорода (дегидрогалогенирование) и образование тройной связи.
Физические свойства
Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении молекулярной массы соединений.
Алкины имеют специфический запах. Они лучше растворяются в воде, чем алканы и алкены.
Химические свойства
Реакции присоединения
Алкины относятся к непредельным соединениям и вступают в реакции присоединения. В основном это реакции электро-фильного присоединения.
1. Галогенирование (присоединение молекулы галогена). Алкин способен присоединить две молекулы галогена (хлора, брома).
2. Гидрогалогенирование (присоединение галогеноводорода).
Реакция присоединения галогеноводорода, протекающая по электрофильному механизму, также идет в две стадии, причем на обеих стадиях выполняется правило Марковникова:
СН3—С=СН + НВr —> СН3—СВr =СН2
2-бромпропен
СН3—СВr=СН2 + НВr —> СН3—СВr2—СН3
2,2-дибромпропан
3. Гидратация (присоединение воды). Большое значение для промышленного синтеза кетонов и альдегидов имеет реакция присоединения воды (гидратация), которую называют реакцией Кучерова.
4. Гидрирование алкинов. Алкины присоединяют водород в присутствии металлических катализаторов. Так как тройная связь содержит две реакционноспособные я-связи, алкины присоединяют водород в две ступени.
Тримеризация
При пропускании этина над активированным углем образуется смесь продуктов, одним из которых является бензол:
Окисление алкинов
Этин (ацетилен) горит в кислороде с выделением очень большого количества теплоты:
2С2Н2 + 502 —> 4С02 + 2Н20 + 2600 кДж
На этой реакции основано действие кислород-ацетиленовой горелки, пламя которой имеет очень высокую температуру (более 3000 °С), что позволяет использовать ее для резки и сварки металлов.
На воздухе ацетилен горит коптящим пламенем, так как содержание углерода в его молекуле выше, чем в молекулах этана и этена.
Алкины, как и алкены, обесцвечивают подкисленные растворы перманганата калия, при этом происходит разрушение кратной связи.
Механизм реакций электрофильного присоединения к алкинам
Давайте рассмотрим, почему бромоводород присоединяется к алкинам в соответствии с правилом Марковникова.
Предпочтительное присоединение катиона водорода (электро-фильной частицы) к более гидрированному атому углерода определяется большей устойчивостью катиона СН3 —> С+—СН2, стабилизированного положительным индуктивным эффектом метильной группы, по сравнению с карбокатионом СН3—СН=СН+, в котором донорное влияние метильной группы на углерод с положительным зарядом ослаблено.
Для того чтобы определить направление присоединения второй молекулы бромоводорода, надо сравнить устойчивость следующих карбокатионов:

Частица (а) оказывается более устойчивой, так как атом брома обладает положительным мезомерным эффектом (орбиталь с непо-деленной электронной парой брома перекрывается с незаполненной орбиталью атома углерода), который может проявиться только в том случае, если атом брома присоединен непосредственно к атому углерода, обладающему незаполненной орбиталью, т. е. несущему положительный заряд:
Вr—C+—СН СН3
Гидратация (присоединение воды). Вода присоединяется к ацетилену в присутствии солей двухвалентной ртути в кислой среде с образованием непредельного спирта — енола.
Получившийся енол немедленно превращается в альдегид:
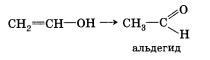
Явление взаимопревращения енолов и альдегидов (енолов и ке-тонов) называется кето-енольной таутомерией и будет более подробно рассмотрено в § 18 «Альдегиды и кетоны».
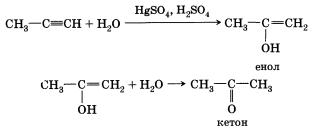
Только при гидратации этина образуется альдегид. В случае алкинов с более длинной цепью в соответствии с правилом Марков-никова будет происходить образование енола с гидроксигруппой при менее гидрированном атоме углерода (водород присоединяется к крайнему атому углеродной цепи). Такие енолы превращаются в кетоны:
Димеризация
Помимо тримеризации ацетилена, возможна его димеризация. Под действием солей одновалентной меди образуется винилацетилен.
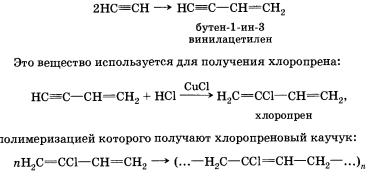
Вза'имодействие с основаниями
При взаимодействии с сильными основаниями (например, амидом натрия) алкины, содержащие тройную связь на конце молекулы (т. е. атом водорода, присоединенный к атому углерода в sр-гибридизации), теряют катион водорода и образуют соли — ацетилениды:
НС=-СН + NаКН2 —> НС=-СNа + NH3
амид ацетиленид
натрия натрия
Таким образом, можно сказать, что алкины проявляют свойства кислоты.
Неподеленная электронная пара, находящаяся на гибридной орбитали атома углерода в состоянии ер-гибридизации, лучше удерживается ядром, чем в случае sр3-гибридизации, что приводит к более высокой кислотности алкинов.
Способность атома водорода, находящегося при тройной связи, замещаться на металл применяют для отделения алкинов с тройной связью на конце молекулы от всех остальных алкинов.
Смесь алкинов пропускают через аммиачный раствор оксида серебра. Образовавшаяся соль выпадает в осадок. Ее отфильтровывают и разлагают кислотой.
Следует отметить, что полученная соль серебра и подобные ей соединения меди взрывоопасны. Способность ацетиленидов реагировать с галогенопроизводными используют для синтеза соединений, содержащих тройную связь.
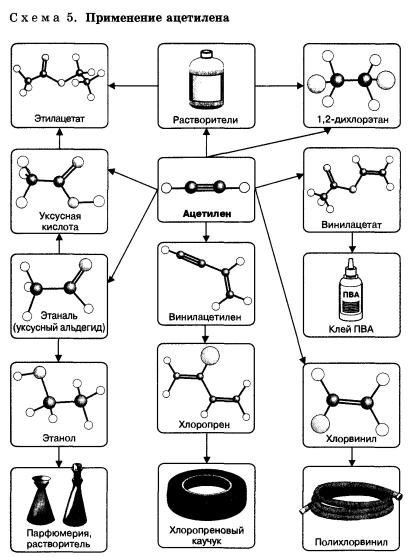
Применение
Алкины являются сырьем для производства большого количества органических соединений и материалов: альдегидов, кетонов, растворителей (тетрагалогенэтанов), исходных веществ для получения синтетических каучуков, поливинил-хлорида и других полимеров (схема 5).
Ацетилен является ценнейшим горючим с очень высокой теплотой горения.
1. Возможна ли для алкинов цис-транс-изомерия?
2. Напишите все возможные формулы изомеров углеводорода состава С5Н8, относящихся к классу алкинов.
3. Предложите способы получения ацетилена из неорганических веществ. Напишите уравнения соответствующих реакций.
4. Расшифруйте следующую цепочку превращений. Назовите соединения А, Б и В.
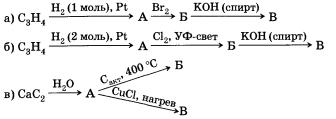
5. С помощью каких реагентов и при каких условиях можно получить бутин-2 из бутена-2? Запишите уравнения реакций.
6*. Почему во всех работах, связанных с ацетиленом, категорически запрещено применять медь или ее сплавы в реакторах, инструментах, коммуникациях и т. д.?
7*.При сжигании 2,48 г смеси пропана, пропена и пропина образовалось 4,03 г углекислого газа (н. у.). Сколько граммов воды получилось при этом?
8*. 3,92 л (н. у.) смеси газообразных алкена и алкина, содержащих одинаковое число атомов углерода, могут присоединить 40 г брома. Образовавшаяся при этом смесь имеет массу 47,2 г. Определите качественный и количественный (в процентах по объему) состав исходной смеси углеродов.
опорный каркас урока 10 класса, самопроверка по химии, креативные задания для десятиклассников
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|