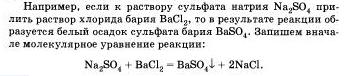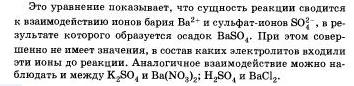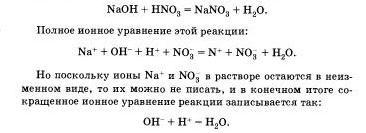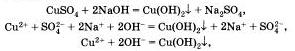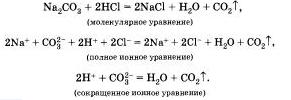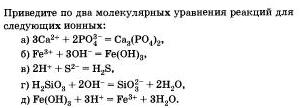|
|
|
| Строка 1: |
Строка 1: |
| - | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Ионные уравнения<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Ионные уравнения, уравнения</metakeywords>''' | + | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Ионные уравнения<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Ионные уравнения, уравнения</metakeywords>''' Большинство [[Скорость_химических_реакций|химических реакций]] протекает в растворах. Растворы электролитов содержат ионы, поэтому реакции и растворах электролитов фактически сводятся к реакциям между ионами.<br><br>Реакции между ионами называют [[Классификация_химических_реакций|ионными реакциями]], а уравнения таких реакций - ионными уравнениями.<br><br>При составлении ионных уравнении следует руководствоваться тем. что формулы веществ малодиссоцвшрующих. нерастворимых и газообразных записываются в молекулярном виде. |
| - | Большинство химических реакций протекает в растворах. Растворы электролитов содержат ионы, поэтому реакции и растворах электролитов фактически сводятся к реакциям между ионами.<br><br>Реакции между ионами называют ионными ре акциями, а уравнения таких реакций - ионными уравнениями.<br><br>При составлении ионных уравнении следует руководствоваться тем. что формулы веществ малодиссоцвшрующих. нерастворимых и газообразных записываются в молекулярном виде. | + | |
| | | | |
| - | <br>Бели вещество выпадает в осадок, то рядом с его формулой ставят стрелку, направленную вниз, а если в ходе реакции выделяется газообразное вещество, то рядом с его формулой ставят стрелку, направленную вверх. | + | <br>Бели вещество выпадает в осадок, то рядом с его формулой ставят стрелку, направленную вниз, а если в ходе реакции выделяется газообразное вещество, то рядом с его формулой ставят стрелку, направленную вверх. |
| | | | |
| - | [[Image:him8-117.jpg]] | + | [[Image:Him8-117.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Перепишем это уравнение, изобразив сильные электролиты в виде ионов, а уходящие из сферы реакции - в виде молекул: |
| | | | |
| - | Перепишем это уравнение, изобразив сильные электролиты в виде ионов, а уходящие из сферы реакции - в виде молекул:
| + | [[Image:Him8-118.jpg|химия 8 класс]] |
| | | | |
| - | [[Image:him8-118.jpg]]
| + | <br> |
| | | | |
| | + | Мы записали, таким обратом, полное ионное уравнение реакции. |
| | | | |
| | + | <br>Если исключить из обеих частей равенства одинаковые ионы, то есть не участвующие в реакции в левой и правой часто уравнения), то получим сокращенное ионное уравнение реакции:<br>[[Image:Him8-119.jpg|химия 8 класс]] |
| | | | |
| - | Мы записали, таким обратом, полное ионное уравнение реакции.
| + | <br> |
| | | | |
| - | <br>Если исключить из обеих частей равенства одинаковые ионы, то есть не участвующие в реакции в левой и правой часто уравнения), то получим сокращенное ионное уравнение реакции:<br>[[Image:him8-119.jpg]]
| + | [[Image:Him8-120.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Таким образом, сокращенные ионные уравнения представляют собой уравнения в общем виде, которые характеризуют сущность химической реакции п показывают, какие ионы реагируют и какое вещество образуется в результате. |
| | | | |
| - | [[Image:him8-120.jpg]] | + | <br>Реакции ионного обмена протекают до конца в тех случаях, когда образуется или осадок, или малодиссоциирующее вещество, например вода. Беля к раствору гидроксида натрия, окрашенного фенолфталеином в малиновый цвет, прилить избыток раствора азотной кислоты, то раствор обесцветится, что послужит сигналом протекания химической реакции:<br>[[Image:Him8-121.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Оно показывает, что взаимодействие сильной [[Кислоты._Полные_уроки|кислоты]] п щелочи сводится к взаимодействию ионов Н+ и ионов ОН -, в результате которого образуется малодиссоцвирующее вещество — вода. |
| | | | |
| - | Таким образом, сокращенные ионные уравнения представляют собой уравнения в общем виде, которые характеризуют сущность химической реакции п показывают, какие ионы реагируют и какое вещество образуется в результате.
| + | <br>Указанная реакция взаимодействия сильной кислоты со щелочью называется реакцией нейтрализации. Это частный случай реакции обмена. |
| | | | |
| - | <br>Реакции ионного обмена протекают до конца в тех случаях, когда образуется или осадок, или малодиссоциирующее вещество, например вода. Беля к раствору гидроксида натрия, окрашенного фенолфталеином в малиновый цвет, прилить избыток раствора азотной кислоты, то раствор обесцветится, что послужит сигналом протекания химической реакции:<br>[[Image:him8-121.jpg]] | + | <br> |
| | | | |
| | + | Подобная реакция обмена может протекать не только между кислотами и щелочами, но и между кислотами и нерастворимыми основаниями. Например, если получить голубой осадок нерастворимого гидроксида меди (II) взаимодействием сульфата меди і II і со щелочью: |
| | | | |
| | + | [[Image:Him8-123.jpg|химия 8 класс]] |
| | | | |
| - | Оно показывает, что взаимодействие сильной кислоты п щелочи сводится к взаимодействию ионов Н+ и ионов ОН -, в результате которого образуется малодиссоцвирующее вещество — вода.
| + | а затем поделить полученный осадок на три части и прилить к осадку в первой пробирке раствор серной кислоты, к осадку во второй пробирке раствор соляной кислоты, а к осадку в третьей пробирке раствор [[Азотные,_калийные_и_фосфорные_удобрения|азотной]] кислоты, то во всех трех пробирках осадок растворится. Это будет означать, что во всех случаях прошла химическая реакция, суть которой и отражена с помощью одного и того же ионного уравнения. |
| | | | |
| - | <br>Указанная реакция взаимодействия сильной кислоты со щелочью называется реакцией нейтрализации. Это частный случай реакции обмена. | + | <br> |
| | | | |
| | + | [[Image:Him8-122.jpg|химия 8 класс]]<br> |
| | | | |
| | + | Чтобы в этом убедиться, запишите молекулярные, полные и сокращенные ионные уравнения приведенных реакций. |
| | | | |
| - | Подобная реакция обмена может протекать не только между кислотами и щелочами, но и между кислотами и нерастворимыми основаниями. Например, если получить голубой осадок нерастворимого гидроксида меди (II) взаимодействием сульфата меди і II і со щелочью:
| + | <br>Рассмотрим ионные реакции, которые протекают с образованием газа. В две пробирки нальем по 2 мл растворов карбоната натрия и карбоната калия. Затем в первую прильем раствор соляной, а во вторую — азотной кислоты. В обоих случаях мы заметим характерное "вскипание" из-за выделяющегося углекислого газа. Запишем уравнения реакций для первого случая:<br>[[Image:Him8-124.jpg|химия 8 класс]] |
| | | | |
| - | [[Image:him8-123.jpg]]
| + | <br>Реакции, протекающие в растворах электролитов, эапис каются с помощью ионных уравнений. Эти реакции называл реакциями ионного обмена, так как в растворах электролиты обмениваются своими ионами. Таким образом, можно сделать два вывода.<br> <br>1. Реакции в водных растворах электролитов являются реакциями между ионами, а потому изображаются в виде ионных уравнений.<br>Они проще молекулярных и носят более общий характер. |
| - | | + | |
| - | а затем поделить полученный осадок на три части и прилить к осадку в первой пробирке раствор серной кислоты, к осадку во второй пробирке раствор соляной кислоты, а к осадку в третьей пробирке раствор азотной кислоты, то во всех трех пробирках осадок растворится. Это будет означать, что во всех случаях прошла химическая реакция, суть которой и отражена с помощью одного и того же ионного уравнения.
| + | |
| - | | + | |
| - | | + | |
| - | | + | |
| - | [[Image:him8-122.jpg]]<br>
| + | |
| - | | + | |
| - | Чтобы в этом убедиться, запишите молекулярные, полные и сокращенные ионные уравнения приведенных реакций.
| + | |
| - | | + | |
| - | <br>Рассмотрим ионные реакции, которые протекают с образованием газа. В две пробирки нальем по 2 мл растворов карбоната натрия и карбоната калия. Затем в первую прильем раствор соляной, а во вторую — азотной кислоты. В обоих случаях мы заметим характерное "вскипание" из-за выделяющегося углекислого газа. Запишем уравнения реакций для первого случая:<br>[[Image:him8-124.jpg]]
| + | |
| - | | + | |
| - | <br>Реакции, протекающие в растворах электролитов, эапис каются с помощью ионных уравнений. Эти реакции называл реакциями ионного обмена, так как в растворах электролиты обмениваются своими ионами. Таким образом, можно сделать два вывода.<br> <br>1. Реакции в водных растворах электролитов являются реакциями между ионами, а потому изображаются в виде ионных уравнений.<br>Они проще молекулярных и носят более общий характер. | + | |
| | | | |
| | <br>2. Реакции ионного обмена в растворах электролитов практически необратимо протекают только в том случае, если в результате образуется осадок, газ или малодиссоциирующее вещество.<br><br>1. Молекулярное и ионное уравнения реакций. | | <br>2. Реакции ионного обмена в растворах электролитов практически необратимо протекают только в том случае, если в результате образуется осадок, газ или малодиссоциирующее вещество.<br><br>1. Молекулярное и ионное уравнения реакций. |
| Строка 56: |
Строка 55: |
| | 2. Реакции нониого обмена. | | 2. Реакции нониого обмена. |
| | | | |
| - | 3. Реакции нейтрализации. | + | 3. Реакции нейтрализации. |
| | | | |
| - | <br>Запишите молекулярные и ионные уравнения реакций, о которых говорилось в первой части параграфа, — между сульфатом калия и нитратом бария, между серной кислотой н хлоридом бария. В чем суть обеих реакций? | + | <br>Запишите молекулярные и ионные уравнения реакций, о которых говорилось в первой части параграфа, — между сульфатом калия и нитратом бария, между серной кислотой н хлоридом бария. В чем суть обеих реакций? |
| | | | |
| - | <br>Запишите молекулярное п ионное уравнения реакций, о которых говорилось во второй части параграфа. — между гидроксидом меди (II) и соляной кислотой, между гид-роксидом меди (II) и азотной кислотой. В чем суть обеих реакций? | + | <br>Запишите молекулярное п ионное уравнения реакций, о которых говорилось во второй части параграфа. — между гидроксидом меди (II) и соляной кислотой, между гид-роксидом меди (II) и азотной кислотой. В чем суть обеих реакций? |
| | | | |
| - | <br>Запишите молекулярное и ионное уравнения реакций между карбонатом калия и фосфорной кислотой. Что объединяет ату реакцию и те реакции, о которых говорилось в конце параграфа? | + | <br>Запишите молекулярное и ионное уравнения реакций между карбонатом калия и [[Азотные, калийные и фосфорные удобрения|фосфорной кислотой]]. Что объединяет ату реакцию и те реакции, о которых говорилось в конце параграфа? |
| | | | |
| - | <br>Предложите свои примеры ионных реакций, протекающих с образованием осадков, пользуясь таблицей растворимости. Уравнения реакций запишите в молекулярной и ионной формах.<br> | + | <br>Предложите свои примеры ионных реакций, протекающих с образованием осадков, пользуясь таблицей растворимости. Уравнения реакций запишите в молекулярной и ионной формах.<br> |
| | | | |
| - | [[Image:him8-125.jpg]] | + | [[Image:Him8-125.jpg|химия 8 класс]] |
| | | | |
| - | <br> <sub>рефераты к [[Химия|уроку химии]], цитаты для [[Химия_8_класс|8 класса]], [[Гипермаркет_знаний_-_первый_в_мире!|учебники и пособия]]</sub> | + | <br> <sub>рефераты к [[Химия|уроку химии]], цитаты для [[Химия 8 класс|8 класса]], [[Гипермаркет знаний - первый в мире!|учебники и пособия]]</sub> |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Версия 06:03, 29 июня 2012
Гипермаркет знаний>>Химия>>Химия 8 класс>> Химия: Ионные уравнения Большинство химических реакций протекает в растворах. Растворы электролитов содержат ионы, поэтому реакции и растворах электролитов фактически сводятся к реакциям между ионами.
Реакции между ионами называют ионными реакциями, а уравнения таких реакций - ионными уравнениями.
При составлении ионных уравнении следует руководствоваться тем. что формулы веществ малодиссоцвшрующих. нерастворимых и газообразных записываются в молекулярном виде.
Бели вещество выпадает в осадок, то рядом с его формулой ставят стрелку, направленную вниз, а если в ходе реакции выделяется газообразное вещество, то рядом с его формулой ставят стрелку, направленную вверх.
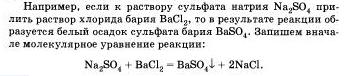
Перепишем это уравнение, изобразив сильные электролиты в виде ионов, а уходящие из сферы реакции - в виде молекул:
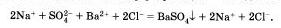
Мы записали, таким обратом, полное ионное уравнение реакции.
Если исключить из обеих частей равенства одинаковые ионы, то есть не участвующие в реакции в левой и правой часто уравнения), то получим сокращенное ионное уравнение реакции:
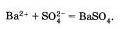
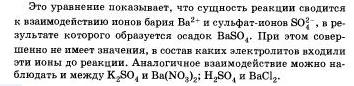
Таким образом, сокращенные ионные уравнения представляют собой уравнения в общем виде, которые характеризуют сущность химической реакции п показывают, какие ионы реагируют и какое вещество образуется в результате.
Реакции ионного обмена протекают до конца в тех случаях, когда образуется или осадок, или малодиссоциирующее вещество, например вода. Беля к раствору гидроксида натрия, окрашенного фенолфталеином в малиновый цвет, прилить избыток раствора азотной кислоты, то раствор обесцветится, что послужит сигналом протекания химической реакции:
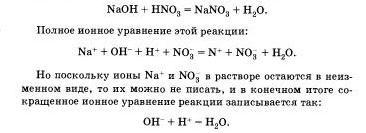
Оно показывает, что взаимодействие сильной кислоты п щелочи сводится к взаимодействию ионов Н+ и ионов ОН -, в результате которого образуется малодиссоцвирующее вещество — вода.
Указанная реакция взаимодействия сильной кислоты со щелочью называется реакцией нейтрализации. Это частный случай реакции обмена.
Подобная реакция обмена может протекать не только между кислотами и щелочами, но и между кислотами и нерастворимыми основаниями. Например, если получить голубой осадок нерастворимого гидроксида меди (II) взаимодействием сульфата меди і II і со щелочью:
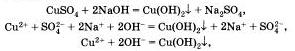
а затем поделить полученный осадок на три части и прилить к осадку в первой пробирке раствор серной кислоты, к осадку во второй пробирке раствор соляной кислоты, а к осадку в третьей пробирке раствор азотной кислоты, то во всех трех пробирках осадок растворится. Это будет означать, что во всех случаях прошла химическая реакция, суть которой и отражена с помощью одного и того же ионного уравнения.
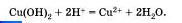
Чтобы в этом убедиться, запишите молекулярные, полные и сокращенные ионные уравнения приведенных реакций.
Рассмотрим ионные реакции, которые протекают с образованием газа. В две пробирки нальем по 2 мл растворов карбоната натрия и карбоната калия. Затем в первую прильем раствор соляной, а во вторую — азотной кислоты. В обоих случаях мы заметим характерное "вскипание" из-за выделяющегося углекислого газа. Запишем уравнения реакций для первого случая:
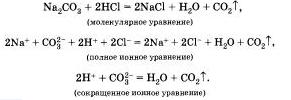
Реакции, протекающие в растворах электролитов, эапис каются с помощью ионных уравнений. Эти реакции называл реакциями ионного обмена, так как в растворах электролиты обмениваются своими ионами. Таким образом, можно сделать два вывода.
1. Реакции в водных растворах электролитов являются реакциями между ионами, а потому изображаются в виде ионных уравнений.
Они проще молекулярных и носят более общий характер.
2. Реакции ионного обмена в растворах электролитов практически необратимо протекают только в том случае, если в результате образуется осадок, газ или малодиссоциирующее вещество.
1. Молекулярное и ионное уравнения реакций.
2. Реакции нониого обмена.
3. Реакции нейтрализации.
Запишите молекулярные и ионные уравнения реакций, о которых говорилось в первой части параграфа, — между сульфатом калия и нитратом бария, между серной кислотой н хлоридом бария. В чем суть обеих реакций?
Запишите молекулярное п ионное уравнения реакций, о которых говорилось во второй части параграфа. — между гидроксидом меди (II) и соляной кислотой, между гид-роксидом меди (II) и азотной кислотой. В чем суть обеих реакций?
Запишите молекулярное и ионное уравнения реакций между карбонатом калия и фосфорной кислотой. Что объединяет ату реакцию и те реакции, о которых говорилось в конце параграфа?
Предложите свои примеры ионных реакций, протекающих с образованием осадков, пользуясь таблицей растворимости. Уравнения реакций запишите в молекулярной и ионной формах.
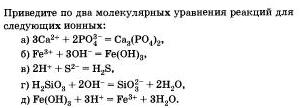
рефераты к уроку химии, цитаты для 8 класса, учебники и пособия
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|