|
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Неметаллы: атомы и простые вещества. Кислород, озон, воздух
Все химические элементы разделяют на металлы и неметаллы в зависимости от строения и свойств их атомов. Также на металлы и неметаллы классифицируют образуемые элементами простые вещества, исходя из их физических и химических свойств.
С металлами вы познакомились в предыдущей главе. Теперь перейдем к рассмотрению неметаллов.
Само слово «неметаллы» указывает, что свойства неметаллических элементов и соответствующих им простых веществ противоположны свойствам металлов.
Если для атомов металлов характерны сравнительно большие радиусы и небольшое число электронов на внешнем уровне (1е-, З- ), атомам неметаллов, наоборот, свойственны небольшие радиусы атомов и число электронов на внешнем энергетическом уровне от 4 до 8 (у бора этих электронов 3, но атомы этого элемента имеют очень небольшой радиус). Отсюда и стремление атомов металлов к отдаче внешних электронов, т. е. восстановительные свойства, а для атомов неметаллов — стремление к приему недостающих до заветной восьмерки электронов, т. е. окислительные свойства.
Среди 109 известных сегодня химических элементов (из них 88 элементов найдено в природе) к неметаллам относят 22 элемента. О расположении металлов и неметаллов в периодической системе элементов мы уже рассказывали в предыдущей главе. Здесь еще раз отметим, что металлы в периодической системе расположены в основном под диагональю В—Аt, а неметаллы — по этой диагонали и над ней.
Свойства простых веществ, образуемых неметаллами, отличаются большим разнообразием. Хотя по сравнению с металлами неметаллов гораздо меньше, для них трудно выделить общие характерные признаки. Судите сами: водород Н2, кислород и озон 02 и 03, фтор F2, хлор Сl2, азот — газы при обычных условиях, бром Вr2 — жидкость, а бор, углерод (алмаз, графит), кремний, фосфор (красный и белый), сера (пластическая и ромбическая), селен, теллур, иод 12, астат — твердые вещества.
Если для подавляющего большинства металлов характерен серебристо-белый цвет, то окраска неметаллов — простых веществ охватывает все цвета спектра: красный (красный фосфор, красно-бурый жидкий бром), желтый (сера), зеленый (хлор — желто-зеленый газ), фиолетовый (пары иода).
Температуры плавления неметаллов также лежат в очень широком интервале: от 3800 °С у графита до -210 °С у азота. Эта особенность свойств неметаллов является следствием образования ими двух типов кристаллических решеток: молекулярной (O2, N2, галогены, белый фосфор и др.) и атомной (алмаз, графит, кремний, бор и др.). Разным строением кристаллических решеток объясняется и явление аллотропии (вспомните, что это такое). Например, элемент фосфор образует простое вещество с молекулярной кристаллической решеткой — белый фосфор, молекулы которого имеют состав Р4, и простое вещество с атомной кристаллической решеткой — красный фосфор Р.
Вторая причина аллотропии связана с разным числом атомов в молекулах простых веществ. Типичный пример — простые вещества, образуемые кислородом: обычный кислород 02 и озон O3.
В отличие от бесцветного кислорода О2, не имеющего запаха, озон — это светло-синий газ с сильным запахом. Вы уже знаете из курса прошлого года, что примесь озона в воздухе, появляющаяся после грозы, дает ощущение приятной свежести; содержится озон и в воздухе сосновых лесов и морского побережья.
В природе озон образуется при электрических разрядах или окислении органических смолистых веществ, а также при действии ультрафиолетовых лучей на кислород. В лаборатории его получают в специальных приборах — озонаторах при действии на кислород тихим (без искр) электрическим разрядом (рис. 16).
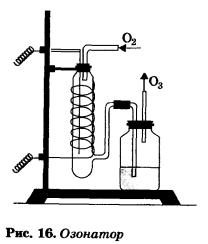
Озон — гораздо более сильный окислитель, чем кислород. Его молекулы распадаются при обычной температуре с отщеплением атомарного кислорода:
О3 = О2 + О
На сильной окислительной способности озона основано его применение: отбеливание тканей, удаление запаха у жиров и масел, дезинфекция воздуха в помещениях, обеззараживание питьевой воды.
Озон имеет очень большое значение для сохранения всего живого на нашей планете. Напомним, что озоновый пояс Земли, расположенный на высоте 20—25 км, задерживает губительные ультрафиолетовые лучи, которые разрушительно действуют на клетки живых организмов. Поэтому понятно, как важно сохранить этот весьма чувствительный к действию различных химических веществ «озоновый щит» планеты от разрушения.
Озон относят к переменным составляющим воздуха. Еще в конце ХVIII в. Лавуазье установил, что воздух не простое вещество, а смесь газообразных неметаллов: азота — (на его
долю приходится 4/5 объема воздуха) и кислорода — 02 (с объемной долей 1/5). В дальнейшем представления о составе воздуха были уточнены. В настоящее время различают постоянные, переменные и случайные составные части воздуха.
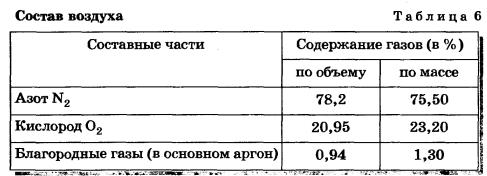
Постоянные составные части воздуха — это кислород, азот и благородные газы (аргон, неон и т. п.), содержание их в воздухе одинаково везде у поверхности Земли (табл. 6).
Переменные составные части воздуха — это углекислый газ (около 0,03% по объему), водяные пары и озон. Содержание их может сильно изменяться в зависимости от природных и промышленных условий.
К случайным составным частям воздуха относят пыль, микроорганизмы, пыльцу растений, некоторые газы, в том числе и те, которые образуют кислотные дожди: оксиды серы, азота и др.
Воздух, свободный от переменных и случайных составных частей, прозрачен, лишен цвета, вкуса и запаха, 1 л его при н. у. имеет массу 1,29 г, а 22,4 л, т. е. молярный объем, весит 29 г.
Воздух — это океан из газов, на дне которого живут люди, животные и растения. Он необходим для дыхания и фотосинтеза. Растворенный в воде кислород воздуха служит для дыхания обитателей водной среды (рыб, водных растений).
Велика роль воздуха в процессах выветривания (разрушения) горных пород и для почвообразования. Под действием воздуха и бактерий минерализуются органические остатки — отжившие органические вещества превращаются в минеральные соединения и снова усваиваются растениями.
Из жидкого воздуха получают азот и кислород, используя разные температуры их кипения (при перегонке сжиженного воздуха первым испаряется азот).
1. Элементы-металлы и элементы-неметаллы. Строение атомов неметаллов.
2. Простые вещества-металлы и простые вещества-неметаллы.
3. Аллотропия. Кислород и озон.
4. Состав воздуха.
Определите, во сколько раз тяжелее (легче) воздуха кислород, углекислый газ, водород, т. е. определите относительную плотность этих газов по воздуху D возд.
Зная объемный состав воздуха, найдите количество (т. е. число молей) каждого газа: азота и кислорода — в 100 л воздуха при н. у.
Определите число молекул а) кислорода, б) азота, содержащихся в 22,4 л воздуха при н. у.
Какой объем воздуха (н. у.) потребуется для сжигания 20 м3 сероводорода, если при этом образуются вода и оксид серы(IV)? Какова масса этого воздуха?
Приготовьте сообщение о применении кислорода.
Что такое озоновые дыры? Как предупредить их появление?
всё для подготовки домашнего задания, исправления и дополнения к урокам, фишки для любознательных
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|












