|
|
|
| (5 промежуточных версий не показаны.) | | Строка 1: |
Строка 1: |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Физика и астрономия|Физика и астрономия]]>>[[Физика 10 класс|Физика 10 класс]]>>Физика: Первый закон термодинамики ''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Физика и астрономия|Физика и астрономия]]>>[[Физика 10 класс|Физика 10 класс]]>>Физика: Первый закон термодинамики ''' |
| - |
| |
| - | <br>
| |
| | | | |
| | <metakeywords>Физика, 10 класс, Первый закон термодинамики</metakeywords> | | <metakeywords>Физика, 10 класс, Первый закон термодинамики</metakeywords> |
| | | | |
| - | Первый закон термодинамики - это закон сохранения энергии, распространенный на тепловые явления. Он показывает, от каких причин зависит изменение внутренней энергии.<br> '''Закон сохранения энергии.''' К середине XIX в. многочисленные опыты доказали, что ''механическая энергия'' ''никогда не пропадает бесследно''. Падает, например, молот на кусок свинца, и свинец нагревается вполне определенным образом. Силы трения тормозят тела, которые при этом разогреваются.<br> На основании множества подобных наблюдений и обобщения опытных фактов был сформулирован '''''закон сохранения энергии:'''''<br> '''''Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит из одной формы в другую.'''''<br> Закон сохранения энергии управляет всеми явлениями природы и связывает их воедино. Он всегда выполняется абсолютно точно, неизвестно ни одного случая, когда бы этот великий закон не выполнялся.<br> Этот закон был открыт в середине XIX в. немецким ученым, врачом по образованию Р. Майером (1814-1878), английским ученым Дж. Джоулем (1818-1889) и получил наиболее точную формулировку в трудах немецкого ученого Г. Гельмгольца (1821-1894).<br> '''Первый закон термодинамики.''' Закон сохранения и превращения энергии, распространенный на тепловые явления, носит название ''первого закона термодинамики.''<br> В термодинамике рассматриваются тела, положение центра тяжести которых практически не меняется. Механическая энергия таких тел остается постоянной, изменяться может лишь внутренняя энергия каждого тела.<br> До сих пор мы рассматривали процессы, в которых внутренняя энергия системы изменялась либо за счет совершения работы, либо за счет теплообмена с окружающими телами.<br> В ''общем случае'' при переходе системы из одного состояния в другое внутренняя энергия изменяется одновременно как за счет совершения работы, так и за счет передачи теплоты. '''''Первый закон термодинамики''''' формулируется именно для таких общих случаев:<br> '''''Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:'''''
| + | <h2>Закон сохранения энергии</h2> |
| | + | |
| | + | Первый закон термодинамики - это закон сохранения энергии, распространенный на тепловые явления. Он показывает, от каких причин зависит изменение внутренней энергии. |
| | + | |
| | + | К середине XIX в. многочисленные опыты доказали, что ''механическая энергия'' ''никогда не пропадает бесследно''. Падает, например, молот на кусок свинца, и свинец нагревается вполне определенным образом. [[Закон_Гука._Силы_трения|Силы трения]] тормозят тела, которые при этом разогреваются. |
| | + | |
| | + | На основании множества подобных наблюдений и обобщения опытных фактов был сформулирован закон сохранения энергии: |
| | + | |
| | + | '''Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит из одной формы в другую.''' |
| | + | |
| | + | Закон сохранения энергии управляет всеми явлениями [[Поэзия_родной_природы.|природы]] и связывает их воедино. Он всегда выполняется абсолютно точно, неизвестно ни одного случая, когда бы этот великий закон не выполнялся. |
| | + | |
| | + | Этот закон был открыт в середине XIX в. немецким ученым, врачом по образованию Р. Майером (1814-1878), английским ученым Дж. Джоулем (1818-1889) и получил наиболее точную формулировку в трудах немецкого ученого Г. Гельмгольца (1821-1894). |
| | + | |
| | + | <h2>Первый закон термодинамики</h2> |
| | + | |
| | + | Закон сохранения и превращения энергии, распространенный на тепловые явления, носит название первого закона термодинамики. |
| | + | |
| | + | В термодинамике рассматриваются тела, положение центра тяжести которых практически не меняется. Механическая энергия таких тел остается постоянной, изменяться может лишь внутренняя энергия каждого тела. |
| | + | |
| | + | До сих пор мы рассматривали процессы, в которых внутренняя энергия системы изменялась либо за счет совершения работы, либо за счет теплообмена с окружающими телами. |
| | + | |
| | + | В ''общем случае'' при переходе системы из одного состояния в другое внутренняя энергия изменяется одновременно как за счет совершения работы, так и за счет передачи теплоты. |
| | + | |
| | + | Первый закон [[Применение_первого_закона_термодинамики_к_различным_процессам|термодинамики]] формулируется именно для таких общих случаев: |
| | + | |
| | + | Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе: |
| | + | |
| | + | [[Image:A78-1.jpg|center|216x32px|Первый закон термодинамики]] |
| | + | |
| | + | Если система является изолированной, то работа внешних сил равна нулю (''А'' = 0) и система не обменивается теплотой с окружающими телами (''Q'' = 0). В этом случае согласно первому закону термодинамики [[Image:A78-3.jpg|152x18px|A78-3.jpg]] или ''U<sub>1</sub>=U<sub>2</sub>. Внутренняя энергия изолированной системы остается неизменной (сохраняется). |
| | + | |
| | + | Часто вместо работы ''A'' внешних тел над системой рассматривают работу ''A´'' системы над внешними телами. Учитывая, что [[Image:A78-5.jpg|79x17px|A78-5.jpg]], первый закон термодинамики (13.10) можно записать так: |
| | + | |
| | + | <br>[[Image:A78-2.jpg|center|214x17px|Первый закон термодинамики]] |
| | + | |
| | + | Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами. |
| | + | |
| | + | <h2>Невозможность создания вечного [[Двигатель_внутреннего_сгорания|двигателя]]</h2> |
| | + | |
| | + | Из первого закона термодинамики вытекает невозможность создания вечного двигателя - устройства, способного совершать неограниченное количество работы без затрат топлива или каких-либо других материалов. Если к системе не поступает тепло (''Q''=0), то работа ''A´'' согласно уравнению (13.11) может быть совершена только за счет убыли внутренней энергии: [[Image:A78-6.jpg|78x14px|A78-6.jpg]]. После того как запас энергии окажется исчерпанным, двигатель перестанет работать. |
| | + | |
| | + | <h2>Работа и количество теплоты - характеристики процесса изменения внутренней энергии</h2> |
| | + | |
| | + | В данном состоянии система всегда обладает определенной внутренней энергией. |
| | + | |
| | + | Но нельзя говорить, что в системе содержится определенное количество теплоты или работы. Как работа, так и количество теплоты являются величинами, характеризующими ''изменение внутренней энергии'' системы в результате того или иного процесса. |
| | + | |
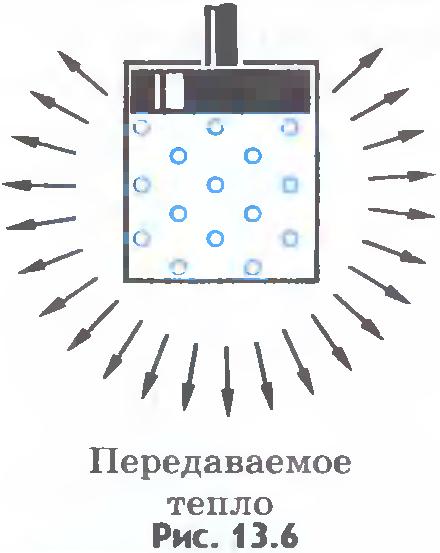
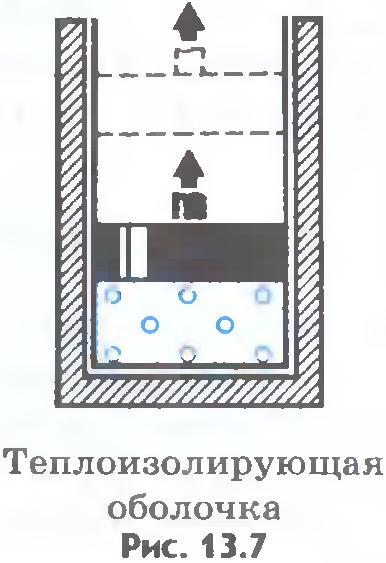
| | + | Внутренняя энергия системы может измениться одинаково как за счет совершения системой работы, так и за счет передачи окружающим телам какого-либо количества теплоты. Например, нагретый газ в цилиндре может уменьшить свою энергию остывая, без совершения работы (''рис.13.6''). Но он может потерять точно такое же количество энергии, перемещая поршень, без отдачи теплоты окружающим телам. Для этого стенки цилиндра и поршень должны быть теплонепроницаемыми (''рис.13.7''). |
| | + | |
| | + | <br>[[Image:A13.6.jpg|center|201x253px|Первый закон термодинамики]][[Image:A13.7.jpg|center|183x267px|Первый закон термодинамики]] |
| | + | |
| | + | В дальнейшем на протяжении всего курса [[Загадка_квантовой_физики|физики]] мы будем знакомиться с другими формами энергии, способами их превращения и передачи. |
| | + | |
| | + | Внутренняя энергия системы тел изменяется при совершении работы и при передаче количества теплоты. В каждом состоянии система обладает определенной внутренней энергией. Работа и количество теплоты не содержатся в теле, а характеризуют процесс изменения его внутренней энергии. |
| | + | |
| | + | <h2>История возникновения термодинамики</h2> |
| | + | |
| | + | Каждый из нас владеет способом подсознательно ощущать тепло и холод. Это происходит на интуитивном уровне. Человек имел представление о температурном режиме еще задолго до того, как появились научные теории о нагреве тел. |
| | + | |
| | + | Но современный человек привык к благам цивилизации и многие полезные вещи ему кажутся привычными. Сейчас у каждого дома для измерения температуры есть современные термометры или градусники. Но такие приборы появились не так уж и давно. В древние времена, естественно, что никаких градусников не существовало и в помине. Очень долго люди для определения температуры тела пользовались своими ощущениями. Понятиями холодный, теплый и горячий человек руководствовался до тех пор, пока не был изобретен термоскоп. |
| | + | |
| | + | Знания о теплоте на научной основе стали развиваться с изобретения этого прибора. Если верить историческим данным, то изобретателем первого термоскопа был ученый и астроном Галилео Галилей. Благодаря этому новому изобретению в те времена человек мог определять степень «нагретости» тела. Вот так можно сказать, что с этого момента началась история развития термодинамики. |
| | | | |
| - | [[Image:a78-1.jpg|center]] Если система является изолированной, то работа внешних сил равна нулю (''А'' = 0) и система не обменивается теплотой с окружающими телами (''Q'' = 0). В этом случае согласно первому закону термодинамики [[Image:a78-3.jpg]] или ''U<sub>1</sub>=U<sub>2</sub>. Внутренняя энергия изолированной системы остается неизменной (сохраняется).''<br> Часто вместо работы ''A'' внешних тел над системой рассматривают работу ''A´'' системы над внешними телами. Учитывая, что [[Image:a78-5.jpg]], первый закон термодинамики (13.10) можно записать так:<br>[[Image:a78-2.jpg|center]] Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.<br> '''Невозможность создания вечного двигателя.''' Из первого закона термодинамики вытекает невозможность создания вечного двигателя - устройства, способного совершать неограниченное количество работы без затрат топлива или каких-либо других материалов. Если к системе не поступает тепло (''Q''=0), то работа ''A´'' согласно уравнению (13.11) может быть совершена только за счет убыли внутренней энергии: [[Image:a78-6.jpg]]. После того как запас энергии окажется исчерпанным, двигатель перестанет работать.<br> '''Работа и количество теплоты - характеристики процесса изменения внутренней энергии.''' В данном состоянии система всегда обладает определенной внутренней энергией.<br> Но нельзя говорить, что в системе содержится определенное количество теплоты или работы. Как работа, так и количество теплоты являются величинами, характеризующими ''изменение внутренней энергии'' системы в результате того или иного процесса.<br> Внутренняя энергия системы может измениться одинаково как за счет совершения системой работы, так и за счет передачи окружающим телам какого-либо количества теплоты. Например, нагретый газ в цилиндре может уменьшить свою энергию остывая, без совершения работы (''рис.13.6''). Но он может потерять точно такое же количество энергии, перемещая поршень, без отдачи теплоты окружающим телам. Для этого стенки цилиндра и поршень должны быть теплонепроницаемыми (''рис.13.7'').<br>[[Image:a13.6.jpg|center]][[Image:a13.7.jpg|center]] В дальнейшем на протяжении всего курса физики мы будем знакомиться с другими формами энергии, способами их превращения и передачи.<br> Внутренняя энергия системы тел изменяется при совершении работы и при передаче количества теплоты. В каждом состоянии система обладает определенной внутренней энергией. Работа и количество теплоты не содержатся в теле, а характеризуют процесс изменения его внутренней энергии.<br><br><br> ???<br> 1. Как формулируется первый закон термодинамики?<br> 2. В каком случае изменение внутренней энергии отрицательно?<br> 3. Почему можно говорить, что система обладает внутренней энергией, но нельзя сказать, что она обладает запасом определенного количества теплоты или работы?<br>
| |
| | <br> | | <br> |
| | + | [[Image:10kl_Termodinamika001.jpg|500x500px|термодинамика]] |
| | + | <br> |
| | + | |
| | + | Однако, прибор Галилея имел значительный недостаток, так как показания термоскопа |
| | + | зависели от давления атмосферы, и поэтому появилась необходимость в его совершенствовании. В 1714 году был изобретен еще один прибор, который отдаленно напоминал теперешний термометр. Он собой представлял колбу, которую вначале наполняли водой, а потом добавляли ртуть или спирт. Такой ртутный термометр был изобретен немецким физиком Габриэлем Фаренгейтом. |
| | | | |
| - | ''Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс''
| + | Но измерение температуры по Фарингейту было не совсем удобно, поэтому французский учёный Реомюр предложил шкалу Цельсия, которая успешно пользуется популярностью, по сей день. |
| | | | |
| | + | <br> |
| | + | [[Image:10kl_Termodinamika02.jpg|500x500px|термодинамика]] |
| | <br> | | <br> |
| | | | |
| - | <sub>Планирования [[Физика и астрономия|по физике]], учебники и книги онлайн, курсы и задания [[Физика 10 класс|по физике для 10 класса]]</sub>
| + | Термодинамика – это наука об основных способах, с помощью которых происходит преобразование внутренней энергии тел для осуществления механической работы. |
| | | | |
| - | '''<u>Содержание урока</u>'''
| + | <h2>Где нашла применение термодинамика</h2> |
| - | '''[[Image:1236084776 kr.jpg|10x10px]] конспект урока '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас
| + | Так как все законы термодинамики имеют общий характер, и кроме того, не зависят от конкретных деталей строения вещества на уровне атомов, то они широко применяются в различных научных и технических вопросах. Термодинамика нашла широкое применение в области энергетики, тепловой техники, в химических реакциях, фазовых переходах и даже «черных дырах». |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы
| + | Без термодинамики не обойтись в физических науках, химических, ее используют в машиностроении, аэрокосмической отрасли. Она имеет огромное значение в клеточной биологии, медицине и даже в экономике. |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии
| + | |
| - |
| + | '''Задание''' |
| - | '''<u>Практика</u>'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников
| + | |
| - |
| + | |
| - | '''<u>Иллюстрации</u>'''
| + | |
| - | '''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты
| + | |
| - |
| + | |
| - | '''<u>Дополнения</u>'''
| + | |
| - | '''[[Image:1236084776 kr.jpg|10x10px]] рефераты'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие
| + | |
| - |
| + | |
| - | <u>Совершенствование учебников и уроков
| + | |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми
| + | |
| - |
| + | |
| - | '''<u>Только для учителей</u>'''
| + | |
| - | '''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения
| + | |
| - |
| + | |
| - |
| + | |
| - | '''<u>Интегрированные уроки</u>'''
| + | |
| - |
| + | |
| | | | |
| - | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам].
| + | 1. Как формулируется первый закон термодинамики?<br> |
| | + | 2. В каком случае изменение внутренней энергии отрицательно?<br> |
| | + | 3. Почему можно говорить, что система обладает внутренней энергией, но нельзя сказать, что она обладает запасом определенного количества [[Количество_теплоты|теплоты]] или работы?<br> |
| | | | |
| - | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум].
| + | ''Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс'' |
Текущая версия на 08:59, 29 июня 2015
Гипермаркет знаний>>Физика и астрономия>>Физика 10 класс>>Физика: Первый закон термодинамики
Закон сохранения энергии
Первый закон термодинамики - это закон сохранения энергии, распространенный на тепловые явления. Он показывает, от каких причин зависит изменение внутренней энергии.
К середине XIX в. многочисленные опыты доказали, что механическая энергия никогда не пропадает бесследно. Падает, например, молот на кусок свинца, и свинец нагревается вполне определенным образом. Силы трения тормозят тела, которые при этом разогреваются.
На основании множества подобных наблюдений и обобщения опытных фактов был сформулирован закон сохранения энергии:
Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит из одной формы в другую.
Закон сохранения энергии управляет всеми явлениями природы и связывает их воедино. Он всегда выполняется абсолютно точно, неизвестно ни одного случая, когда бы этот великий закон не выполнялся.
Этот закон был открыт в середине XIX в. немецким ученым, врачом по образованию Р. Майером (1814-1878), английским ученым Дж. Джоулем (1818-1889) и получил наиболее точную формулировку в трудах немецкого ученого Г. Гельмгольца (1821-1894).
Первый закон термодинамики
Закон сохранения и превращения энергии, распространенный на тепловые явления, носит название первого закона термодинамики.
В термодинамике рассматриваются тела, положение центра тяжести которых практически не меняется. Механическая энергия таких тел остается постоянной, изменяться может лишь внутренняя энергия каждого тела.
До сих пор мы рассматривали процессы, в которых внутренняя энергия системы изменялась либо за счет совершения работы, либо за счет теплообмена с окружающими телами.
В общем случае при переходе системы из одного состояния в другое внутренняя энергия изменяется одновременно как за счет совершения работы, так и за счет передачи теплоты.
Первый закон термодинамики формулируется именно для таких общих случаев:
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
Если система является изолированной, то работа внешних сил равна нулю (А = 0) и система не обменивается теплотой с окружающими телами (Q = 0). В этом случае согласно первому закону термодинамики 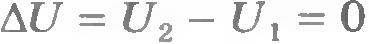 или U1=U2. Внутренняя энергия изолированной системы остается неизменной (сохраняется). или U1=U2. Внутренняя энергия изолированной системы остается неизменной (сохраняется).
Часто вместо работы A внешних тел над системой рассматривают работу A´ системы над внешними телами. Учитывая, что  , первый закон термодинамики (13.10) можно записать так: , первый закон термодинамики (13.10) можно записать так:
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Невозможность создания вечного двигателя
Из первого закона термодинамики вытекает невозможность создания вечного двигателя - устройства, способного совершать неограниченное количество работы без затрат топлива или каких-либо других материалов. Если к системе не поступает тепло (Q=0), то работа A´ согласно уравнению (13.11) может быть совершена только за счет убыли внутренней энергии:  . После того как запас энергии окажется исчерпанным, двигатель перестанет работать. . После того как запас энергии окажется исчерпанным, двигатель перестанет работать.
Работа и количество теплоты - характеристики процесса изменения внутренней энергии
В данном состоянии система всегда обладает определенной внутренней энергией.
Но нельзя говорить, что в системе содержится определенное количество теплоты или работы. Как работа, так и количество теплоты являются величинами, характеризующими изменение внутренней энергии системы в результате того или иного процесса.
Внутренняя энергия системы может измениться одинаково как за счет совершения системой работы, так и за счет передачи окружающим телам какого-либо количества теплоты. Например, нагретый газ в цилиндре может уменьшить свою энергию остывая, без совершения работы (рис.13.6). Но он может потерять точно такое же количество энергии, перемещая поршень, без отдачи теплоты окружающим телам. Для этого стенки цилиндра и поршень должны быть теплонепроницаемыми (рис.13.7).
В дальнейшем на протяжении всего курса физики мы будем знакомиться с другими формами энергии, способами их превращения и передачи.
Внутренняя энергия системы тел изменяется при совершении работы и при передаче количества теплоты. В каждом состоянии система обладает определенной внутренней энергией. Работа и количество теплоты не содержатся в теле, а характеризуют процесс изменения его внутренней энергии.
История возникновения термодинамики
Каждый из нас владеет способом подсознательно ощущать тепло и холод. Это происходит на интуитивном уровне. Человек имел представление о температурном режиме еще задолго до того, как появились научные теории о нагреве тел.
Но современный человек привык к благам цивилизации и многие полезные вещи ему кажутся привычными. Сейчас у каждого дома для измерения температуры есть современные термометры или градусники. Но такие приборы появились не так уж и давно. В древние времена, естественно, что никаких градусников не существовало и в помине. Очень долго люди для определения температуры тела пользовались своими ощущениями. Понятиями холодный, теплый и горячий человек руководствовался до тех пор, пока не был изобретен термоскоп.
Знания о теплоте на научной основе стали развиваться с изобретения этого прибора. Если верить историческим данным, то изобретателем первого термоскопа был ученый и астроном Галилео Галилей. Благодаря этому новому изобретению в те времена человек мог определять степень «нагретости» тела. Вот так можно сказать, что с этого момента началась история развития термодинамики.
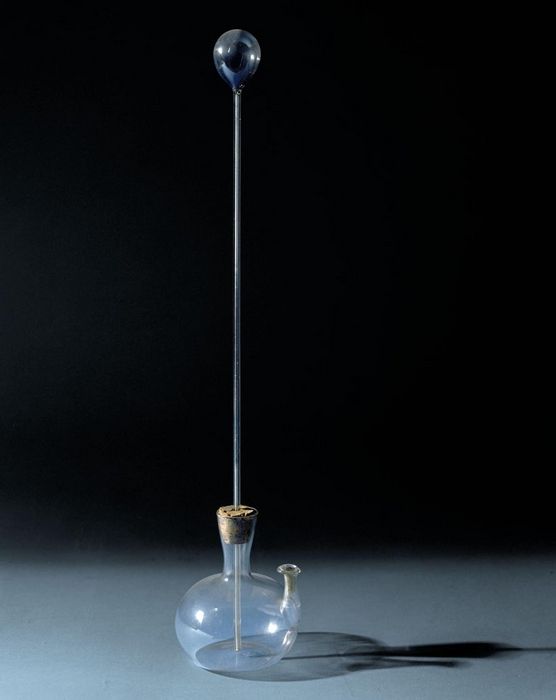
Однако, прибор Галилея имел значительный недостаток, так как показания термоскопа
зависели от давления атмосферы, и поэтому появилась необходимость в его совершенствовании. В 1714 году был изобретен еще один прибор, который отдаленно напоминал теперешний термометр. Он собой представлял колбу, которую вначале наполняли водой, а потом добавляли ртуть или спирт. Такой ртутный термометр был изобретен немецким физиком Габриэлем Фаренгейтом.
Но измерение температуры по Фарингейту было не совсем удобно, поэтому французский учёный Реомюр предложил шкалу Цельсия, которая успешно пользуется популярностью, по сей день.
Термодинамика – это наука об основных способах, с помощью которых происходит преобразование внутренней энергии тел для осуществления механической работы.
Где нашла применение термодинамика
Так как все законы термодинамики имеют общий характер, и кроме того, не зависят от конкретных деталей строения вещества на уровне атомов, то они широко применяются в различных научных и технических вопросах. Термодинамика нашла широкое применение в области энергетики, тепловой техники, в химических реакциях, фазовых переходах и даже «черных дырах».
Без термодинамики не обойтись в физических науках, химических, ее используют в машиностроении, аэрокосмической отрасли. Она имеет огромное значение в клеточной биологии, медицине и даже в экономике.
Задание
1. Как формулируется первый закон термодинамики?
2. В каком случае изменение внутренней энергии отрицательно?
3. Почему можно говорить, что система обладает внутренней энергией, но нельзя сказать, что она обладает запасом определенного количества теплоты или работы?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
|