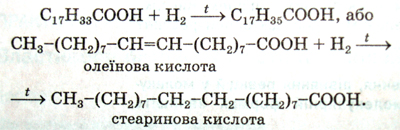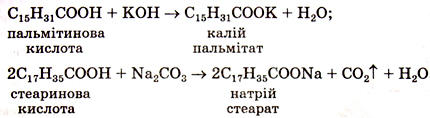|
|
|
| (12 промежуточных версий не показаны.) | | Строка 1: |
Строка 1: |
| - | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 11 клас]]>>[[Хімія 11 клас|Хімія 11 клас]]>> Хімія: Органічні сполуки в побуті. Поняття про побутові хімікати. Загальні правила поводження з побутовими хімікатами. Мило, його склад, мийна дія. Синтетичні мийні засоби. Захист навколишнього середовища від забруднення синтетичними мийними засобами. Органічні розчинники, їх застосування. Попередження забруднення середовища при використанні органічних речовин у побуті''' | + | '''[[Гіпермаркет Знань - перший в світі!|<metakeywords>Хімією, клас, урок 13, на тему, 11 клас, мило, побутові хімікати, мийні засоби, синтетичні мийні засоби</metakeywords>Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 11 клас|Хімія 11 клас]]>>Органічні сполуки в побуті. Поняття про побутові хімікати. Загальні правила поводження з побутовими хімікатами. Мило, його склад, мийна дія. Синтетичні мийні засоби. Захист навколишнього середовища від забруднення синтетичними мийними засобами. Органічні розчинники, їх застосування. Попередження забруднення середовища при використанні органічних речовин у побуті''' |
| | | | |
| - | <br> Вищі кислоти – це карбонові кислоти, молекули яких містять 10 і більше атомів Карбону. Серед них найважливішими є насичені кислоти – пальмітинова С<sub>15</sub>Н<sub>31</sub>СООН і стеаринова С<sub>17</sub>Н<sub>35</sub>СООН, а також ненасичена олеїнова С<sub>17</sub>Н<sub>33</sub>СООН. Ці кислоти раніше добували тільки з рослинних і тваринних жирів, тому їх ще називають ''жирними кислотами''.<br> Пальмітинова і стеаринова кислоти – тверді речовини, а олеїнова – рідина. Сполуки практично не розчиняються у воді.<br> Хімічні властивості вищих карбонових кислот, як і нижчих кислот, зумовлені насамперед наявністю <br>функціональної групи – СООН. Вищі карбонові кислоти дуже слабкі; вони реагують з лугами й спиртами.<br> Олеїнова кислота є ненасиченою сполукою і тому здатна вступати реакції приєднання з галогенами, галогеноводнями тощо. Реагуючи з воднем, вона перетворюється на стеаринову кислоту:<br><br> Крім того, олеїнова кислота може окислюватися калій перманганатом та іншими окисниками.<br>Вищі карбонові кислоти добувають гідролізом природних жирів, а також окисненням високомолекулярних <br>вуглеводнів нафти. | + | <br> Вищі кислоти – це карбонові кислоти, молекули яких містять 10 і більше атомів Карбону. Серед них найважливішими є насичені кислоти – пальмітинова С<sub>15</sub>Н<sub>31</sub>СООН і стеаринова С<sub>17</sub>Н<sub>35</sub>СООН, а також ненасичена олеїнова С<sub>17</sub>Н<sub>33</sub>СООН. Ці кислоти раніше добували тільки з рослинних і тваринних жирів, тому їх ще називають жирними кислотами.<br> |
| | + | |
| | + | Пальмітинова і стеаринова кислоти – тверді речовини, а олеїнова – рідина. Сполуки практично не розчиняються у воді.<br> |
| | + | |
| | + | Хімічні властивості вищих карбонових кислот, як і нижчих [[13._Кислоти,_їх_склад,_назви|кислот]], зумовлені насамперед наявністю <br>функціональної групи – СООН. Вищі карбонові кислоти дуже слабкі; вони реагують з лугами й спиртами.<br> |
| | + | |
| | + | Олеїнова кислота є ненасиченою сполукою і тому здатна вступати реакції приєднання з галогенами, галогеноводнями тощо. Реагуючи з воднем, вона перетворюється на стеаринову кислоту: |
| | + | |
| | + | <br> [[Image:First salt.jpg|400px|Кислоти]]<br> |
| | + | |
| | + | Крім того, олеїнова кислота може окислюватися калій перманганатом та іншими окисниками.<br>Вищі карбонові кислоти добувають гідролізом природних жирів, а також окисненням високомолекулярних <br>вуглеводнів [[Тема_8._Нафта._Склад,_властивості_нафти._Продукти_перегонки_нафти,_їх_застосування._Детонаційна_стійкість_бензину|нафти]]. |
| | | | |
| | <br>'''Мила'''. | | <br>'''Мила'''. |
| | | | |
| - | Широкого застосування набули солі жирних кислот – мила. Натрієві солі є твердими речовинами, а <br>калієві – рідкими. Їхні аніони містять від 10 до 20 атомів Карбону. (Якщо атомів Карбону в аніоні солі <br>менше 10, то сполука не виявляє мийної дії, а якщо більше 20, то сіль практично нерозчинна в воді.)<br> Мило виробляли вже із середніх віків. Традиційний процес миловаріння полягає в нагріванні жирів із лугом <br>до утворення однорідної тягучої рідини. При добавлянні до неї насиченого розчину кухонної солі розчинність мила зменшується, воно виділяється з розчину і спливає на поверхню. Цей процес називається ''висолюванням''. Мило збирають і заповнюють ним форми, де воно твердне.<br> Інший спосіб виготовлення мила полягає в дії лугу або соди на жирні кислоти:<br><br> Мийна дія мила полягає у відокремленні частинок бруду, наприклад від поверхні тканини, й утворенні <br>емульсії чи суспензії. Розглянемо, як це відбувається.<br> Потрапляючи у воду, мило розчиняється і зазнає неповного гідролізу:<br><br>Аніон карбонової кислоти складається із двох частин – полярної (-СООН<sup>-</sup>) і неполярної (наприклад, С<sub>17</sub>Н<sub>35</sub>-).<br> Неполярна (гідрофобна) частина аніона контактує із жировою складовою забруднення, а полярна <br>(гідрофільна) залишається у воді, сполучаючись з її молекулами водневими зв’язками (як показано на <br>малюнку нижче). Луг сприяє відокремленню частинок жирових забруднень від шкіри або тканини та їх <br>подрібненню, а аніони кислоти – утворенню піни, в якій ці часточки утримуються.<br><br> Мила належать до поверхнево-активних речовин(скорочено - ПАР). Це група органічних сполук, які містять полярні(гідрофільні) групи атомів різного складу і неполярні (гідрофобні) вуглеводневі ланцюги з більш ніж десятьма атомами Карбону.<br> Усі ПАР сприяють швидкому змочуванню водою забруднених поверхонь, відокремленню від них часточок бруду і переходу їх у розчин.<br> Використання мила має певні недоліки. Луг, який утворюється під час гідролізу, роз’їдає тканини, руйнує барвники. Мило втрачає свої властивості у твердій воді, бо йони Кальцію і Магнію, що містяться в ній, утворюють з аніонами жирних кислот малорозчинні солі:<br><br>'''Синтетичні мийні засоби'''.<br>Нині мила все більше витісняються синтетичними мийними засобами (скорочено - СМЗ), або детергентами, які позбавлені вищезгаданих недоліків. Основу СМЗ становлять поверхнево-активні речовини; у них є також різні добавки вибілювачі (хімічні, оптичні), ароматизатори, пом’якшувачі води, антистатики, дезінфікуючі речовини тощо. СМЗ здебільшого містять кілька поверхнево-активних речовин, які за властивостями доповнюють одна одну. Вміст ПАР різних типів у цих засобах сягає в середньому 35% за масою.
| + | Широкого застосування набули солі жирних кислот – мила. Натрієві солі є твердими речовинами, а <br>калієві – рідкими. Їхні аніони містять від 10 до 20 атомів Карбону. (Якщо атомів Карбону в аніоні солі <br>менше 10, то сполука не виявляє мийної дії, а якщо більше 20, то сіль практично нерозчинна в воді.)<br> |
| | + | |
| | + | Мило виробляли вже із середніх віків. Традиційний процес миловаріння полягає в нагріванні жирів із лугом <br>до утворення однорідної тягучої [[Тиск_і_сила_тиску._Одиниці_тиску._Тиск_рідин_і_газів._Манометри._Закон_Паскаля._Сполучені_посудини._Насоси.|рідини]]. При добавлянні до неї насиченого розчину кухонної солі розчинність мила зменшується, воно виділяється з розчину і спливає на поверхню. Цей процес називається висолюванням. Мило збирають і заповнюють ним форми, де воно твердне.<br> |
| | + | |
| | + | Інший спосіб виготовлення мила полягає в дії лугу або соди на жирні кислоти: |
| | + | |
| | + | <br>[[Image:Salt.jpg]]<br> |
| | + | |
| | + | Мийна дія мила полягає у відокремленні частинок бруду, наприклад від поверхні тканини, й утворенні <br>емульсії чи суспензії. Розглянемо, як це відбувається.<br> |
| | + | |
| | + | Потрапляючи у воду, мило розчиняється і зазнає неповного гідролізу: |
| | + | |
| | + | <br>[[Image:Third salt.jpg|400px|Гідроліз]]<br> |
| | + | |
| | + | Аніон карбонової кислоти складається із двох частин – полярної (-СООН<sup>-</sup>) і неполярної (наприклад, С<sub>17</sub>Н<sub>35</sub>-).<br> |
| | + | |
| | + | Неполярна (гідрофобна) частина аніона контактує із жировою складовою забруднення, а полярна <br>(гідрофільна) залишається у воді, сполучаючись з її молекулами водневими зв’язками (як показано на <br>малюнку нижче). Луг сприяє відокремленню частинок жирових забруднень від шкіри або тканини та їх <br>подрібненню, а аніони [[Застосування_сульфатної_кислоти_і_сульфатів._Конспект_уроку|кислоти]] – утворенню піни, в якій ці часточки утримуються. |
| | + | |
| | + | <br>[[Image:67-66.jpg|400px|Водний розчин мила]]<br> |
| | + | |
| | + | Мила належать до поверхнево-активних речовин(скорочено - ПАР). Це група органічних сполук, які містять полярні(гідрофільні) групи атомів різного складу і неполярні (гідрофобні) вуглеводневі ланцюги з більш ніж десятьма атомами [[Колообіг_Оксигену,_Нітрогену,_Карбону_в_природі|Карбон]]у.<br> |
| | + | |
| | + | Усі ПАР сприяють швидкому змочуванню водою забруднених поверхонь, відокремленню від них часточок бруду і переходу їх у розчин.<br> |
| | + | |
| | + | Використання мила має певні недоліки. Луг, який утворюється під час гідролізу, роз’їдає тканини, руйнує барвники. Мило втрачає свої властивості у твердій воді, бо йони Кальцію і Магнію, що містяться в ній, утворюють з аніонами жирних кислот малорозчинні солі: |
| | + | |
| | + | <br>[[Image:Last.jpg|400px|Мило втрачає свої властивості]] |
| | + | |
| | + | '''Синтетичні мийні засоби'''.<br>Нині мила все більше витісняються синтетичними мийними засобами (скорочено - СМЗ), або детергентами, які позбавлені вищезгаданих недоліків. Основу СМЗ становлять поверхнево-активні речовини; у них є також різні добавки вибілювачі (хімічні, оптичні), ароматизатори, пом’якшувачі води, антистатики, дезінфікуючі речовини тощо. СМЗ здебільшого містять кілька поверхнево-активних речовин, які за властивостями доповнюють одна одну. Вміст ПАР різних типів у цих засобах сягає в середньому 35% за масою. <br> |
| | + | |
| | + | |
| | + | |
| | + | ''П.П. Попель, Л.С. Крикля, І.О. Савченко, "Хімія. [[11_клас_уроки|11 клас]]. Підручник для загальноосвітніх навчальних закладів."'' |
| | + | |
| | + | <br> |
| | + | |
| | + | '''<u>Зміст уроку</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект уроку і опорний каркас |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентація уроку |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративні методи та інтерактивні технології |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] закриті вправи (тільки для використання вчителями) |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] оцінювання |
| | + | |
| | + | '''<u>Практика</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачі та вправи,самоперевірка |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикуми, лабораторні, кейси |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рівень складності задач: звичайний, високий, олімпійський |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашнє завдання |
| | + | |
| | + | '''<u>Ілюстрації</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] реферати |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фішки для допитливих |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] гумор, притчі, приколи, приказки, кросворди, цитати |
| | + | |
| | + | '''<u>Доповнення</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] зовнішнє незалежне тестування (ЗНТ) |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] підручники основні і допоміжні |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] тематичні свята, девізи |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статті |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] національні особливості |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словник термінів |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] інше |
| | + | |
| | + | '''<u>Тільки для вчителів</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/Idealny_urok.html ідеальні уроки] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарний план на рік |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методичні рекомендації |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] програми |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/forum/ обговорення] |
| | | | |
| | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. | | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. |
| | | | |
| | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. | | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. |
Текущая версия на 13:51, 7 ноября 2012
Гіпермаркет Знань>>Хімія>>Хімія 11 клас>>Органічні сполуки в побуті. Поняття про побутові хімікати. Загальні правила поводження з побутовими хімікатами. Мило, його склад, мийна дія. Синтетичні мийні засоби. Захист навколишнього середовища від забруднення синтетичними мийними засобами. Органічні розчинники, їх застосування. Попередження забруднення середовища при використанні органічних речовин у побуті
Вищі кислоти – це карбонові кислоти, молекули яких містять 10 і більше атомів Карбону. Серед них найважливішими є насичені кислоти – пальмітинова С15Н31СООН і стеаринова С17Н35СООН, а також ненасичена олеїнова С17Н33СООН. Ці кислоти раніше добували тільки з рослинних і тваринних жирів, тому їх ще називають жирними кислотами.
Пальмітинова і стеаринова кислоти – тверді речовини, а олеїнова – рідина. Сполуки практично не розчиняються у воді.
Хімічні властивості вищих карбонових кислот, як і нижчих кислот, зумовлені насамперед наявністю
функціональної групи – СООН. Вищі карбонові кислоти дуже слабкі; вони реагують з лугами й спиртами.
Олеїнова кислота є ненасиченою сполукою і тому здатна вступати реакції приєднання з галогенами, галогеноводнями тощо. Реагуючи з воднем, вона перетворюється на стеаринову кислоту:
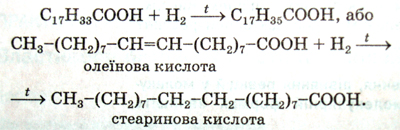
Крім того, олеїнова кислота може окислюватися калій перманганатом та іншими окисниками.
Вищі карбонові кислоти добувають гідролізом природних жирів, а також окисненням високомолекулярних
вуглеводнів нафти.
Мила.
Широкого застосування набули солі жирних кислот – мила. Натрієві солі є твердими речовинами, а
калієві – рідкими. Їхні аніони містять від 10 до 20 атомів Карбону. (Якщо атомів Карбону в аніоні солі
менше 10, то сполука не виявляє мийної дії, а якщо більше 20, то сіль практично нерозчинна в воді.)
Мило виробляли вже із середніх віків. Традиційний процес миловаріння полягає в нагріванні жирів із лугом
до утворення однорідної тягучої рідини. При добавлянні до неї насиченого розчину кухонної солі розчинність мила зменшується, воно виділяється з розчину і спливає на поверхню. Цей процес називається висолюванням. Мило збирають і заповнюють ним форми, де воно твердне.
Інший спосіб виготовлення мила полягає в дії лугу або соди на жирні кислоти:
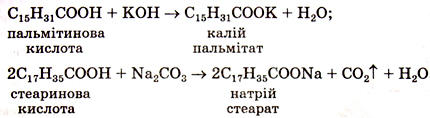
Мийна дія мила полягає у відокремленні частинок бруду, наприклад від поверхні тканини, й утворенні
емульсії чи суспензії. Розглянемо, як це відбувається.
Потрапляючи у воду, мило розчиняється і зазнає неповного гідролізу:
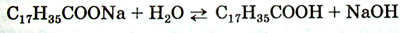
Аніон карбонової кислоти складається із двох частин – полярної (-СООН-) і неполярної (наприклад, С17Н35-).
Неполярна (гідрофобна) частина аніона контактує із жировою складовою забруднення, а полярна
(гідрофільна) залишається у воді, сполучаючись з її молекулами водневими зв’язками (як показано на
малюнку нижче). Луг сприяє відокремленню частинок жирових забруднень від шкіри або тканини та їх
подрібненню, а аніони кислоти – утворенню піни, в якій ці часточки утримуються.
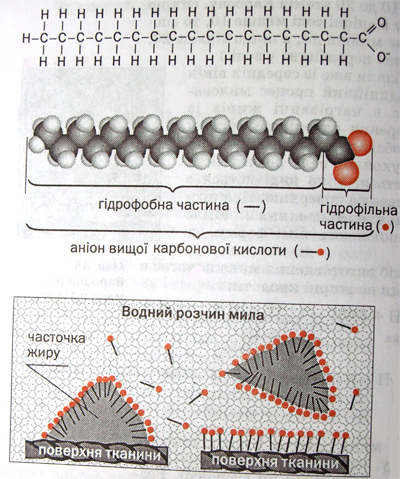
Мила належать до поверхнево-активних речовин(скорочено - ПАР). Це група органічних сполук, які містять полярні(гідрофільні) групи атомів різного складу і неполярні (гідрофобні) вуглеводневі ланцюги з більш ніж десятьма атомами Карбону.
Усі ПАР сприяють швидкому змочуванню водою забруднених поверхонь, відокремленню від них часточок бруду і переходу їх у розчин.
Використання мила має певні недоліки. Луг, який утворюється під час гідролізу, роз’їдає тканини, руйнує барвники. Мило втрачає свої властивості у твердій воді, бо йони Кальцію і Магнію, що містяться в ній, утворюють з аніонами жирних кислот малорозчинні солі:
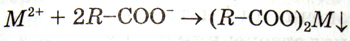
Синтетичні мийні засоби.
Нині мила все більше витісняються синтетичними мийними засобами (скорочено - СМЗ), або детергентами, які позбавлені вищезгаданих недоліків. Основу СМЗ становлять поверхнево-активні речовини; у них є також різні добавки вибілювачі (хімічні, оптичні), ароматизатори, пом’якшувачі води, антистатики, дезінфікуючі речовини тощо. СМЗ здебільшого містять кілька поверхнево-активних речовин, які за властивостями доповнюють одна одну. Вміст ПАР різних типів у цих засобах сягає в середньому 35% за масою.
П.П. Попель, Л.С. Крикля, І.О. Савченко, "Хімія. 11 клас. Підручник для загальноосвітніх навчальних закладів."
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|