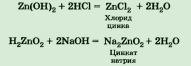|
|
|
| Строка 1: |
Строка 1: |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева, Характеристика химического элемента, на основании его положения в Периодической системе Д. И. Менделеева</metakeywords>''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева, Характеристика химического элемента, на основании его положения в Периодической системе Д. И. Менделеева</metakeywords>''' |
| | | | |
| - | <br>Общая характеристика химических элементов<br><br>Как и литературным героям, химическим элементам — «героям» химических процессов можно давать характеристику. Только если для первых эту характеристику дают на основании литературного произведения, то для вторых в качестве первоисточника используют Периодическую систему Д. И. Менделеева. И в первом, и во втором случае необходим план.<br><br>Характеризуя химический элемент, будем придерживаться <u>следующего плана:</u><br><br>1. Положение элемента в Периодической системе и строение его атомов.<br><br>2. Характер простого вещества (металл, неметалл, переходный металл).<br><br>3. Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по подгруппе элементами.<br><br>4. Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по периоду элементами.<br><br>5. Состав высшего оксида, его характер (основный, кислотный, амфотерный).<br><br>6. Состав высшего гидроксида, его характер (кислота, основание, амфотерный гидроксид).<br><br>7. Состав летучего водородного соединения (для неметаллов).<br><br>В приведенном плане для вас незнакомыми являются следующие химические понятия: переходные металлы, амфотерные оксиды, гидроксиды. Их смысл будет раскрыт в следующем параграфе. Пока же рассмотрим характеристику какого-либо металла и неметалла.<br> | + | <br>Общая характеристика химических элементов<br><br>Как и литературным героям, [[Периодическая_система_химических_элементов_Д._И._Менделеева._Полные_уроки|химическим элементам]] — «героям» химических процессов можно давать характеристику. Только если для первых эту характеристику дают на основании литературного произведения, то для вторых в качестве первоисточника используют Периодическую систему Д. И. [[Периодическая_система_химических_элементов_Д._И._Менделеева._Знаки_химических_элементов|Менделеева]]. И в первом, и во втором случае необходим план.<br><br>Характеризуя химический элемент, будем придерживаться <u>следующего плана:</u><br><br>1. Положение элемента в Периодической системе и строение его атомов.<br><br>2. Характер простого вещества ([[Пропильной_металл|металл]], неметалл, переходный металл).<br><br>3. Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по подгруппе элементами.<br><br>4. Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по периоду элементами.<br><br>5. Состав высшего [[Оксиды,_их_классификация_и_свойства|оксида]], его характер (основный, кислотный, амфотерный).<br><br>6. Состав высшего гидроксида, его характер (кислота, основание, амфотерный гидроксид).<br><br>7. Состав летучего водородного соединения (для неметаллов).<br><br>В приведенном плане для вас незнакомыми являются следующие химические понятия: переходные металлы, амфотерные оксиды, гидроксиды. Их смысл будет раскрыт в следующем параграфе. Пока же рассмотрим характеристику какого-либо металла и неметалла.<br> |
| | | | |
| - | Таким образом, гидроксиду цинка присуще амфотерное поведение: он может реагировать с кислотами как основание и со щелочами как кислота. Соответственно его формулу можно представить двояко:<br><br>Zn(ОН)2 = H2ZnH2<br><br>Основание Кислота<br><br>Тогда уравнения реакций гидроксида цинка с кислотой и со щелочью можно записать так:<br><br>[[Image:him9-1.jpg]]<br><br><br><br>В обоих случаях образуется растворимая соль.<br><br>Аналогично гидроксиду и оксид цинка проявляет амфотдо-ный характер — образует соли при взаимодействии как с кислотами, так и с основаниями.<br><br>В первой реакции оксид цинка ведет себя как основный оксид, а во второй реакции выступает в роли кислотного оксида — образует соль, в которой цинк входит в состав кислотного остатка.<br><br><u>''Амфотерными''</u> являются оксиды и гидроксиды многих элементов, например бериллия, алюминия, свинца, хрома.<br><br>Если химический элемент-металл проявляет несколько степеней окисления, то его оксид и гидроксид с низшей степенью окисления будут проявлять основные свойства, с высшей — кислотные, а с промежуточной — амфотерные. Например, для хрома<br>[[Image:him09-2.jpg]]<br><br>Амфотерные оксиды и гидроксиды образуют чаще всего те элементы, которые составляют побочные подгруппы Периодической системы (таблицы) Д. И. Менделеева. Эти элементы называют переходными элементами или переходными металлами. | + | Таким образом, гидроксиду цинка присуще амфотерное поведение: он может реагировать с [[Кислоты_органические_и_неорганические|кислотами]] как основание и со щелочами как кислота. Соответственно его формулу можно представить двояко:<br><br>Zn(ОН)2 = H2ZnH2<br><br>Основание Кислота<br><br>Тогда уравнения реакций гидроксида цинка с кислотой и со щелочью можно записать так:<br><br>[[Image:Him9-1.jpg|химия 9 класс]]<br><br><br><br>В обоих случаях образуется растворимая [[Соли_(Химия_8_класс)|соль]].<br><br>Аналогично гидроксиду и оксид цинка проявляет амфотдо-ный характер — образует соли при взаимодействии как с кислотами, так и с основаниями.<br><br>В первой реакции оксид цинка ведет себя как основный оксид, а во второй реакции выступает в роли кислотного оксида — образует соль, в которой цинк входит в состав кислотного остатка.<br><br><u>''Амфотерными''</u> являются оксиды и гидроксиды многих элементов, например бериллия, алюминия, свинца, хрома.<br><br>Если химический элемент-металл проявляет несколько степеней окисления, то его оксид и гидроксид с низшей степенью окисления будут проявлять основные свойства, с высшей — кислотные, а с промежуточной — амфотерные. Например, для хрома<br>[[Image:Him09-2.jpg|химия 9 класс]]<br><br>Амфотерные оксиды и гидроксиды образуют чаще всего те элементы, которые составляют побочные подгруппы Периодической системы (таблицы) Д. И. Менделеева. Эти элементы называют переходными элементами или переходными металлами. |
| | | | |
| | <br>1. Амфотерные оксиды и гидроксиды. | | <br>1. Амфотерные оксиды и гидроксиды. |
| Строка 9: |
Строка 9: |
| | 2. Переходные элементы, или переходные металлы. | | 2. Переходные элементы, или переходные металлы. |
| | | | |
| - | 3. Зависимость химических свойств оксидов и гидроксидов элементов побочных подгрупп таблицы Д. И. Менделеева от степеней окисления их атомов.<br><br>Почему для получения амфотерного гидроксида из раствора соли переходного элемента раствор щелочи к ней приливают по каплям?<br><br>Запишите уравнения реакций для следующих превращений:<br><br>Бериллий-> Оксид бериллия<br><br>Сульфат бериллия Бериллат калия Нитрат бериллия<br><br>Гидроксид бериллия<br><br>Первую реакцию рассмотрите с позиций окисления-восстановления.<br><br>Приведите по два молекулярных уравнения реакций, соответствующих сокращенным ионным уравнениям:<br><br>а) Ве(ОН)2 + 2Н+ -> Ве2+ + 2Н2О<br><br>б) Ве(ОН)2 + 20Н+ -> ВеО + 2Н2О<br><br>Докажите, что амфотерность подтверждает относительный характер деления элементов на металлы и неметаллы.<br><br> <sub>конспект [[Химия|урока химии]], задачи по [[Химия_9_класс|химии 9 класса]], учебники по [[Гипермаркет_знаний_-_первый_в_мире!|всем предметам]]</sub> | + | 3. Зависимость химических свойств оксидов и гидроксидов элементов побочных подгрупп таблицы Д. И. Менделеева от степеней окисления их [[Основные_сведения_о_строении_атомов._Полные_уроки|атомов]].<br><br>Почему для получения амфотерного гидроксида из раствора соли переходного элемента раствор щелочи к ней приливают по каплям?<br><br>Запишите уравнения реакций для следующих превращений:<br><br>Бериллий-> Оксид бериллия<br><br>Сульфат бериллия Бериллат калия Нитрат бериллия<br><br>Гидроксид бериллия<br><br>Первую реакцию рассмотрите с позиций окисления-восстановления.<br><br>Приведите по два молекулярных уравнения реакций, соответствующих сокращенным ионным уравнениям:<br><br>а) Ве(ОН)2 + 2Н+ -> Ве2+ + 2Н2О<br><br>б) Ве(ОН)2 + 20Н+ -> ВеО + 2Н2О<br><br>Докажите, что амфотерность подтверждает относительный характер деления элементов на металлы и неметаллы.<br><br> <sub>конспект [[Химия|урока химии]], задачи по [[Химия 9 класс|химии 9 класса]], учебники по [[Гипермаркет знаний - первый в мире!|всем предметам]]</sub> |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Текущая версия на 08:35, 1 июля 2012
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева
Общая характеристика химических элементов
Как и литературным героям, химическим элементам — «героям» химических процессов можно давать характеристику. Только если для первых эту характеристику дают на основании литературного произведения, то для вторых в качестве первоисточника используют Периодическую систему Д. И. Менделеева. И в первом, и во втором случае необходим план.
Характеризуя химический элемент, будем придерживаться следующего плана:
1. Положение элемента в Периодической системе и строение его атомов.
2. Характер простого вещества (металл, неметалл, переходный металл).
3. Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по подгруппе элементами.
4. Сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по периоду элементами.
5. Состав высшего оксида, его характер (основный, кислотный, амфотерный).
6. Состав высшего гидроксида, его характер (кислота, основание, амфотерный гидроксид).
7. Состав летучего водородного соединения (для неметаллов).
В приведенном плане для вас незнакомыми являются следующие химические понятия: переходные металлы, амфотерные оксиды, гидроксиды. Их смысл будет раскрыт в следующем параграфе. Пока же рассмотрим характеристику какого-либо металла и неметалла.
Таким образом, гидроксиду цинка присуще амфотерное поведение: он может реагировать с кислотами как основание и со щелочами как кислота. Соответственно его формулу можно представить двояко:
Zn(ОН)2 = H2ZnH2
Основание Кислота
Тогда уравнения реакций гидроксида цинка с кислотой и со щелочью можно записать так:
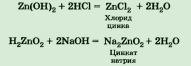
В обоих случаях образуется растворимая соль.
Аналогично гидроксиду и оксид цинка проявляет амфотдо-ный характер — образует соли при взаимодействии как с кислотами, так и с основаниями.
В первой реакции оксид цинка ведет себя как основный оксид, а во второй реакции выступает в роли кислотного оксида — образует соль, в которой цинк входит в состав кислотного остатка.
Амфотерными являются оксиды и гидроксиды многих элементов, например бериллия, алюминия, свинца, хрома.
Если химический элемент-металл проявляет несколько степеней окисления, то его оксид и гидроксид с низшей степенью окисления будут проявлять основные свойства, с высшей — кислотные, а с промежуточной — амфотерные. Например, для хрома
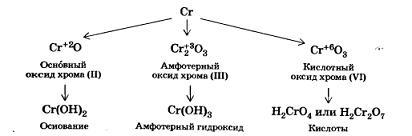
Амфотерные оксиды и гидроксиды образуют чаще всего те элементы, которые составляют побочные подгруппы Периодической системы (таблицы) Д. И. Менделеева. Эти элементы называют переходными элементами или переходными металлами.
1. Амфотерные оксиды и гидроксиды.
2. Переходные элементы, или переходные металлы.
3. Зависимость химических свойств оксидов и гидроксидов элементов побочных подгрупп таблицы Д. И. Менделеева от степеней окисления их атомов.
Почему для получения амфотерного гидроксида из раствора соли переходного элемента раствор щелочи к ней приливают по каплям?
Запишите уравнения реакций для следующих превращений:
Бериллий-> Оксид бериллия
Сульфат бериллия Бериллат калия Нитрат бериллия
Гидроксид бериллия
Первую реакцию рассмотрите с позиций окисления-восстановления.
Приведите по два молекулярных уравнения реакций, соответствующих сокращенным ионным уравнениям:
а) Ве(ОН)2 + 2Н+ -> Ве2+ + 2Н2О
б) Ве(ОН)2 + 20Н+ -> ВеО + 2Н2О
Докажите, что амфотерность подтверждает относительный характер деления элементов на металлы и неметаллы.
конспект урока химии, задачи по химии 9 класса, учебники по всем предметам
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|