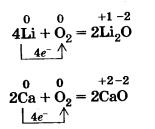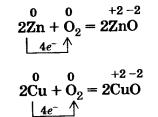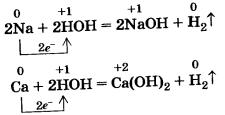|
|
|
| Строка 1: |
Строка 1: |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Химические свойства металлов<metakeywords>химия, 9 класс, класс, урок химии, на тему, урок на тему, урок для 9 класса, Химические свойства металлов</metakeywords>''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Химические свойства металлов<metakeywords>химия, 9 класс, класс, урок химии, на тему, урок на тему, урок для 9 класса, Химические свойства металлов</metakeywords>''' |
| | | | |
| - | В химических реакциях металлы проявляют только восстановительные свойства, т. е. их атомы отдают электроны, образуя в результате положительные ионы. Окислителями при этом могут выступать неметаллы (кислород, галогены, сера и др.), катионы водорода Н+ и катионы других металлов.<br><br>С кислородом воздуха легко взаимодействуют щелочные и щелочноземельные металлы:<br> | + | В химических реакциях металлы проявляют только восстановительные свойства, т. е. их [[Основные_сведения_о_строении_атомов._Полные_уроки|атомы]] отдают электроны, образуя в результате положительные ионы. Окислителями при этом могут выступать неметаллы (кислород, галогены, сера и др.), катионы водорода Н+ и катионы других металлов.<br><br>С кислородом воздуха легко взаимодействуют щелочные и щелочноземельные металлы:<br> |
| | | | |
| - | [[Image:Ahim09-9.jpg]] | + | [[Image:Ahim09-9.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | Железо, цинк, медь и другие менее активные металлы энергично окисляются кислородом только при нагревании:<br>[[Image:Ahim09-10.jpg]] | + | Железо, цинк, медь и другие менее активные [[Металлы_(Химия_11_класс)|металлы]] энергично окисляются кислородом только при нагревании:<br>[[Image:Ahim09-10.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | Золото и платиновые металлы не окисляются кислородом воздуха ни при каких условиях.<br><br>Как вы уже знаете, металлы образуют с неметаллами бинарные соединения — оксиды, хлориды, сульфиды, фосфиды и т. д., например:<br> | + | Золото и платиновые металлы не окисляются [[Кислород|кислородом]] воздуха ни при каких условиях.<br><br>Как вы уже знаете, металлы образуют с неметаллами бинарные соединения — оксиды, хлориды, сульфиды, фосфиды и т. д., например:<br> |
| | | | |
| - | [[Image:Ahim09-11.jpg]] | + | [[Image:Ahim09-11.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | Щелочные и щелочноземельные металлы легко реагируют с водой, восстанавливая катионы водорода до свободного водорода, и образуют при этом растворимые гидроксиды — щелочи:<br><br>[[Image:Ahim09-12.jpg]] | + | Щелочные и щелочноземельные металлы легко реагируют с водой, восстанавливая катионы водорода до свободного водорода, и образуют при этом растворимые гидроксиды — щелочи:<br><br>[[Image:Ahim09-12.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | Менее активные металлы, например железо, взаимодействуют с водой только в раскаленном виде:<br>[[Image:Ahim09-13.jpg]] | + | Менее активные металлы, например железо, взаимодействуют с водой только в раскаленном виде:<br>[[Image:Ahim09-13.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | При этом, как и при горении железа, получается оксид состава Fе3O4, который представляет собой смесь двух оксидов FеО • Fе2O3. Его называют также железной окалиной.<br><br>По восстановительной способности, как вы уже знаете, металлы располагаются в ряд, который называют электрохимическим рядом напряжений:<br><br>К, Са, Nа, Мg, Аl, Zn, Fе, Ni, Sn, РЬ, (Н2), Сu, Нg, Аg, Аu<br><br>В этот ряд помещен и водород, который, как и металлы, способен отдавать электроны, образуя при этом положительно заряженные ионы Н+.<br><br>Как вы, очевидно, помните из курса химии 8 класса, из положения металлов в ряду напряжений вытекают два правила, характеризующие химические свойства металлов. Повторим их.<br> | + | При этом, как и при горении железа, получается оксид состава Fе3O4, который представляет собой смесь двух оксидов FеО • Fе2O3. Его называют также железной окалиной.<br><br>По восстановительной способности, как вы уже знаете, металлы располагаются в ряд, который называют электрохимическим рядом напряжений:<br><br>К, Са, Nа, Мg, Аl, Zn, Fе, Ni, Sn, РЬ, (Н2), Сu, Нg, Аg, Аu<br><br>В этот ряд помещен и водород, который, как и металлы, способен отдавать электроны, образуя при этом положительно заряженные ионы Н+.<br><br>Как вы, очевидно, помните из курса [[Химия_8_класс|химии 8 класса]], из положения металлов в ряду напряжений вытекают два правила, характеризующие химические свойства металлов. Повторим их.<br> |
| | | | |
| - | 1. Металлы, стоящие в ряду напряжений левее водорода, вытесняют его из растворов кислот, а стоящие правее — не вытесняют водород из растворов кислот:<br>[[Image:Ahim09-14.jpg]] | + | 1. Металлы, стоящие в ряду напряжений левее водорода, вытесняют его из растворов кислот, а стоящие правее — не вытесняют водород из растворов кислот:<br>[[Image:Ahim09-14.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | А вот медь не реагирует с хлороводородной кислотой. Напомним, что это правило имеет ряд поправок:<br><br>а) правило соблюдается, если в реакции металла с кислотой образуется растворимая соль;<br><br>б) концентрированная серная кислота и азотная кислота любой концентрации реагирует с металлами по-особому, при этом водород не образуется;<br><br>в) на щелочные металлы правило не распространяется, так как они легко взаимодействуют с водой (а указанное правило относится к реакциям водных растворов кислот с металлами).<br><br>2. Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее, например:<br>[[Image:Ahim09-15.jpg]] | + | А вот медь не реагирует с хлороводородной кислотой. Напомним, что это правило имеет ряд поправок:<br><br>а) правило соблюдается, если в реакции металла с кислотой образуется растворимая соль;<br><br>б) концентрированная серная кислота и азотная кислота любой концентрации реагирует с металлами по-особому, при этом водород не образуется;<br><br>в) на щелочные металлы правило не распространяется, так как они легко взаимодействуют с водой (а указанное правило относится к реакциям водных растворов кислот с металлами).<br><br>2. Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее, например:<br>[[Image:Ahim09-15.jpg|химия 9 класс]] |
| | | | |
| | <br> | | <br> |
| | | | |
| - | Это правило также имеет поправки, аналогичные таковым к первому правилу, а именно — правило соблюдается при условии образования растворимой соли; правило не распространяется на щелочные металлы.<br><br>1. Восстановительные свойства металлов. | + | Это правило также имеет поправки, аналогичные таковым к первому правилу, а именно — правило соблюдается при условии образования растворимой [[Соли._Полные_уроки|соли]]; правило не распространяется на щелочные металлы.<br><br>1. Восстановительные свойства металлов. |
| | | | |
| | 2. Взаимодействие металлов с кислородом и другими неметаллами. | | 2. Взаимодействие металлов с кислородом и другими неметаллами. |
| Строка 43: |
Строка 43: |
| | 4. Правила применения электрохимического ряда напряжений при определении возможности взаимодействия металлов с растворами кислот и солей. | | 4. Правила применения электрохимического ряда напряжений при определении возможности взаимодействия металлов с растворами кислот и солей. |
| | | | |
| - | 5. Поправки к правилам применения электрохимического ряда напряжений.<br><br>Определите число электронов, которое отдают три атома железа молекуле воды в реакции образования железной окалины. | + | 5. Поправки к правилам применения электрохимического ряда напряжений.<br><br>Определите число электронов, которое отдают три атома железа молекуле [[Круговорот_воды_в_природе._Водные_ресурсы_Земли|воды]] в реакции образования железной окалины. |
| | | | |
| - | Какой объем воздуха потребуется для сжигания 36 г магния? (Напоминаем, что объемная доля кислорода в воздухе равна 0,21.)<br><br>Какой объем водорода может быть получен при растворении в воде 120 мг кальция, если выход газа составляет 80% от теоретически возможного?<br><br>Почему щелочные и щелочноземельные металлы хранят под керосином? Почему литий, в отличие от натрия и калия, хранят в вазелине?<br><br>Определите коэффициенты в следующем уравнении реакции, используя метод электронного баланса:<br>[[Image:ahim09-16.jpg]] | + | Какой объем воздуха потребуется для сжигания 36 г магния? (Напоминаем, что объемная доля кислорода в воздухе равна 0,21.)<br><br>Какой объем водорода может быть получен при растворении в воде 120 мг кальция, если выход газа составляет 80% от теоретически возможного?<br><br>Почему щелочные и щелочноземельные металлы хранят под керосином? Почему литий, в отличие от натрия и калия, хранят в вазелине?<br><br>Определите коэффициенты в следующем уравнении реакции, используя метод электронного баланса:<br>[[Image:Ahim09-16.jpg|химия 9 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Какой ион проявляет в этой реакции окислительные свойства?<br><br>Можно ли получить водород при взаимодействии свинца с раствором серной кислоты?<br><br>Определите коэффициенты в следующем уравнении методом электронного баланса:<br>Zn+ H2SO4(конц) -> ZnSO4 + H2S + H2O |
| | | | |
| - | Какой ион проявляет в этой реакции окислительные свойства?<br><br>Можно ли получить водород при взаимодействии свинца с раствором серной кислоты?<br><br>Определите коэффициенты в следующем уравнении методом электронного баланса:<br>Zn+ H2SO4(конц) -> ZnSO4 + H2S + H2O
| + | Какое вещество проявляет в этой реакции восстановительные свойства? |
| - | | + | |
| - | Какое вещество проявляет в этой реакции восстановительные свойства? | + | |
| | | | |
| | <br> <sub>аудио для [[Химия|урока химии]], анекжоты для урока [[Химия 9 класс|химии в 9 классе]], [[Гипермаркет знаний - первый в мире!|учебные пособия]]</sub> | | <br> <sub>аудио для [[Химия|урока химии]], анекжоты для урока [[Химия 9 класс|химии в 9 классе]], [[Гипермаркет знаний - первый в мире!|учебные пособия]]</sub> |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Текущая версия на 09:14, 1 июля 2012
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Химические свойства металлов
В химических реакциях металлы проявляют только восстановительные свойства, т. е. их атомы отдают электроны, образуя в результате положительные ионы. Окислителями при этом могут выступать неметаллы (кислород, галогены, сера и др.), катионы водорода Н+ и катионы других металлов.
С кислородом воздуха легко взаимодействуют щелочные и щелочноземельные металлы:
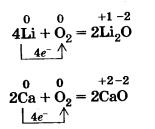
Железо, цинк, медь и другие менее активные металлы энергично окисляются кислородом только при нагревании:
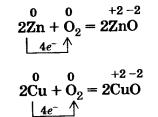
Золото и платиновые металлы не окисляются кислородом воздуха ни при каких условиях.
Как вы уже знаете, металлы образуют с неметаллами бинарные соединения — оксиды, хлориды, сульфиды, фосфиды и т. д., например:
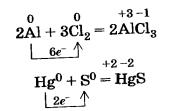
Щелочные и щелочноземельные металлы легко реагируют с водой, восстанавливая катионы водорода до свободного водорода, и образуют при этом растворимые гидроксиды — щелочи:
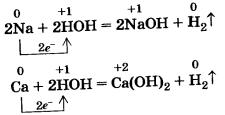
Менее активные металлы, например железо, взаимодействуют с водой только в раскаленном виде:
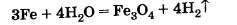
При этом, как и при горении железа, получается оксид состава Fе3O4, который представляет собой смесь двух оксидов FеО • Fе2O3. Его называют также железной окалиной.
По восстановительной способности, как вы уже знаете, металлы располагаются в ряд, который называют электрохимическим рядом напряжений:
К, Са, Nа, Мg, Аl, Zn, Fе, Ni, Sn, РЬ, (Н2), Сu, Нg, Аg, Аu
В этот ряд помещен и водород, который, как и металлы, способен отдавать электроны, образуя при этом положительно заряженные ионы Н+.
Как вы, очевидно, помните из курса химии 8 класса, из положения металлов в ряду напряжений вытекают два правила, характеризующие химические свойства металлов. Повторим их.
1. Металлы, стоящие в ряду напряжений левее водорода, вытесняют его из растворов кислот, а стоящие правее — не вытесняют водород из растворов кислот:
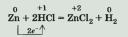
А вот медь не реагирует с хлороводородной кислотой. Напомним, что это правило имеет ряд поправок:
а) правило соблюдается, если в реакции металла с кислотой образуется растворимая соль;
б) концентрированная серная кислота и азотная кислота любой концентрации реагирует с металлами по-особому, при этом водород не образуется;
в) на щелочные металлы правило не распространяется, так как они легко взаимодействуют с водой (а указанное правило относится к реакциям водных растворов кислот с металлами).
2. Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее, например:
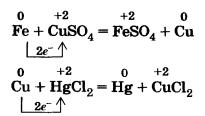
Это правило также имеет поправки, аналогичные таковым к первому правилу, а именно — правило соблюдается при условии образования растворимой соли; правило не распространяется на щелочные металлы.
1. Восстановительные свойства металлов.
2. Взаимодействие металлов с кислородом и другими неметаллами.
3. Электрохимический ряд напряжений.
4. Правила применения электрохимического ряда напряжений при определении возможности взаимодействия металлов с растворами кислот и солей.
5. Поправки к правилам применения электрохимического ряда напряжений.
Определите число электронов, которое отдают три атома железа молекуле воды в реакции образования железной окалины.
Какой объем воздуха потребуется для сжигания 36 г магния? (Напоминаем, что объемная доля кислорода в воздухе равна 0,21.)
Какой объем водорода может быть получен при растворении в воде 120 мг кальция, если выход газа составляет 80% от теоретически возможного?
Почему щелочные и щелочноземельные металлы хранят под керосином? Почему литий, в отличие от натрия и калия, хранят в вазелине?
Определите коэффициенты в следующем уравнении реакции, используя метод электронного баланса:
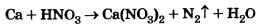
Какой ион проявляет в этой реакции окислительные свойства?
Можно ли получить водород при взаимодействии свинца с раствором серной кислоты?
Определите коэффициенты в следующем уравнении методом электронного баланса:
Zn+ H2SO4(конц) -> ZnSO4 + H2S + H2O
Какое вещество проявляет в этой реакции восстановительные свойства?
аудио для урока химии, анекжоты для урока химии в 9 классе, учебные пособия
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|