|
|
|
| Строка 1: |
Строка 1: |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Химические формулы. Относительная атомная и молекулярная массы<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Химические формулы, Относительная атомная и молекулярная массы</metakeywords>''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Химические формулы. Относительная атомная и молекулярная массы<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Химические формулы, Относительная атомная и молекулярная массы</metakeywords>''' |
| | | | |
| | + | <br> |
| | | | |
| | + | Состав простых и сложных веществ химики всего мира отражают очень красиво и лаконично в виде химических формул. [[Химические_формулы._Полные_уроки|Химические формулы]] — это аналоги слов, которые записываются с помощью букв — знаков химических элементов. |
| | | | |
| - | Состав простых и сложных веществ химики всего мира отражают очень красиво и лаконично в виде химических формул. Химические формулы — это аналоги слов, которые записываются с помощью букв — знаков химических элементов.
| + | <br>Выразим с помощью химических символов состав самого распространенного Вещества на Земле — воды. В молекулу воды входят два атома водорода и один атом кислорода. Теперь переведем это предложение в химическую формулу с помощью химических символов (водорода — Ни кислорода — О). Число атомов в формуле запишем с помощью индексов-цифр, стоящих справа внизу от химического символа (индекс 1 для кислорода не пишут): Н2Щ (читается «аш-два-о»). |
| | | | |
| - | <br>Выразим с помощью химических символов состав самого распространенного Вещества на Земле — воды. В молекулу воды входят два атома водорода и один атом кислорода. Теперь переведем это предложение в химическую формулу с помощью химических символов (водорода — Ни кислорода — О). Число атомов в формуле запишем с помощью индексов-цифр, стоящих справа внизу от химического символа (индекс 1 для кислорода не пишут): Н2Щ (читается «аш-два-о»). | + | <br>Формулы простых веществ водорода и [[Кислород|кислорода]], молекулы которых состоят из двух одинаковых атомов, записывают так: Н2 (читается «аш-два») и О2 (читается «о-два»). |
| | | | |
| - | <br>Формулы простых веществ водорода и кислорода, молекулы которых состоят из двух одинаковых атомов, записывают так: Н2 (читается «аш-два») и О2 (читается «о-два»). | + | <br>Чтобы отразить число молекул, пользуются коэффициентами, которые пишут перед химическими формулами, например запись 2СОг (читается •два-цэ-о-два») означает, что имеют в виду две молекулы углекислого газа, каждая из которых состоит из одного атома углерода и двух атомов кислорода.<br>Аналогично записывают коэффициенты, когда указывают число свободных атомов химического элемента. |
| | | | |
| - | <br>Чтобы отразить число молекул, пользуются коэффициентами, которые пишут перед химическими формулами, например запись 2СОг (читается •два-цэ-о-два») означает, что имеют в виду две молекулы углекислого газа, каждая из которых состоит из одного атома углерода и двух атомов кислорода.<br>Аналогично записывают коэффициенты, когда указывают число свободных атомов химического элемента.
| + | [[Image:Him8-4.jpg|формула]] |
| | | | |
| - | [[Image:him8-4.jpg]]
| + | <br>Размеры молекул, а тем более атомоя настолько малы, что их невозможно рассмотреть даже в лучшие оптические микроскопы, дающие увеличение в 5—6 тысяч раз. Их невозможно рассмотреть и в электронные микроскопы, дающие увеличение в 40 тысяч раз. Естественно, что ничтожно малому размеру молекул и атомов соответствуют и ничтожно малые их массы. |
| | | | |
| - | <br>Размеры молекул, а тем более атомоя настолько малы, что их невозможно рассмотреть даже в лучшие оптические микроскопы, дающие увеличение в 5—6 тысяч раз. Их невозможно рассмотреть и в электронные микроскопы, дающие увеличение в 40 тысяч раз. Естественно, что ничтожно малому размеру молекул и атомов соответствуют и ничтожно малые их массы. | + | <br>Давайте рассчитаем, во сколько раз масса атома кислорода больше массы атома водорода, самого легкого элемента:<br> [[Image:Him8-5.jpg|формула]] |
| | | | |
| - | <br>Давайте рассчитаем, во сколько раз масса атома кислорода больше массы атома водорода, самого легкого элемента:<br> [[Image:him8-5.jpg]] | + | <br>Аналогично, масса атома углерода больше массы атома водорода в 12 раз.<br> [[Image:Him8-6.jpg|формула]] |
| | | | |
| - | <br>Аналогично, масса атома углерода больше массы атома водорода в 12 раз.<br> [[Image:him8-6.jpg]] | + | <br>[[Масса_молекул._Количество_вещества|Масса молекулы]] воды больше массы атома водорода в 18 раз. Величину, которая показывает, во сколько раз масса атома данного химического элемента больше массы атома водорода, называют относительной атомной массой. |
| | | | |
| - | <br>Масса молекулы воды больше массы атома водорода в 18 раз. Величину, которая показывает, во сколько раз масса атома данного химического элемента больше массы атома водорода, называют относительной атомной массой.
| + | [[Image:Him8-7.jpg|молекулы]] |
| | | | |
| - | [[Image:him8-7.jpg]]
| + | <br> |
| | | | |
| | + | Ученые-[[Фізика_і_астрономія|физики]] и ученые-химики придерживаются мнения, что относительной атомной массой элемента нужно считать величину, показывающую, во сколько раз массв его атома больше 1/12 массы атома углерода. Относительную атомную массу обозначают Ar, где r — начальная буква английского слова rеlative, что означает "относительный". Например, |
| | | | |
| | + | [[Image:Him8-8.jpg|формула]] |
| | | | |
| - | Ученые-физики и ученые-химики придерживаются мнения, что относительной атомной массой элемента нужно считать величину, показывающую, во сколько раз массв его атома больше 1/12 массы атома углерода. Относительную атомную массу обозначают Ar, где r — начальная буква английского слова rеlative, что означает "относительный". Например,
| + | <br> |
| | | | |
| - | [[Image:him8-8.jpg]] | + | Значения относительных атомных масс указаны в таблице [[Периодическая_система_химических_элементов_Д._И._Менделеева._Полные_уроки|Менделеева]] под химическими знаками элементов. |
| | | | |
| | + | <br>Аналогично, относительную молекулярную массу вещества обозначают Mr, например Mr (Н20) = 18. <br>Аr и Мr — величины, которые не имеют единиц измерения. |
| | | | |
| | + | <br>Чтобы узнать относительную молекулярную массу вещества, не обязательно делить массу его молекулы на массу атома водорода. Нужно просто сложить относительные атомные массы элементов, образующих вещество, с учетом числа атомов, например:<br> [[Image:Him8-9.jpg|формула]] |
| | | | |
| - | Значения относительных атомных масс указаны в таблице Менделеева под химическими знаками элементов.
| + | <br>1. Химическая формула. 2. Индексы и коэффициенты. 3. Относительная атомная масса Аr. 4. Относительна молекулярная масса Mr<br> <br>Что называется относительной молекулярной массой? Почему Аr и Мr не имеют единиц измерения?<br><br>[[Image:Him8-10.jpg|формула]] |
| | | | |
| - | <br>Аналогично, относительную молекулярную массу вещества обозначают Mr, например Mr (Н20) = 18. <br>Аr и Мr — величины, которые не имеют единиц измерения.
| + | <br> <sub>задания [[Химия 8 класс|по химии]] для 8 класса, [[Химия|химия]] в таблицах, учебники [[Гипермаркет знаний - первый в мире!|по всем предметам]]</sub> |
| - | | + | |
| - | <br>Чтобы узнать относительную молекулярную массу вещества, не обязательно делить массу его молекулы на массу атома водорода. Нужно просто сложить относительные атомные массы элементов, образующих вещество, с учетом числа атомов, например:<br> [[Image:him8-9.jpg]]
| + | |
| - | | + | |
| - | <br>1. Химическая формула. 2. Индексы и коэффициенты. 3. Относительная атомная масса Аr. 4. Относительна молекулярная масса Mr<br> <br>Что называется относительной молекулярной массой? Почему Аr и Мr не имеют единиц измерения?<br><br>[[Image:him8-10.jpg]]
| + | |
| - | | + | |
| - | <br> <sub>задания [[Химия_8_класс|по химии]] для 8 класса, [[Химия|химия]] в таблицах, учебники [[Гипермаркет_знаний_-_первый_в_мире!|по всем предметам]]</sub> | + | |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Текущая версия на 12:18, 27 июня 2012
Гипермаркет знаний>>Химия>>Химия 8 класс>> Химия: Химические формулы. Относительная атомная и молекулярная массы
Состав простых и сложных веществ химики всего мира отражают очень красиво и лаконично в виде химических формул. Химические формулы — это аналоги слов, которые записываются с помощью букв — знаков химических элементов.
Выразим с помощью химических символов состав самого распространенного Вещества на Земле — воды. В молекулу воды входят два атома водорода и один атом кислорода. Теперь переведем это предложение в химическую формулу с помощью химических символов (водорода — Ни кислорода — О). Число атомов в формуле запишем с помощью индексов-цифр, стоящих справа внизу от химического символа (индекс 1 для кислорода не пишут): Н2Щ (читается «аш-два-о»).
Формулы простых веществ водорода и кислорода, молекулы которых состоят из двух одинаковых атомов, записывают так: Н2 (читается «аш-два») и О2 (читается «о-два»).
Чтобы отразить число молекул, пользуются коэффициентами, которые пишут перед химическими формулами, например запись 2СОг (читается •два-цэ-о-два») означает, что имеют в виду две молекулы углекислого газа, каждая из которых состоит из одного атома углерода и двух атомов кислорода.
Аналогично записывают коэффициенты, когда указывают число свободных атомов химического элемента.

Размеры молекул, а тем более атомоя настолько малы, что их невозможно рассмотреть даже в лучшие оптические микроскопы, дающие увеличение в 5—6 тысяч раз. Их невозможно рассмотреть и в электронные микроскопы, дающие увеличение в 40 тысяч раз. Естественно, что ничтожно малому размеру молекул и атомов соответствуют и ничтожно малые их массы.
Давайте рассчитаем, во сколько раз масса атома кислорода больше массы атома водорода, самого легкого элемента:
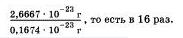
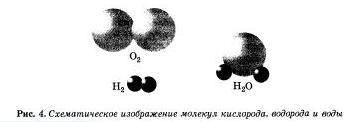
Аналогично, масса атома углерода больше массы атома водорода в 12 раз.

Масса молекулы воды больше массы атома водорода в 18 раз. Величину, которая показывает, во сколько раз масса атома данного химического элемента больше массы атома водорода, называют относительной атомной массой.
Ученые-физики и ученые-химики придерживаются мнения, что относительной атомной массой элемента нужно считать величину, показывающую, во сколько раз массв его атома больше 1/12 массы атома углерода. Относительную атомную массу обозначают Ar, где r — начальная буква английского слова rеlative, что означает "относительный". Например,
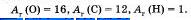
Значения относительных атомных масс указаны в таблице Менделеева под химическими знаками элементов.
Аналогично, относительную молекулярную массу вещества обозначают Mr, например Mr (Н20) = 18.
Аr и Мr — величины, которые не имеют единиц измерения.
Чтобы узнать относительную молекулярную массу вещества, не обязательно делить массу его молекулы на массу атома водорода. Нужно просто сложить относительные атомные массы элементов, образующих вещество, с учетом числа атомов, например:
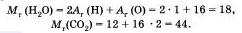
1. Химическая формула. 2. Индексы и коэффициенты. 3. Относительная атомная масса Аr. 4. Относительна молекулярная масса Mr
Что называется относительной молекулярной массой? Почему Аr и Мr не имеют единиц измерения?

задания по химии для 8 класса, химия в таблицах, учебники по всем предметам
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|












