|
|
|
| (19 промежуточных версий не показаны.) | | Строка 1: |
Строка 1: |
| - | <br> <br>ХІМІЧНИЙ СКЛАД ЖИВИХ ОРГАНІЗМІВ. НЕОРГАНІЧНІ СПОЛУКИ<br> <br>Що спільного між живою та неживою природою? Які основні неорганічні сполуки входять до складу живих організмів? Які їхні функції? Що таке катіони і аніони?<br>Що вивчає біохімія? Науку, що вивчає хімічний склад живих організмів, будову, властивості та роль виявлених у них сполук, шляхи їхнього виникнення та перетворення, називають біологічною хімією, або біохімією. Ця наука як галузь біології сформувалась у другій половині XIX століття.<br>Сучасна біохімія досліджує живу матерію на різних рівнях її організації: молекулярному, клітинному, організмовому. Одне з основних її завдань - з'ясування механізмів регуляції життєдіяльності клітин і організму в цілому, які забезпечують єдність процесів обміну речовин та перетворення енергії в організмі.<br>Який елементарний хімічний склад живих організмів? Живі організми містять майже всі відомі в природі хімічні елементи. Одні з них виявлені в усіх організмів без винятку, інші - лише в окремих або трапляються зрідка (див. таблицю).<br>Хімічний склад живих організмів відносно сталий. У найбільшій кількості в них наявні чотири хімічні елементи: Гідроген, Карбон, Нітроген і Окси-ген. їхня частка у хімічному складі клітини становить майже 98%, і вони належать до макроелементів. їх називають також органогенними, оскільки насамперед ці елементи входять до складу органічних сполук.<br>До макроелементів також належать Фосфор, Калій, Сульфур, Хлор, Кальцій, Магній, Натрій і Ферум, їхня сумарна частка становить до 1,9%. Понад 50 хімічних елементів відносять до мікроелементів (Йод, Кобальт, Манган, Купрум, Молібден, Цинк тощо). їхній вміст у клітині - від 10~12 до 10~3 %. Ще менше у клітині ультрамікроелементів: Плюмбуму, Брому, Аргентуму, Ауруму та ін. Хімічні елементи, що містяться в клітині, входять до складу органічних та неорганічних сполук або перебувають у вигляді іонів.<br>Хімічний склад усіх живих організмів відносно подібний. Натомість, у різних компонентів неживої природи він різний. Наприклад, у водній оболонці Землі (гідросфері) переважають Гідроген і Оксиген, у газоподібній (атмосфері) - Оксиген і Нітроген, у твердій (літосфері) — Силіцій, Оксиген та ін. | + | <metakeywords>Гіпермаркет Знань - перший в світі!, Гіпермаркет Знань, Біологія, 10 клас, клас, урок, на Тему, Неорганічні сполуки, вода, та мінеральні солі, Живі організми, обміну речовин, ліпіди, кров, білки, вуглеводи, мембрана</metakeywords> |
| | | | |
| | + | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Біологія|Біологія]]>>[[Біологія 10 клас|Біологія 10 клас]]>> Біологія: Неорганічні сполуки: вода та мінеральні солі.''' |
| | | | |
| | + | <br> |
| | | | |
| - | [[Image:tab.jpeg]]<br> <br> | + | '''Неорганічні сполуки: вода та мінеральні солі. '''<br> <br> ''Які властивості води? '' |
| | + | |
| | + | Серед неорганічних сполук живих організмів особлива роль належить воді. Вода є основним середовищем, у якому відбуваються процеси '''[[Значення обміну речовин і енергії.|обміну речовин]]''' та перетворення енергії. Вміст води в більшості живих організмів становить 60-70%, а в деяких (наприклад, у медуз) до 98%. Вода утворює основу внутрішнього середовища живих організмів ('''[[Кровь и остальные компоненты внутренней среды организма|крові]]''', лімфи, міжклітинної рідини).<br> |
| | + | |
| | + | '''<br>Вода має унікальні хімічні та фізичні властивості. ''' |
| | + | |
| | + | Порівняно з іншими рідинами в неї відносно висока температура кипіння і випаровування. Молекула води (Н<sub>2</sub>0) складається з двох атомів Гідрогену, які пов'язані міцним ковалентним зв'язком з атомом Оксигену. Молекула води електронейтральна, бо на її різних полюсах розташовані позитивний та негативний електричні заряди. Це визначає і таку властивість молекули води, як полярність. Саме завдяки полярності сусідні молекули води можуть притягуватись одна до одної: сили електричної взаємодії виникають між негативним зарядом на атомі Оксигену однієї молекули та позитивним зарядом на атомі Гідрогену іншої. Такий тип зв'язку називають водневим. Він у 15-20 разів слабший за ковалентний (мал. 2).<br> |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:Мал.2.jpg|480px|Просторова структура молекули води (1) та утворення водневого зв'язку (2)]] |
| | + | |
| | + | ''Мал. 2. Просторова структура молекули води (1) та утворення водневого зв'язку (2)'' |
| | + | |
| | + | <br> |
| | + | |
| | + | ''Які функції води в клітині? '' |
| | + | |
| | + | Вода визначає внутрішньоклітинний тиск (тургор) та об'єм клітин. Вона здатна формувати водну оболонку навколо певних сполук (наприклад, '''[[Фішки до теми: Будова і властивості білків.|білків]]'''), що запобігає їхній взаємодії між собою. Таку воду називають зв'язаною (структурованою). її частка становить 4-5% від загальної кількості води в організмі. Іншу частину води (95-96%), не зв'язану з іншими сполуками, називають вільною. Саме вільна вода є універсальним розчинником, кращим, ніж більшість інших рідин.<br> |
| | + | |
| | + | Залежно від того, розчиняються певні сполуки у воді чи ні, їх умовно поділяють на гідрофільні, або полярні, та гідрофобні, або неполярні. До гідрофільних (від грец. хідор - вода та філіа - люблю) сполук, здатних розчинятись у воді, належить більшість солей, наприклад, кухонна сіль (NаСІ). Вода розчиняє більшість речовин, які містять групи (-ОН, -СООН та ін.), здатні іонізуватися (тобто розпадатися на електрично заряджені частинки) під час взаємодії з нею. |
| | + | |
| | + | Гідрофобні (від грец. фобос - страх) сполуки (майже всі жири, деякі білки та ін.) містять неполярні групи (-СН, -СН<sub>2</sub>СН<sub>3</sub> та ін.), які не взаємодіють з водою, тому в ній не розчиняються. |
| | + | |
| | + | Вода як універсальний розчинник відіграє надзвичайно важливу роль у живих організмах, оскільки більшість біохімічних реакцій відбувається у водних розчинах. Надходять речовини у клітини та виводяться з них продукти життєдіяльності також переважно в розчиненому вигляді. Вода бере безпосередню участь у реакціях гідролізу (від грец. лізіс - розкладання) - розщеплення органічних сполук з приєднанням до місця розриву іонів молекули води (Н<sup>+</sup> та ОН<sup>-</sup>). |
| | + | |
| | + | <br> |
| | + | |
| | + | '''З водою пов'язана також регуляція теплового режиму організмів. ''' |
| | + | |
| | + | Їй притаманна велика теплоємність, тобто здатність поглинати тепло за незначних змін власної температури. Завдяки цьому вода запобігає різким змінам температури в клітинах і в організмі в цілому за значних її коливань у навколишньому середовищі. Під час випаровування води організми витрачають багато тепла. Так вони захищають себе від перегрівання. Завдяки високій теплопровідності, вода забезпечує рівномірний розподіл теплоти між тканинами організму, циркулюючи по порожнинах органів і тіла (порожнинна рідина, кров, лімфа тощо). |
| | + | |
| | + | Важливе біологічне значення для функціонування організмів має і те, що вода під впливом розчинених у ній речовин може змінювати свої властивості, зокрема температуру замерзання і кипіння. Так, із настанням зими у клітинах морозостійких рослин і холоднокровних тварин підвищується концентрація розчинних '''[[Фішки до теми:Вуглеводи, їх будова, властивості.|вуглеводів]]''' та інших сполук (наприклад, гліцерину). Це перешкоджає переходу води в організмах у кристалічний стан і таким чином запобігає їхній загибелі. |
| | + | |
| | + | На перебіг біохімічних реакцій у водних розчинах істотно впливає концентрація іонів гідрогену у воді, її оцінюють за водневим показником - рН (значення від'ємного десяткового логарифму концентрації іонів гідрогену). |
| | + | |
| | + | <br> |
| | + | |
| | + | ''Які ще неорганічні сполуки, крім води, е в організмах? Які їхні функції? '' |
| | + | |
| | + | Для підтримання процесів життєдіяльності окремих клітин і організму в цілому важливе значення мають солі неорганічних (мінеральних) сполук. У живих організмах вони розчинені в воді (у вигляді іонів) або перебувають у вигляді твердих сполук. Іони утворені катіонами металів (калію, натрію, кальцію, магнію тощо) і аніонами кислот (хлоридної - СІ<sup>-</sup>, сульфатної - НSO<sub>4</sub><sup>-</sup>, SO<sub>4</sub><sup>2-</sup>, карбонатної - НСО<sub>3</sub><sup>-</sup>, фосфатної - Н<sub>2</sub>РО<sub>4</sub><sup>-</sup>, НРО<sub>4</sub><sup>2-</sup> та ін.). |
| | + | |
| | + | Різна концентрація К<sup>+</sup> і Na<sup>+</sup> поза клітинами та всередині них спричинює виникнення різниці електричних потенціалів на плазматичних мембранах клітини. Це забезпечує передачу нервових імпульсів, а також транспорт речовин через '''[[Клітинні мембрани, їх будова та функції. Повні уроки|мембрани]]'''. Регуляторну функцію та активацію багатьох ферментів здійснюють Са<sup>2+</sup> і Мg<sup>2+</sup>. Сполуки кальцію (СаСО<sub>3</sub>) входять до складу черепашок молюсків і найпростіших (радіолярій) внутрішньоклітинний скелет побудований з двооксиду силіцію (SіО<sub>2</sub>) або сульфатнокислого стронцію (SrSO<sub>4</sub>). |
| | + | |
| | + | Важливі функції виконують також неорганічні кислоти. Так, хлоридна кислота створює кисле середовище в шлунку хребетних тварин і людини, забезпечуючи цим активність ферментів шлункового соку. Залишки сульфатної кислоти, приєднуючись до нерозчинних у воді сполук, забезпечують їхню розчинність. Це сприяє виведенню даних сполук з клітин і організму. |
| | + | |
| | + | Загальний вміст неорганічних речовин у клітинах різних типів варіює в межах від одного до декількох відсотків.<br><u><br></u>'''<u>Контрольні запитання</u>''' |
| | + | |
| | + | ''1. Що вивчає наука біохімія?<br>2. У яких співвідношеннях перебувають у живих клітинах різні хімічні елементи?<br>3. Які властивості води як основи внутрішнього середовища організмів?<br>4. Які функції виконує вода в живих організмах?<br>5. У якому стані в клітині перебувають солі? Які їхні функції в живих організмах?''<br> <br>'''<u>Поміркуйте</u>''' |
| | + | |
| | + | Які особливості будови молекул води забезпечують її властивості?<br>Як фізико-хімічні властивості води забезпечують процеси життєдіяльності окремих клітин і всього організму?<br> <br> |
| | + | |
| | + | <br> |
| | + | |
| | + | ''М.Є. Кучеренко, Ю.Г. Первес, П.Г. Балан, В.М. Войціцький, Загальна '''[[Біологія — наука про живу природу. Значення біології. Повні уроки|біологія]]''', 10 клас<br>Вислано читачами інтернет-сайту.''<br> |
| | + | |
| | + | <br> |
| | + | |
| | + | '''Роль неорганічних речовин у життєдіяльності організмів ''' |
| | + | |
| | + | <br><u>'''Пригадайте:'''</u> |
| | + | |
| | + | ''які основні класи неорганічних сполук виявляють у живих організмах? '' |
| | + | |
| | + | ''Які їхні функції? '' |
| | + | |
| | + | ''Що таке радіонукліди, ізотопи?'' |
| | + | |
| | + | <br>Вам уже відомо, що всі хімічні речовини поділяють на органічні та неорганічні. Загальний вміст неорганічних речовин (крім води) у різних клітинах варіює в межах від одного до декількох відсотків. Серед неорганічних речовин важливу роль у забезпеченні функціонування окремих клітин і цілісних організмів відіграють вода, неорганічні кислоти, луги та солі. |
| | + | |
| | + | Солі неорганічних кислот усередині живих організмів розчинені у воді (у вигляді йонів) або перебувають у твердому стані (наприклад, солі Кальцію та Фосфору у складі скелета людини та більшості хребетних тварин) (мал. 5.1). |
| | + | |
| | + | Вони утворені катіонами металічних елементів (Калію, Натрію, Кальцію, Магнію тощо) та аніонами неорганічних кислот (СІ-, Н804 , 802-, НСО3, Н2РО4, НРО2- та ін.). |
| | + | |
| | + | Різна концентрація йонів №+ і К+ поза клітинами та всередині них приводить до виникнення різниці електричних потенціалів на мембранах, які оточують клітини. Це забезпечує транспорт речовин через мембрани, а також передачу нервових імпульсів. До складу багатьох ферментів входять йони Са<sup>2+</sup> і Мд<sup>2+</sup>, які забезпечують їхню активність. Присутність у плазмі крові йонів Са<sup>2+</sup> - необхідна умова зсідання крові. За нестачі солей Кальцію порушується робота серцевого та скелетних м'язів (зокрема, виникають судоми). |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:B1014.jpg|550px|Солі Кальцію]] |
| | + | |
| | + | <br>Сталий уміст натрій хлориду (0,9 %) у плазмі крові - необхідна складова підтримання гомеостазу нашого організму. Розчин натрій хлориду такої концентрації ще називають фізіологічним. Його використовують при ін'єкціях певних ліків або вводять за незначних крововтрат (пригадайте, з якою метою). |
| | + | |
| | + | Щодоби до організму людини має надходити 12-15 г кухонної солі (№С1). Всмоктування солей починається ще в шлунку, а завершується в кишечнику. Рецептори, розташовані у стінках кровоносних судин і тканинах, здатні визначати концентрацію солей. Імпульси від цих рецепторів надходять до гіпоталамуса, який, у свою чергу, регулює діяльність залоз внутрішньої секреції. Залежно від вмісту солей в організмі під впливом нейрогуморальної регуляції змінюється їхній вміст у сечі. |
| | + | |
| | + | Через порушення обміну речовин солі можуть відкладатися у суглобах, що спричиняє важкі захворювання - остеохондроз та подагру, за яких спотворюються суглоби кінцівок, втрачається гнучкість хребта, розвиваються напади болю в нирках. Ці захворювання можуть призвести до зменшення рухомості та втрати працездатності. Щоб їх уникнути, необхідно вести активний спосіб життя, не зловживати м'ясними та жирними стравами, сіллю та іншими приправами, відмовитися від алкоголю. |
| | + | |
| | + | У порожнинах органів або їхніх вивідних проток можуть формуватися щільні утворення - «камені». Найчастіше вони утворюються в нирках, жовчному міхурі, ниркових мисках і сечовому міхурі при відкладанні там кальцієвих солей органічних (сечова та щавлева) або неорганічних (карбонатної чи ортофосфатної) кислот. Унаслідок розвивається сечокам'яна хвороба - камені, поступово збільшуючись, спочатку викликають болі в поперековій ділянці, а потім, просуваючись через сечовивідні шляхи, -напади дуже сильного болю. Інколи камені закупорюють сечоводи і тоді, аби врятувати життя хворого, застосовують хірургічне втручання. |
| | + | |
| | + | <br> |
| | + | |
| | + | '''Важливі функції виконують в організмі і неорганічні кислоти. ''' |
| | + | |
| | + | Ми вже згадували, хлоридна кислота створює кисле середовище в шлунку хребетних тварин і людини, забезпечуючи активність ферментів шлункового соку. У людей, в шлунку яких хлоридної кислоти виробляється недостатня кількість, порушуються процеси перетравлення білків, можливе розмноження у шлунку великої кількості шкідливих бактерій тощо. Збільшення секреції хлоридної кислоти також небезпечне для організму людини, зокрема воно спричиняє печію. |
| | + | |
| | + | Залишки сульфатної кислоти, приєднуючись до нерозчинних у воді сполук, забезпечують їхню розчинність. Це сприяє виведенню таких речовин у розчиненому стані з клітин і організму. Ортофосфатна кислота необхідна для синтезу АТФ (є універсальним накопичувачем енергії в клітині) та різних типів нуклеїнових кислот. |
| | + | |
| | + | <br>'''Кислотно-лужний баланс. ''' |
| | + | |
| | + | Внутрішнє середовище людини має певне співвідношення позитивних і негативних йонів - кислотно-лужний баланс. У разі його порушення можуть виникати важкі захворювання. Зокрема, при підвищенні вмісту позитивних йонів організм погано засвоює Кальцій, Натрій, Калій, а при зростанні вмісту негативних -повільніше засвоюється їжа, що негативно впливає на функції печінки і нирок, виникають алергічні стани, загострюються хронічні захворювання тощо. |
| | + | |
| | + | <br>'''Екологічні захворювання. ''' |
| | + | |
| | + | Не всі сполуки, які надходять в організми з водою та їжею, корисні для них. Наприклад, для організму людини небезпечне надходження солей важких металів (Плюмбуму, Хрому тощо) та радіонуклідів. Багато важких металів міститься у транспортних викидах. Тому обабіч великих автомобільних трас не слід збирати гриби, бо вони здатні накопичувати у своєму тілі ці речовини, а також радіонукліди. Ці сполуки можуть відіграти роль канцерогенних, тобто таких, що сприяють утворенню в організмі доброякісних та злоякісних пухлин, призводять до надмірного розмноження клітин крові: лейкоцитів (лейкози), рідше -еритроцитів (еритроцитози). Потрапивши в організм вагітної жінки, радіонукліди можуть зумовити вади розвитку зародка. |
| | + | |
| | + | Для організму людини та тварин небезпечні радіоактивні ізотопи багатьох хімічних елементів: Йоду, Цезію, Стронцію, Урану та ін. Потрапляючи в організми, Стронцій-90 може відкладатись у кістках, заступаючи Кальцій. Унаслідок цього кістки стають ламкими. Ізотоп Йоду порушує функції щитоподібної залози. Значні концентрації радіонуклідів здатні накопичувати рослини. З рослинною їжею вони згодом потрапляють в організми тварин і людини. |
| | + | |
| | + | Унаслідок аварії на ЧАЕС радіонуклідами забруднено понад 8,4 млн га земель, серед них 3,5 млн га орних. Якщо врахувати забрудненість ґрунтів України також важкими металами та отрутохімікатами (пестицидами), то нині в незадовільному стані перебуває близько 20 % території нашої країни. Найвищий рівень забрудненості ґрунтів важкими металами зафіксовано в Донецькій і Закарпатській областях. Так, у Донецькій області це пов'язано з діяльністю промислових підприємств і гірничодобувних шахт, а в Закарпатській -неодноразовими аваріями на гірничодобувних підприємствах Румунії, внаслідок чого значна кількість важких металів потрапила у р. Тису і під час її розливу -на сільськогосподарські угіддя. |
| | + | |
| | + | Слід зазначити, що навколо великих промислових підприємств радіус забруднення токсичними речовинами становить від 1 до 20 км і їхня концентрація може перевищувати гранично допустиму в 5-10 разів. Істотним чинником забруднення ґрунтів є викиди вихлопних газів транспортом. Уміст Плюмбуму в ґрунті навіть на відстані 50 км від траси може перевищувати допустимий у 3-4 рази. |
| | + | |
| | + | <br> |
| | + | |
| | + | '''Високий вміст нітратів в їжі та воді шкідливий для організму людини. ''' |
| | + | |
| | + | Тому за вмістом нітратів, наприклад в овочах, має здійснюватися постійний контроль. Існують спеціальні норми вмісту нітратів та інших шкідливих сполук у продуктах харчування та воді. Згідно з ними визначені так звані гранично допустимі концентрації (ГДК). Якщо вміст шкідливих речовин у воді чи продуктах харчування перевищує показники ГДК, то такі продукти і воду мають вилучати з продажу і вжитку. |
| | + | |
| | + | Забруднення атмосфери спричиняють викиди шкідливих для [http://xvatit.com/sneeze/ '''здоров'я'''] людини й інших організмів відходів промислових підприємств, вихлопних газів автомобільного транспорту (сполук Сульфуру, Нітрогену, чадного газу СО, важких металів тощо). Підприємства будівельної і вугільної промисловості (цементні та гіпсові заводи, відкриті вугільні кар'єри тощо) є джерелами забруднення атмосфери пилом. |
| | + | |
| | + | Особливу небезпеку для довкілля становлять кислотні дощі, спричинені забрудненням атмосфери сірчистим газом 802 (промислові підприємства та автотранспорт викидають в атмосферу понад 160 млн тонн сірчистого газу щорік) та оксидами Нитрогену (М20, М203 і М02). При з'єднанні з водою атмосфери ці речовини утворюють сильні неорганічні кислоти. На великих територіях промислово розвинених країн зареєстровано опади, кислотність яких перевищує нормальну від 10 до 1000 разів. Від кислотних дощів руйнуються екосистеми прісних водойм, гинуть ліси (мал. 5.2), знижується врожайність ґрунтів. |
| | + | |
| | + | Під керівництвом Міжнародного союзу охорони природи та природних ресурсів (МСОП) нині розроблено стратегічні принципи побудови екологічно стабільного суспільства, які погоджено з урядами більшості країн світу. Однією з умов побудови такого суспільства є чітке обмеження (квотування) промислових викидів країнами світу. При цьому країни, які не повністю використовують свої квоти (це стосується, зокрема, України), можуть продавати невикористану частину квоти іншим. Отримані кошти використовують для впровадження методик, спрямованих на поліпшення стану довкілля. |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:B1015.jpg|550px|Промисловість]] |
| | + | |
| | + | <br> |
| | + | |
| | + | '''Коротко про головне''' |
| | + | |
| | + | Загальний вміст неорганічних речовин (крім води) у клітинах різних типів варіює в межах від одного до декількох відсотків. Серед цих сполук важливу роль у забезпеченні нормального функціонування окремих клітин і цілісних організмів відіграють кислоти, луги та солі. |
| | + | |
| | + | <br> |
| | + | |
| | + | ''П.Г. Балан, Ю.Г. Вервес, В.П. Поліщук. Біологія, 10 клас<br>Вислано читачами інтернет-сайту.''<br> |
| | + | |
| | + | <br> |
| | + | |
| | + | '''Функції води в життєдіяльності організмів ''' |
| | + | |
| | + | <br><u>'''Пригадайте:'''</u> |
| | + | |
| | + | ''яка будова молекули води? '' |
| | + | |
| | + | ''Як відбувається водно-сольовий обмін в організмі людини? '' |
| | + | |
| | + | ''Що таке адаптації, транспірація, ковалентний і водневий типи зв'язків між молекулами?'' |
| | + | |
| | + | <br>Серед усіх хімічних сполук виняткова роль у забезпеченні процесів життєдіяльності організмів належить воді. Саме у водному середовищі виникло життя на нашій планеті, тому без води неможлива життєдіяльність жодних організмів. |
| | + | |
| | + | Вміст води в організмах становить 60-70 %, а в деяких випадках - до 98 %. Цитоплазма більшості клітин містить приблизно 80 % води. Кров і лімфа людини містять понад 80 % води. Отже, вода утворює основу внутрішнього середовища організмів (цитоплазми одноклітинних тварин, крові, лімфи, порожнинної рідини багатоклітинних організмів, соків рослин тощо). У водному середовищі відбуваються процеси обміну речовин і перетворення енергії. Вода бере безпосередню участь у реакціях розщеплення органічних сполук. |
| | + | |
| | + | <br> |
| | + | |
| | + | '''Структура, властивості та функції' води. ''' |
| | + | |
| | + | Воді притаманні унікальні хімічні й фізичні властивості. Погляньте на малюнок 6.1: молекула води (Н2О) складається з двох атомів Гідрогену, сполучених з атомом Оксигену ковалентними зв'язками. На полюсах молекули води розміщені позитивні і негативний заряди, тобто вона полярна. Завдяки цьому дві сусідні молекули зазвичай взаємно притягуються за рахунок сил електростатичної взаємодії між негативним зарядом атома Оксигену однієї молекули та позитивним зарядом атома Гідрогену іншої. |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:B1016.jpg|550px|Молекули води]] |
| | + | |
| | + | <br> |
| | + | |
| | + | При цьому виникає водневий зв'язок (мал. 6.2), у 15-20 разів слабший за ковалентний. Коли вода перебуває в рідкому стані, її молекули безперервно рухаються і водневі зв'язки постійно то розриваються, то виникають знову.<br>Частина молекул води формує водну оболонку навколо деяких сполук (наприклад, білків). Таку воду називають зв'язаною, або структурованою (4-5 % загальної кількості води в організмах). Структурована вода, що формує водну оболонку навколо певних молекул, запобігає їхній взаємодії. Крім того, вода бере участь у підтриманні структури певних молекул, наприклад білків. Решта 95-96 % води має назву вільної: вона не пов'язана з іншими сполуками. |
| | + | |
| | + | Залежно від температури середовища вода здатна змінювати агрегатний стан. За зниження температури вода з рідкого стану може переходити в твердий, а за підвищення - у газуватий. |
| | + | |
| | + | Утворення кристаликів льоду в клітинах організмів руйнує клітинні структури. Це призводить до загибелі клітин і всього організму. Саме тому ссавців і людину неможливо заморозити, а потім - розморозити без втрати здатності відновлювати процеси життєдіяльності. |
| | + | |
| | + | Під впливом розчинених у ній речовин вода може змінювати свої властивості, зокрема точки температур замерзання (плавлення) і кипіння, що має важливе біологічне значення. Наприклад, у клітинах рослин з настанням зими підвищується концентрація розчинів вуглеводів, членистоногих - гліцерину, риб - білків тощо. Це знижує температуру, за якої вода переходить у твердий стан, що запобігає промерзанню. Уявіть собі: серед комах відомі льодовичники (мал. 6.3), здатні зберігати активність на сніговому покриві (вони мешкають і в Україні). |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:B1017.jpg|240px|Льодовичник]] |
| | + | |
| | + | <br> |
| | + | |
| | + | Молекулам води притаманна здатність до іонізації, коли вони розщеплюються на йони Гідрогену та гідроксилу. При цьому між молекулами води та йонами встановлюється динамічна рівновага: |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:B1018.jpg]] |
| | + | |
| | + | <br>Хоча іонізація хімічно чистої води дуже слабка (за температури +25 °С із 107 молекул тільки одна перебуває в іонізованому стані), вона відіграє важливу біологічну роль. Від концентрації йонів Гідрогену, яку оцінюють за водневим показником (рН - значення негативного десяткового логарифма концентрації йонів Н+), залежать структурні особливості та активність макромолекул тощо. Нейтральній реакції розчину відповідає рН 7,0. Якщо його значення нижче -реакція розчину кисла, вище - лужна. У різних частинах організму і навіть однієї клітини можна спостерігати різні значення водневого показника. Це важливо для здійснення процесів обміну речовин, оскільки одні ферменти активні в лужному середовищі, інші - у кислому. Наприклад, в інфузорії-туфельки травні вакуолі періодично «подорожують» по клітині, опиняючись то в кислому, то в лужному середовищі. При цьому послідовно активні то одні травні ферменти, то інші, що сприяє кращому перетравленню поживних речовин. Пригадайте; у людини та ссавців ферменти шлункового соку активні в кислому середовищі, а підшлункового - у лужному. |
| | + | |
| | + | Водні розчини, здатні протистояти зміні їхнього показника рН при додаванні певної кількості кислоти або лугу, називають буферними системами. Вони складаються зі слабкої кислоти (донора Н+) і основи (акцептора Н+), здатних відповідно зв'язувати йони гідроксилу (ОН-) та Гідрогену (Н+), завдяки чому рН усередині клітини майже не змінюється. |
| | + | |
| | + | Вода визначає фізичні властивості клітин - об'єм і внутрішньоклітинний тиск (тургор). Порівняно з іншими рідинами в неї відносно високі температури кипіння та плавлення, що зумовлено водневими зв'язками між молекулами води.<br>Вода - значно кращий розчинник, ніж більшість інших відомих рідин. Тому всі речовини поділяють на такі, що добре розчиняються у воді (гідрофільні) та нерозчинні (гідрофобні). |
| | + | |
| | + | До гідрофільних сполук належить багато кристалічних солей, наприклад кухонна сіль (]аСІ), глюкоза, фруктоза, тростинний цукор тощо. Гідрофільні сполуки містять полярні (частково заряджені) групи, здатні взаємодіяти з молекулами води або іонізуватися (утворювати заряджені йони з нейтральних частин своєї молекули). Це, наприклад, амінокислоти, які містять карбоксильні (-СООН) та амінні (-]]Н2) групи. |
| | + | |
| | + | Гідрофобні речовини (майже всі '''[[Ліпіди: будова, властивості, функції. Презентація уроку|ліпіди]]''', деякі білки) містять неполярні групи, які не взаємодіють з молекулами води. Вони розчиняються переважно в неполярних органічних розчинниках (хлороформ, бензол). |
| | + | |
| | + | Існують й амфіфільні речовини, наприклад фосфоліпіди (сполуки ліпідів із залишками ортофосфатної кислоти), ліпопротеїди (сполуки ліпідів з білками), багато білків. Одна частина молекули цих сполук виявляє гідрофільні властивості, інша - гідрофобні. |
| | + | |
| | + | Коли певна сполука переходить у розчин, її молекули набувають здатності до руху і їхня реакційна здатність зростає. Саме тому більша частина біохімічних реакцій відбувається у водних розчинах. |
| | + | |
| | + | <br>'''Вода як універсальний розчинник відіграє важливу роль в обміні речовин. ''' |
| | + | |
| | + | Проникнення речовин у клітину та виведення з неї продуктів життєдіяльності можливе здебільшого лише в розчиненому стані. |
| | + | |
| | + | Вода як універсальний розчинник відіграє надзвичайно важливу роль у транспорті різних сполук у живих організмах. Розчини органічних і неорганічних речовин рослини транспортують по провідних тканинах або міжклітинниках. У тварин таку функцію виконують кров, лімфа, тканинна рідина тощо. |
| | + | |
| | + | Вода бере участь у складних біохімічних перетвореннях. Наприклад, за участі води відбуваються реакції гідролізу - розщеплення органічних сполук з приєднанням до місць розривів йонів Н+ та ОН- . |
| | + | |
| | + | З водою пов'язана здатність організмів регулювати свій тепловий режим. Їй властива висока теплоємність, яка зумовлює здатність поглинати тепло за незначних змін власної температури. Теплоємність - кількість тепла, необхідного для нагрівання тіла або середовища на 1 °С. Завдяки цьому вода запобігає різким змінам температури в клітинах та організмі в цілому за різких її коливань у навколишньому середовищі. Оскільки на випаровування води витрачається багато теплоти, організми в такий спосіб захищають себе від перегрівання (наприклад, транспірація у рослин, потовиділення у ссавців, випаровування вологи зі слизових оболонок тварин).<br>Завдяки високій теплопровідності вода забезпечує рівномірний розподіл теплоти між тканинами та органами організму. Наприклад, завдяки циркуляції рідин внутрішнього середовища у тварин або руху розчинів по тілу рослини. |
| | + | |
| | + | Водні розчини певних сполук слугують мастилом, яке захищає поверхні, що постійно зазнають тертя. Наприклад, рідина, яка заповнює порожнину суглобів, полегшує ковзання суглобових поверхонь, зменшуючи тертя між ними. Вона також живить хрящ, що вкриває суглобові поверхні кісток. |
| | + | |
| | + | Кожному виду організмів притаманний водний баланс - певне співвідношення між надходженням води та її витрачанням. Якщо витрати води перевищують її надходження до організму, спостерігають водний дефіцит, що негативно впливає на різні процеси життєдіяльності (у рослин - фотосинтезу, транспірації, у рослин і тварин - терморегуляції, перебігу біохімічних процесів тощо). Тому підтримання водного балансу - одна з умов нормального функціонування будь-якого організму. |
| | + | |
| | + | <br>'''Водний баланс людини. ''' |
| | + | |
| | + | Вміст води в організмі людини становить близько 65 %. Тобто, якщо маса людини становить 60 кг, то з них 39 кг припадає на воду. Слід зазначити, що вміст води залежить і від віку: у новонароджених він становить близько 75-80 %, у період завершення росту -65-70 %, а в людей похилого віку - лише 55-60 %. Між різними органами і тканинами людини вода розподілена нерівномірно: найбільше її в крові та нирках - 82-83 %, головному мозку - до 80 %, печінці - 75 %, м'язах -70-76 %, натомість у жировій тканині - близько 30 %, кістках - близько 20 %. |
| | + | |
| | + | Оскільки організм людини щоденно витрачає приблизно 2-2,5 л води (вона виводиться з неперетравленими рештками їжі, сечею, потом, випаровується з поверхні слизових оболонок ротової порожнини та дихальних шляхів), то така сама її кількість має постійно надходити туди. Шляхи надходження води до організму різні. Крім того, близько 1 л води потрапляє з продуктами харчування, ще майже 300 мл води утворюється внаслідок окиснення жирів, білків і вуглеводів (так звана метаболічна вода). |
| | + | |
| | + | Кількість спожитої за добу води залежить від умов, у яких перебуває людина. Так, у спекотну погоду або під час здійснення важкої фізичної праці витрати води зростають через посилене потовиділення та значне випаровування через слизові оболонки. Зневоднення організму (дегідратація) можливе і внаслідок порушень роботи кишечнику (сильні проноси), значних крововтрат тощо. За таких умов споживання води має збільшитися до 4-7 л на добу. Унаслідок зневоднення уповільнюються процеси травлення та всмоктування поживних речовин, порушуються процеси теплорегуляції; гусне кров, порушується її транспортна функція, у судинах можуть виникати згустки (тромби). Втрата понад 20 % води - смертельно небезпечна для людини. |
| | + | |
| | + | Людина, яка виконує важку фізичну працю за умов підвищеної температури (наприклад, у доменному цеху), втрачає за годину лише внаслідок посиленого потовиділення до 1,6 л води! Тож добова потреба у воді в неї може зростати до 20 л за добу. |
| | + | |
| | + | Першим сигналом недостатнього вмісту води в організмі є відчуття спраги, яке виникає при збудженні відповідного центру в гіпоталамусі (структура проміжного мозку). Його рецептори збуджуються як унаслідок зростання концентрації солей в рідинах організму, так і в разі підвищення концентрації йонів Натрію. Ці подразники сприймають різні групи рецепторів. Відчуття спраги виникає, якщо організм людини втрачає близько 1 % вологи свого тіла, і зникає після споживання певної кількості води, в середньому 0,25-0,5 л. |
| | + | |
| | + | Отже, основні свої потреби у воді людина задовольняє за рахунок питної води. Тому розглянемо вимоги до її якості. |
| | + | |
| | + | <br>'''Питна вода та вимоги до її якості. ''' |
| | + | |
| | + | В Україні вимоги до якості питної води визначені Державним стандартом. Згідно з ним питна вода має бути епідеміологічно безпечною та нешкідливою за хімічним складом. Безпеку води в епідеміологічному відношенні визначають як загальною кількістю мікроорганізмів (не більше 100 в 1 см3 води), так і за кількістю клітин кишкової палички (не більше 3 в 1 дм<sup>3</sup> води). Питна вода не повинна містити водні організми, помітні неозброєним оком, та плівку на поверхні. |
| | + | |
| | + | Основними забруднювачами водних об'єктів у нашій країні є промисловість (понад 55 % від загального скиду) та житлово-комунальне господарство (понад 40 %). Небезпечне забруднення водойм радіонуклідами. Стічні води з високою радіоактивністю (100 і більше Кюрі1 на 1 л води) мають бути поховані в підземних безстічних басейнах або резервуарах. |
| | + | |
| | + | Вам уже відомо, що в річках, озерах та інших водоймах відбуваються природні процеси самоочищення. У них беруть участь різноманітні організми: бактерії, водорості, одноклітинні тварини, губки, двостулкові молюски тощо. Але ці процеси тривають досить повільно, тому за інтенсивного забруднення неочищеними побутовими та промисловими стоками водні екосистеми нездатні самостійно очиститися. |
| | + | |
| | + | Методи очищення стічних вод поділяють на механічні, фізико-хімічні та біологічні (мал. 6.4). Механічні методи полягають в очищенні стічних вод від завислих у них частинок відстоюванням і фільтрацією. Ці методи дають змогу видаляти з побутових стічних вод до 2/3 нерозчинних домішок, а з промислових - до 9/10. |
| | + | |
| | + | За допомогою різноманітних фізико-хімічних методів зі стічної води видаляють розчинні неорганічні та органічні домішки, а також завислі в ній найдрібніші часточки. |
| | + | |
| | + | Завершальним етапом очищення стічних вод є застосування біологічних методів з використанням штучно створених ланцюгів живлення, до яких входять певні види бактерій, одноклітинних і багатоклітинних тварин.<br>Сира вода з природних водойм, а також недостатньо очищена питна вода може стати джерелом збудників різноманітних захворювань: дизентерії, холери, черевного тифу (сальмонельозу), глистних захворювань тощо. Тому перед споживанням воду з колодязів, струмків, бюветів слід добре прокип'ятити, а водопровідну - профільтрувати через спеціальні очисні побутові фільтри. |
| | + | |
| | + | Для обмеження втрат і збереження якості прісної води потрібні такі заходи: |
| | + | |
| | + | - зменшення витрат води для забезпечення роботи промисловості, транспорту та об'єктів сільського господарства;<br>- зменшення витрат прісної води для побутових потреб1; |
| | + | |
| | + | [[Image:B1019.jpg|550px|Очисні споруди]] |
| | + | |
| | + | <br>- охорона малих річок, які відіграють важливу роль у загальному водному балансі планети, зокрема живлять великі річки, від них залежить рівень підземних вод;<br>- створення умов для самоочищення водойм;<br>- проведення лісоохоронних заходів, оскільки внаслідок знищення лісів часто міліють річки та інші водойми;<br>- упровадження ефективних методів очищення стічних вод, здійснення постійного контролю за санітарним станом водойм і якістю питної води;<br>- створення замкнених систем водопостачання промислових, аграрних та енергетичних об'єктів.<br>- постійний контроль за станом джерел питної води. |
| | + | |
| | + | <br><u>'''Ключові терміни та поняття.''' </u> |
| | + | |
| | + | Гідрофільні, гідрофобні та амфіфільні сполуки, гідроліз, водний баланс.<br>Уміст води в організмах становить 60-70 %. |
| | + | |
| | + | Вода утворює основу внутрішнього середовища живих організмів, у якому відбуваються процеси обміну речовин і перетворення енергії. Вода бере безпосередню участь у реакціях розщеплення органічних сполук. |
| | + | |
| | + | Водний баланс - це певне співвідношення між надходженням і витрачанням води живою системою. |
| | + | |
| | + | Вода визначає фізичні властивості клітин - їхній об'єм і внутрішньоклітинний тиск (тургор). |
| | + | |
| | + | Вода - універсальний розчинник. Речовини, здатні добре розчинятися у воді, називають гідрофільними (полярними), нерозчинні - гідрофобними (неполярними). |
| | + | |
| | + | Вода відіграє надзвичайно важливу роль у транспорті різних сполук у живих організмах. Вона бере участь у складних біохімічних реакціях і процесах теплорегуляції організмів. Основні свої потреби людина задовольняє за рахунок питної води певних стандартів якості. Перед споживанням вода має бути очищена. Методи очищення стічних вод поділяють на механічні, фізико-хімічні та біологічні. |
| | + | |
| | + | <br> |
| | + | |
| | + | <br><br> |
| | + | |
| | + | ''П.Г. Балан, Ю.Г. Вервес, В.П. Поліщук. Біологія, 10 клас<br>Вислано читачами інтернет-сайту.'' |
| | + | |
| | + | <br> <sub>Підручники [[Гіпермаркет Знань - перший в світі!|скачати]] безкоштовно, онлайн уроки, реферати з [[Біологія|біології]], домашнє завдання запитання та відповіді</sub><br> |
| | + | |
| | + | '''<u>Зміст уроку</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект уроку і опорний каркас |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентація уроку |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративні методи та інтерактивні технології |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] закриті вправи (тільки для використання вчителями) |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] оцінювання |
| | + | |
| | + | '''<u>Практика</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачі та вправи,самоперевірка |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикуми, лабораторні, кейси |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рівень складності задач: звичайний, високий, олімпійський |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашнє завдання |
| | + | |
| | + | '''<u>Ілюстрації</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] реферати |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фішки для допитливих |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] гумор, притчі, приколи, приказки, кросворди, цитати |
| | + | |
| | + | '''<u>Доповнення</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] зовнішнє незалежне тестування (ЗНТ) |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] підручники основні і допоміжні |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] тематичні свята, девізи |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статті |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] національні особливості |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словник термінів |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] інше |
| | + | |
| | + | '''<u>Тільки для вчителів</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/Idealny_urok.html ідеальні уроки] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарний план на рік |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методичні рекомендації |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] програми |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/forum/ обговорення] |
| | + | |
| | + | <br> |
| | + | |
| | + | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. |
| | + | |
| | + | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. |
Текущая версия на 12:30, 31 августа 2012
Гіпермаркет Знань>>Біологія>>Біологія 10 клас>> Біологія: Неорганічні сполуки: вода та мінеральні солі.
Неорганічні сполуки: вода та мінеральні солі.
Які властивості води?
Серед неорганічних сполук живих організмів особлива роль належить воді. Вода є основним середовищем, у якому відбуваються процеси обміну речовин та перетворення енергії. Вміст води в більшості живих організмів становить 60-70%, а в деяких (наприклад, у медуз) до 98%. Вода утворює основу внутрішнього середовища живих організмів (крові, лімфи, міжклітинної рідини).
Вода має унікальні хімічні та фізичні властивості.
Порівняно з іншими рідинами в неї відносно висока температура кипіння і випаровування. Молекула води (Н20) складається з двох атомів Гідрогену, які пов'язані міцним ковалентним зв'язком з атомом Оксигену. Молекула води електронейтральна, бо на її різних полюсах розташовані позитивний та негативний електричні заряди. Це визначає і таку властивість молекули води, як полярність. Саме завдяки полярності сусідні молекули води можуть притягуватись одна до одної: сили електричної взаємодії виникають між негативним зарядом на атомі Оксигену однієї молекули та позитивним зарядом на атомі Гідрогену іншої. Такий тип зв'язку називають водневим. Він у 15-20 разів слабший за ковалентний (мал. 2).
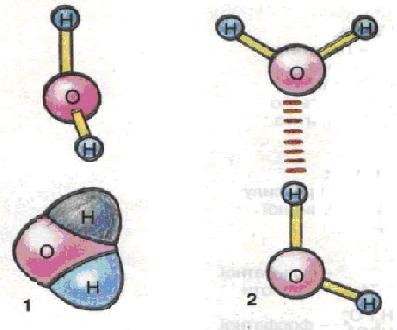
Мал. 2. Просторова структура молекули води (1) та утворення водневого зв'язку (2)
Які функції води в клітині?
Вода визначає внутрішньоклітинний тиск (тургор) та об'єм клітин. Вона здатна формувати водну оболонку навколо певних сполук (наприклад, білків), що запобігає їхній взаємодії між собою. Таку воду називають зв'язаною (структурованою). її частка становить 4-5% від загальної кількості води в організмі. Іншу частину води (95-96%), не зв'язану з іншими сполуками, називають вільною. Саме вільна вода є універсальним розчинником, кращим, ніж більшість інших рідин.
Залежно від того, розчиняються певні сполуки у воді чи ні, їх умовно поділяють на гідрофільні, або полярні, та гідрофобні, або неполярні. До гідрофільних (від грец. хідор - вода та філіа - люблю) сполук, здатних розчинятись у воді, належить більшість солей, наприклад, кухонна сіль (NаСІ). Вода розчиняє більшість речовин, які містять групи (-ОН, -СООН та ін.), здатні іонізуватися (тобто розпадатися на електрично заряджені частинки) під час взаємодії з нею.
Гідрофобні (від грец. фобос - страх) сполуки (майже всі жири, деякі білки та ін.) містять неполярні групи (-СН, -СН2СН3 та ін.), які не взаємодіють з водою, тому в ній не розчиняються.
Вода як універсальний розчинник відіграє надзвичайно важливу роль у живих організмах, оскільки більшість біохімічних реакцій відбувається у водних розчинах. Надходять речовини у клітини та виводяться з них продукти життєдіяльності також переважно в розчиненому вигляді. Вода бере безпосередню участь у реакціях гідролізу (від грец. лізіс - розкладання) - розщеплення органічних сполук з приєднанням до місця розриву іонів молекули води (Н+ та ОН-).
З водою пов'язана також регуляція теплового режиму організмів.
Їй притаманна велика теплоємність, тобто здатність поглинати тепло за незначних змін власної температури. Завдяки цьому вода запобігає різким змінам температури в клітинах і в організмі в цілому за значних її коливань у навколишньому середовищі. Під час випаровування води організми витрачають багато тепла. Так вони захищають себе від перегрівання. Завдяки високій теплопровідності, вода забезпечує рівномірний розподіл теплоти між тканинами організму, циркулюючи по порожнинах органів і тіла (порожнинна рідина, кров, лімфа тощо).
Важливе біологічне значення для функціонування організмів має і те, що вода під впливом розчинених у ній речовин може змінювати свої властивості, зокрема температуру замерзання і кипіння. Так, із настанням зими у клітинах морозостійких рослин і холоднокровних тварин підвищується концентрація розчинних вуглеводів та інших сполук (наприклад, гліцерину). Це перешкоджає переходу води в організмах у кристалічний стан і таким чином запобігає їхній загибелі.
На перебіг біохімічних реакцій у водних розчинах істотно впливає концентрація іонів гідрогену у воді, її оцінюють за водневим показником - рН (значення від'ємного десяткового логарифму концентрації іонів гідрогену).
Які ще неорганічні сполуки, крім води, е в організмах? Які їхні функції?
Для підтримання процесів життєдіяльності окремих клітин і організму в цілому важливе значення мають солі неорганічних (мінеральних) сполук. У живих організмах вони розчинені в воді (у вигляді іонів) або перебувають у вигляді твердих сполук. Іони утворені катіонами металів (калію, натрію, кальцію, магнію тощо) і аніонами кислот (хлоридної - СІ-, сульфатної - НSO4-, SO42-, карбонатної - НСО3-, фосфатної - Н2РО4-, НРО42- та ін.).
Різна концентрація К+ і Na+ поза клітинами та всередині них спричинює виникнення різниці електричних потенціалів на плазматичних мембранах клітини. Це забезпечує передачу нервових імпульсів, а також транспорт речовин через мембрани. Регуляторну функцію та активацію багатьох ферментів здійснюють Са2+ і Мg2+. Сполуки кальцію (СаСО3) входять до складу черепашок молюсків і найпростіших (радіолярій) внутрішньоклітинний скелет побудований з двооксиду силіцію (SіО2) або сульфатнокислого стронцію (SrSO4).
Важливі функції виконують також неорганічні кислоти. Так, хлоридна кислота створює кисле середовище в шлунку хребетних тварин і людини, забезпечуючи цим активність ферментів шлункового соку. Залишки сульфатної кислоти, приєднуючись до нерозчинних у воді сполук, забезпечують їхню розчинність. Це сприяє виведенню даних сполук з клітин і організму.
Загальний вміст неорганічних речовин у клітинах різних типів варіює в межах від одного до декількох відсотків.
Контрольні запитання
1. Що вивчає наука біохімія?
2. У яких співвідношеннях перебувають у живих клітинах різні хімічні елементи?
3. Які властивості води як основи внутрішнього середовища організмів?
4. Які функції виконує вода в живих організмах?
5. У якому стані в клітині перебувають солі? Які їхні функції в живих організмах?
Поміркуйте
Які особливості будови молекул води забезпечують її властивості?
Як фізико-хімічні властивості води забезпечують процеси життєдіяльності окремих клітин і всього організму?
М.Є. Кучеренко, Ю.Г. Первес, П.Г. Балан, В.М. Войціцький, Загальна біологія, 10 клас
Вислано читачами інтернет-сайту.
Роль неорганічних речовин у життєдіяльності організмів
Пригадайте:
які основні класи неорганічних сполук виявляють у живих організмах?
Які їхні функції?
Що таке радіонукліди, ізотопи?
Вам уже відомо, що всі хімічні речовини поділяють на органічні та неорганічні. Загальний вміст неорганічних речовин (крім води) у різних клітинах варіює в межах від одного до декількох відсотків. Серед неорганічних речовин важливу роль у забезпеченні функціонування окремих клітин і цілісних організмів відіграють вода, неорганічні кислоти, луги та солі.
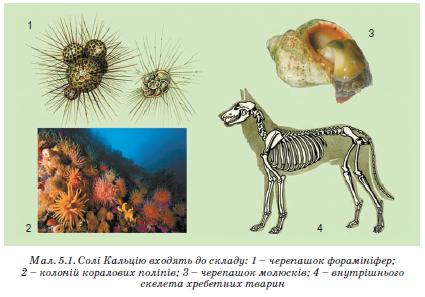
Солі неорганічних кислот усередині живих організмів розчинені у воді (у вигляді йонів) або перебувають у твердому стані (наприклад, солі Кальцію та Фосфору у складі скелета людини та більшості хребетних тварин) (мал. 5.1).
Вони утворені катіонами металічних елементів (Калію, Натрію, Кальцію, Магнію тощо) та аніонами неорганічних кислот (СІ-, Н804 , 802-, НСО3, Н2РО4, НРО2- та ін.).
Різна концентрація йонів №+ і К+ поза клітинами та всередині них приводить до виникнення різниці електричних потенціалів на мембранах, які оточують клітини. Це забезпечує транспорт речовин через мембрани, а також передачу нервових імпульсів. До складу багатьох ферментів входять йони Са2+ і Мд2+, які забезпечують їхню активність. Присутність у плазмі крові йонів Са2+ - необхідна умова зсідання крові. За нестачі солей Кальцію порушується робота серцевого та скелетних м'язів (зокрема, виникають судоми).
Сталий уміст натрій хлориду (0,9 %) у плазмі крові - необхідна складова підтримання гомеостазу нашого організму. Розчин натрій хлориду такої концентрації ще називають фізіологічним. Його використовують при ін'єкціях певних ліків або вводять за незначних крововтрат (пригадайте, з якою метою).
Щодоби до організму людини має надходити 12-15 г кухонної солі (№С1). Всмоктування солей починається ще в шлунку, а завершується в кишечнику. Рецептори, розташовані у стінках кровоносних судин і тканинах, здатні визначати концентрацію солей. Імпульси від цих рецепторів надходять до гіпоталамуса, який, у свою чергу, регулює діяльність залоз внутрішньої секреції. Залежно від вмісту солей в організмі під впливом нейрогуморальної регуляції змінюється їхній вміст у сечі.
Через порушення обміну речовин солі можуть відкладатися у суглобах, що спричиняє важкі захворювання - остеохондроз та подагру, за яких спотворюються суглоби кінцівок, втрачається гнучкість хребта, розвиваються напади болю в нирках. Ці захворювання можуть призвести до зменшення рухомості та втрати працездатності. Щоб їх уникнути, необхідно вести активний спосіб життя, не зловживати м'ясними та жирними стравами, сіллю та іншими приправами, відмовитися від алкоголю.
У порожнинах органів або їхніх вивідних проток можуть формуватися щільні утворення - «камені». Найчастіше вони утворюються в нирках, жовчному міхурі, ниркових мисках і сечовому міхурі при відкладанні там кальцієвих солей органічних (сечова та щавлева) або неорганічних (карбонатної чи ортофосфатної) кислот. Унаслідок розвивається сечокам'яна хвороба - камені, поступово збільшуючись, спочатку викликають болі в поперековій ділянці, а потім, просуваючись через сечовивідні шляхи, -напади дуже сильного болю. Інколи камені закупорюють сечоводи і тоді, аби врятувати життя хворого, застосовують хірургічне втручання.
Важливі функції виконують в організмі і неорганічні кислоти.
Ми вже згадували, хлоридна кислота створює кисле середовище в шлунку хребетних тварин і людини, забезпечуючи активність ферментів шлункового соку. У людей, в шлунку яких хлоридної кислоти виробляється недостатня кількість, порушуються процеси перетравлення білків, можливе розмноження у шлунку великої кількості шкідливих бактерій тощо. Збільшення секреції хлоридної кислоти також небезпечне для організму людини, зокрема воно спричиняє печію.
Залишки сульфатної кислоти, приєднуючись до нерозчинних у воді сполук, забезпечують їхню розчинність. Це сприяє виведенню таких речовин у розчиненому стані з клітин і організму. Ортофосфатна кислота необхідна для синтезу АТФ (є універсальним накопичувачем енергії в клітині) та різних типів нуклеїнових кислот.
Кислотно-лужний баланс.
Внутрішнє середовище людини має певне співвідношення позитивних і негативних йонів - кислотно-лужний баланс. У разі його порушення можуть виникати важкі захворювання. Зокрема, при підвищенні вмісту позитивних йонів організм погано засвоює Кальцій, Натрій, Калій, а при зростанні вмісту негативних -повільніше засвоюється їжа, що негативно впливає на функції печінки і нирок, виникають алергічні стани, загострюються хронічні захворювання тощо.
Екологічні захворювання.
Не всі сполуки, які надходять в організми з водою та їжею, корисні для них. Наприклад, для організму людини небезпечне надходження солей важких металів (Плюмбуму, Хрому тощо) та радіонуклідів. Багато важких металів міститься у транспортних викидах. Тому обабіч великих автомобільних трас не слід збирати гриби, бо вони здатні накопичувати у своєму тілі ці речовини, а також радіонукліди. Ці сполуки можуть відіграти роль канцерогенних, тобто таких, що сприяють утворенню в організмі доброякісних та злоякісних пухлин, призводять до надмірного розмноження клітин крові: лейкоцитів (лейкози), рідше -еритроцитів (еритроцитози). Потрапивши в організм вагітної жінки, радіонукліди можуть зумовити вади розвитку зародка.
Для організму людини та тварин небезпечні радіоактивні ізотопи багатьох хімічних елементів: Йоду, Цезію, Стронцію, Урану та ін. Потрапляючи в організми, Стронцій-90 може відкладатись у кістках, заступаючи Кальцій. Унаслідок цього кістки стають ламкими. Ізотоп Йоду порушує функції щитоподібної залози. Значні концентрації радіонуклідів здатні накопичувати рослини. З рослинною їжею вони згодом потрапляють в організми тварин і людини.
Унаслідок аварії на ЧАЕС радіонуклідами забруднено понад 8,4 млн га земель, серед них 3,5 млн га орних. Якщо врахувати забрудненість ґрунтів України також важкими металами та отрутохімікатами (пестицидами), то нині в незадовільному стані перебуває близько 20 % території нашої країни. Найвищий рівень забрудненості ґрунтів важкими металами зафіксовано в Донецькій і Закарпатській областях. Так, у Донецькій області це пов'язано з діяльністю промислових підприємств і гірничодобувних шахт, а в Закарпатській -неодноразовими аваріями на гірничодобувних підприємствах Румунії, внаслідок чого значна кількість важких металів потрапила у р. Тису і під час її розливу -на сільськогосподарські угіддя.
Слід зазначити, що навколо великих промислових підприємств радіус забруднення токсичними речовинами становить від 1 до 20 км і їхня концентрація може перевищувати гранично допустиму в 5-10 разів. Істотним чинником забруднення ґрунтів є викиди вихлопних газів транспортом. Уміст Плюмбуму в ґрунті навіть на відстані 50 км від траси може перевищувати допустимий у 3-4 рази.
Високий вміст нітратів в їжі та воді шкідливий для організму людини.
Тому за вмістом нітратів, наприклад в овочах, має здійснюватися постійний контроль. Існують спеціальні норми вмісту нітратів та інших шкідливих сполук у продуктах харчування та воді. Згідно з ними визначені так звані гранично допустимі концентрації (ГДК). Якщо вміст шкідливих речовин у воді чи продуктах харчування перевищує показники ГДК, то такі продукти і воду мають вилучати з продажу і вжитку.
Забруднення атмосфери спричиняють викиди шкідливих для здоров'я людини й інших організмів відходів промислових підприємств, вихлопних газів автомобільного транспорту (сполук Сульфуру, Нітрогену, чадного газу СО, важких металів тощо). Підприємства будівельної і вугільної промисловості (цементні та гіпсові заводи, відкриті вугільні кар'єри тощо) є джерелами забруднення атмосфери пилом.
Особливу небезпеку для довкілля становлять кислотні дощі, спричинені забрудненням атмосфери сірчистим газом 802 (промислові підприємства та автотранспорт викидають в атмосферу понад 160 млн тонн сірчистого газу щорік) та оксидами Нитрогену (М20, М203 і М02). При з'єднанні з водою атмосфери ці речовини утворюють сильні неорганічні кислоти. На великих територіях промислово розвинених країн зареєстровано опади, кислотність яких перевищує нормальну від 10 до 1000 разів. Від кислотних дощів руйнуються екосистеми прісних водойм, гинуть ліси (мал. 5.2), знижується врожайність ґрунтів.
Під керівництвом Міжнародного союзу охорони природи та природних ресурсів (МСОП) нині розроблено стратегічні принципи побудови екологічно стабільного суспільства, які погоджено з урядами більшості країн світу. Однією з умов побудови такого суспільства є чітке обмеження (квотування) промислових викидів країнами світу. При цьому країни, які не повністю використовують свої квоти (це стосується, зокрема, України), можуть продавати невикористану частину квоти іншим. Отримані кошти використовують для впровадження методик, спрямованих на поліпшення стану довкілля.

Коротко про головне
Загальний вміст неорганічних речовин (крім води) у клітинах різних типів варіює в межах від одного до декількох відсотків. Серед цих сполук важливу роль у забезпеченні нормального функціонування окремих клітин і цілісних організмів відіграють кислоти, луги та солі.
П.Г. Балан, Ю.Г. Вервес, В.П. Поліщук. Біологія, 10 клас
Вислано читачами інтернет-сайту.
Функції води в життєдіяльності організмів
Пригадайте:
яка будова молекули води?
Як відбувається водно-сольовий обмін в організмі людини?
Що таке адаптації, транспірація, ковалентний і водневий типи зв'язків між молекулами?
Серед усіх хімічних сполук виняткова роль у забезпеченні процесів життєдіяльності організмів належить воді. Саме у водному середовищі виникло життя на нашій планеті, тому без води неможлива життєдіяльність жодних організмів.
Вміст води в організмах становить 60-70 %, а в деяких випадках - до 98 %. Цитоплазма більшості клітин містить приблизно 80 % води. Кров і лімфа людини містять понад 80 % води. Отже, вода утворює основу внутрішнього середовища організмів (цитоплазми одноклітинних тварин, крові, лімфи, порожнинної рідини багатоклітинних організмів, соків рослин тощо). У водному середовищі відбуваються процеси обміну речовин і перетворення енергії. Вода бере безпосередню участь у реакціях розщеплення органічних сполук.
Структура, властивості та функції' води.
Воді притаманні унікальні хімічні й фізичні властивості. Погляньте на малюнок 6.1: молекула води (Н2О) складається з двох атомів Гідрогену, сполучених з атомом Оксигену ковалентними зв'язками. На полюсах молекули води розміщені позитивні і негативний заряди, тобто вона полярна. Завдяки цьому дві сусідні молекули зазвичай взаємно притягуються за рахунок сил електростатичної взаємодії між негативним зарядом атома Оксигену однієї молекули та позитивним зарядом атома Гідрогену іншої.
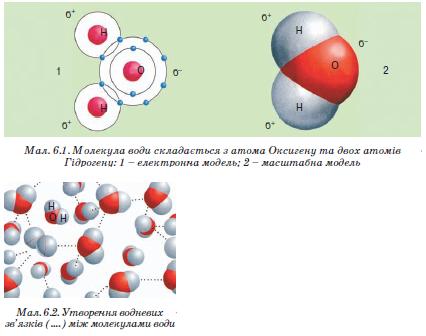
При цьому виникає водневий зв'язок (мал. 6.2), у 15-20 разів слабший за ковалентний. Коли вода перебуває в рідкому стані, її молекули безперервно рухаються і водневі зв'язки постійно то розриваються, то виникають знову.
Частина молекул води формує водну оболонку навколо деяких сполук (наприклад, білків). Таку воду називають зв'язаною, або структурованою (4-5 % загальної кількості води в організмах). Структурована вода, що формує водну оболонку навколо певних молекул, запобігає їхній взаємодії. Крім того, вода бере участь у підтриманні структури певних молекул, наприклад білків. Решта 95-96 % води має назву вільної: вона не пов'язана з іншими сполуками.
Залежно від температури середовища вода здатна змінювати агрегатний стан. За зниження температури вода з рідкого стану може переходити в твердий, а за підвищення - у газуватий.
Утворення кристаликів льоду в клітинах організмів руйнує клітинні структури. Це призводить до загибелі клітин і всього організму. Саме тому ссавців і людину неможливо заморозити, а потім - розморозити без втрати здатності відновлювати процеси життєдіяльності.
Під впливом розчинених у ній речовин вода може змінювати свої властивості, зокрема точки температур замерзання (плавлення) і кипіння, що має важливе біологічне значення. Наприклад, у клітинах рослин з настанням зими підвищується концентрація розчинів вуглеводів, членистоногих - гліцерину, риб - білків тощо. Це знижує температуру, за якої вода переходить у твердий стан, що запобігає промерзанню. Уявіть собі: серед комах відомі льодовичники (мал. 6.3), здатні зберігати активність на сніговому покриві (вони мешкають і в Україні).

Молекулам води притаманна здатність до іонізації, коли вони розщеплюються на йони Гідрогену та гідроксилу. При цьому між молекулами води та йонами встановлюється динамічна рівновага:

Хоча іонізація хімічно чистої води дуже слабка (за температури +25 °С із 107 молекул тільки одна перебуває в іонізованому стані), вона відіграє важливу біологічну роль. Від концентрації йонів Гідрогену, яку оцінюють за водневим показником (рН - значення негативного десяткового логарифма концентрації йонів Н+), залежать структурні особливості та активність макромолекул тощо. Нейтральній реакції розчину відповідає рН 7,0. Якщо його значення нижче -реакція розчину кисла, вище - лужна. У різних частинах організму і навіть однієї клітини можна спостерігати різні значення водневого показника. Це важливо для здійснення процесів обміну речовин, оскільки одні ферменти активні в лужному середовищі, інші - у кислому. Наприклад, в інфузорії-туфельки травні вакуолі періодично «подорожують» по клітині, опиняючись то в кислому, то в лужному середовищі. При цьому послідовно активні то одні травні ферменти, то інші, що сприяє кращому перетравленню поживних речовин. Пригадайте; у людини та ссавців ферменти шлункового соку активні в кислому середовищі, а підшлункового - у лужному.
Водні розчини, здатні протистояти зміні їхнього показника рН при додаванні певної кількості кислоти або лугу, називають буферними системами. Вони складаються зі слабкої кислоти (донора Н+) і основи (акцептора Н+), здатних відповідно зв'язувати йони гідроксилу (ОН-) та Гідрогену (Н+), завдяки чому рН усередині клітини майже не змінюється.
Вода визначає фізичні властивості клітин - об'єм і внутрішньоклітинний тиск (тургор). Порівняно з іншими рідинами в неї відносно високі температури кипіння та плавлення, що зумовлено водневими зв'язками між молекулами води.
Вода - значно кращий розчинник, ніж більшість інших відомих рідин. Тому всі речовини поділяють на такі, що добре розчиняються у воді (гідрофільні) та нерозчинні (гідрофобні).
До гідрофільних сполук належить багато кристалічних солей, наприклад кухонна сіль (]аСІ), глюкоза, фруктоза, тростинний цукор тощо. Гідрофільні сполуки містять полярні (частково заряджені) групи, здатні взаємодіяти з молекулами води або іонізуватися (утворювати заряджені йони з нейтральних частин своєї молекули). Це, наприклад, амінокислоти, які містять карбоксильні (-СООН) та амінні (-]]Н2) групи.
Гідрофобні речовини (майже всі ліпіди, деякі білки) містять неполярні групи, які не взаємодіють з молекулами води. Вони розчиняються переважно в неполярних органічних розчинниках (хлороформ, бензол).
Існують й амфіфільні речовини, наприклад фосфоліпіди (сполуки ліпідів із залишками ортофосфатної кислоти), ліпопротеїди (сполуки ліпідів з білками), багато білків. Одна частина молекули цих сполук виявляє гідрофільні властивості, інша - гідрофобні.
Коли певна сполука переходить у розчин, її молекули набувають здатності до руху і їхня реакційна здатність зростає. Саме тому більша частина біохімічних реакцій відбувається у водних розчинах.
Вода як універсальний розчинник відіграє важливу роль в обміні речовин.
Проникнення речовин у клітину та виведення з неї продуктів життєдіяльності можливе здебільшого лише в розчиненому стані.
Вода як універсальний розчинник відіграє надзвичайно важливу роль у транспорті різних сполук у живих організмах. Розчини органічних і неорганічних речовин рослини транспортують по провідних тканинах або міжклітинниках. У тварин таку функцію виконують кров, лімфа, тканинна рідина тощо.
Вода бере участь у складних біохімічних перетвореннях. Наприклад, за участі води відбуваються реакції гідролізу - розщеплення органічних сполук з приєднанням до місць розривів йонів Н+ та ОН- .
З водою пов'язана здатність організмів регулювати свій тепловий режим. Їй властива висока теплоємність, яка зумовлює здатність поглинати тепло за незначних змін власної температури. Теплоємність - кількість тепла, необхідного для нагрівання тіла або середовища на 1 °С. Завдяки цьому вода запобігає різким змінам температури в клітинах та організмі в цілому за різких її коливань у навколишньому середовищі. Оскільки на випаровування води витрачається багато теплоти, організми в такий спосіб захищають себе від перегрівання (наприклад, транспірація у рослин, потовиділення у ссавців, випаровування вологи зі слизових оболонок тварин).
Завдяки високій теплопровідності вода забезпечує рівномірний розподіл теплоти між тканинами та органами організму. Наприклад, завдяки циркуляції рідин внутрішнього середовища у тварин або руху розчинів по тілу рослини.
Водні розчини певних сполук слугують мастилом, яке захищає поверхні, що постійно зазнають тертя. Наприклад, рідина, яка заповнює порожнину суглобів, полегшує ковзання суглобових поверхонь, зменшуючи тертя між ними. Вона також живить хрящ, що вкриває суглобові поверхні кісток.
Кожному виду організмів притаманний водний баланс - певне співвідношення між надходженням води та її витрачанням. Якщо витрати води перевищують її надходження до організму, спостерігають водний дефіцит, що негативно впливає на різні процеси життєдіяльності (у рослин - фотосинтезу, транспірації, у рослин і тварин - терморегуляції, перебігу біохімічних процесів тощо). Тому підтримання водного балансу - одна з умов нормального функціонування будь-якого організму.
Водний баланс людини.
Вміст води в організмі людини становить близько 65 %. Тобто, якщо маса людини становить 60 кг, то з них 39 кг припадає на воду. Слід зазначити, що вміст води залежить і від віку: у новонароджених він становить близько 75-80 %, у період завершення росту -65-70 %, а в людей похилого віку - лише 55-60 %. Між різними органами і тканинами людини вода розподілена нерівномірно: найбільше її в крові та нирках - 82-83 %, головному мозку - до 80 %, печінці - 75 %, м'язах -70-76 %, натомість у жировій тканині - близько 30 %, кістках - близько 20 %.
Оскільки організм людини щоденно витрачає приблизно 2-2,5 л води (вона виводиться з неперетравленими рештками їжі, сечею, потом, випаровується з поверхні слизових оболонок ротової порожнини та дихальних шляхів), то така сама її кількість має постійно надходити туди. Шляхи надходження води до організму різні. Крім того, близько 1 л води потрапляє з продуктами харчування, ще майже 300 мл води утворюється внаслідок окиснення жирів, білків і вуглеводів (так звана метаболічна вода).
Кількість спожитої за добу води залежить від умов, у яких перебуває людина. Так, у спекотну погоду або під час здійснення важкої фізичної праці витрати води зростають через посилене потовиділення та значне випаровування через слизові оболонки. Зневоднення організму (дегідратація) можливе і внаслідок порушень роботи кишечнику (сильні проноси), значних крововтрат тощо. За таких умов споживання води має збільшитися до 4-7 л на добу. Унаслідок зневоднення уповільнюються процеси травлення та всмоктування поживних речовин, порушуються процеси теплорегуляції; гусне кров, порушується її транспортна функція, у судинах можуть виникати згустки (тромби). Втрата понад 20 % води - смертельно небезпечна для людини.
Людина, яка виконує важку фізичну працю за умов підвищеної температури (наприклад, у доменному цеху), втрачає за годину лише внаслідок посиленого потовиділення до 1,6 л води! Тож добова потреба у воді в неї може зростати до 20 л за добу.
Першим сигналом недостатнього вмісту води в організмі є відчуття спраги, яке виникає при збудженні відповідного центру в гіпоталамусі (структура проміжного мозку). Його рецептори збуджуються як унаслідок зростання концентрації солей в рідинах організму, так і в разі підвищення концентрації йонів Натрію. Ці подразники сприймають різні групи рецепторів. Відчуття спраги виникає, якщо організм людини втрачає близько 1 % вологи свого тіла, і зникає після споживання певної кількості води, в середньому 0,25-0,5 л.
Отже, основні свої потреби у воді людина задовольняє за рахунок питної води. Тому розглянемо вимоги до її якості.
Питна вода та вимоги до її якості.
В Україні вимоги до якості питної води визначені Державним стандартом. Згідно з ним питна вода має бути епідеміологічно безпечною та нешкідливою за хімічним складом. Безпеку води в епідеміологічному відношенні визначають як загальною кількістю мікроорганізмів (не більше 100 в 1 см3 води), так і за кількістю клітин кишкової палички (не більше 3 в 1 дм3 води). Питна вода не повинна містити водні організми, помітні неозброєним оком, та плівку на поверхні.
Основними забруднювачами водних об'єктів у нашій країні є промисловість (понад 55 % від загального скиду) та житлово-комунальне господарство (понад 40 %). Небезпечне забруднення водойм радіонуклідами. Стічні води з високою радіоактивністю (100 і більше Кюрі1 на 1 л води) мають бути поховані в підземних безстічних басейнах або резервуарах.
Вам уже відомо, що в річках, озерах та інших водоймах відбуваються природні процеси самоочищення. У них беруть участь різноманітні організми: бактерії, водорості, одноклітинні тварини, губки, двостулкові молюски тощо. Але ці процеси тривають досить повільно, тому за інтенсивного забруднення неочищеними побутовими та промисловими стоками водні екосистеми нездатні самостійно очиститися.
Методи очищення стічних вод поділяють на механічні, фізико-хімічні та біологічні (мал. 6.4). Механічні методи полягають в очищенні стічних вод від завислих у них частинок відстоюванням і фільтрацією. Ці методи дають змогу видаляти з побутових стічних вод до 2/3 нерозчинних домішок, а з промислових - до 9/10.
За допомогою різноманітних фізико-хімічних методів зі стічної води видаляють розчинні неорганічні та органічні домішки, а також завислі в ній найдрібніші часточки.
Завершальним етапом очищення стічних вод є застосування біологічних методів з використанням штучно створених ланцюгів живлення, до яких входять певні види бактерій, одноклітинних і багатоклітинних тварин.
Сира вода з природних водойм, а також недостатньо очищена питна вода може стати джерелом збудників різноманітних захворювань: дизентерії, холери, черевного тифу (сальмонельозу), глистних захворювань тощо. Тому перед споживанням воду з колодязів, струмків, бюветів слід добре прокип'ятити, а водопровідну - профільтрувати через спеціальні очисні побутові фільтри.
Для обмеження втрат і збереження якості прісної води потрібні такі заходи:
- зменшення витрат води для забезпечення роботи промисловості, транспорту та об'єктів сільського господарства;
- зменшення витрат прісної води для побутових потреб1;

- охорона малих річок, які відіграють важливу роль у загальному водному балансі планети, зокрема живлять великі річки, від них залежить рівень підземних вод;
- створення умов для самоочищення водойм;
- проведення лісоохоронних заходів, оскільки внаслідок знищення лісів часто міліють річки та інші водойми;
- упровадження ефективних методів очищення стічних вод, здійснення постійного контролю за санітарним станом водойм і якістю питної води;
- створення замкнених систем водопостачання промислових, аграрних та енергетичних об'єктів.
- постійний контроль за станом джерел питної води.
Ключові терміни та поняття.
Гідрофільні, гідрофобні та амфіфільні сполуки, гідроліз, водний баланс.
Уміст води в організмах становить 60-70 %.
Вода утворює основу внутрішнього середовища живих організмів, у якому відбуваються процеси обміну речовин і перетворення енергії. Вода бере безпосередню участь у реакціях розщеплення органічних сполук.
Водний баланс - це певне співвідношення між надходженням і витрачанням води живою системою.
Вода визначає фізичні властивості клітин - їхній об'єм і внутрішньоклітинний тиск (тургор).
Вода - універсальний розчинник. Речовини, здатні добре розчинятися у воді, називають гідрофільними (полярними), нерозчинні - гідрофобними (неполярними).
Вода відіграє надзвичайно важливу роль у транспорті різних сполук у живих організмах. Вона бере участь у складних біохімічних реакціях і процесах теплорегуляції організмів. Основні свої потреби людина задовольняє за рахунок питної води певних стандартів якості. Перед споживанням вода має бути очищена. Методи очищення стічних вод поділяють на механічні, фізико-хімічні та біологічні.
П.Г. Балан, Ю.Г. Вервес, В.П. Поліщук. Біологія, 10 клас
Вислано читачами інтернет-сайту.
Підручники скачати безкоштовно, онлайн уроки, реферати з біології, домашнє завдання запитання та відповіді
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|
















