|
|
|
| Строка 1: |
Строка 1: |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Кислородные соединения азота<metakeywords>химия, 9 класс, класс, урок химии, на тему, урок на тему, урок для 9 класса, Кислородные соединения азота, соединения азота</metakeywords>''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Кислородные соединения азота<metakeywords>химия, 9 класс, класс, урок химии, на тему, урок на тему, урок для 9 класса, Кислородные соединения азота, соединения азота</metakeywords>''' |
| | | | |
| - | <u>''Оксиды.''</u> Азот образует пять оксидов со степенями окисления +1, +2, +3, +4, +5.<br><br>Оксиды N20 и N0 несолеобразующие (что это означает?), а остальные оксиды — кислотные: N2O3 соответствует азотистая кислота НN02, а N205 — азотная кислота НNO3. Оксид азота(IV) N02, при растворении в воде образует одновременно две кислоты — HNO2 и НNO3.<br><br>Если же он растворяется в воде в присутствии избытка кислорода, получается только азотная кислота<br><br>4N02 + 02 + 2Н20 = 4НNO3<br><br>Оксид азота(IV) NO2 — бурый, очень ядовитый газ. Он легко получается при окислении кислородом воздуха бесцветного несолеобразующего оксида азота(П):<br><br>2NO + 02 = 2NO2<br><br>Азотная кислота НN03 — бесцветная жидкость, которая «дымится» на воздухе. При хранении на свету концентрированная азотная кислота желтеет, так как частично разлагается с образованием бурого газа N02.<br><br>Азотная кислота проявляет все типичные свойства сильных кислот: взаимодействует с оксидами и гидроксидами металлов, с солями. Но вот с металлами она ведет себя по-особому — ни один из металлов не вытесняет из азотной кислоты водород, независимо от ее концентрации (для серной кислоты такое поведение характерно только в ее концентрированном состоянии). Это объясняется тем, что НNO3 является сильным окислителем, в ней азот имеет максимальную степень окисления +5. Именно он и будет восстанавливаться при взаимодействии с металлами.<br><br>Продукт восстановления зависит от положения металла в ряду напряжений, от концентрации кислоты и условий проведения реакции. Например, при взаимодействии с медью концентрированная азотная кислота восстанавливается до оксида азота(IV):<br><br>Сu + 4НN03(конц) = Сu(NO3)2 + 2NO2 + 2Н20<br><br>а разбавленная — до оксида азота(ПII):<br><br>ЗСu + 8HN03(разб) = ЗСu(HNО3)2 + 2NO + 4Н20<br><br>Железо и алюминий при действии концентрированной HN03 покрывается прочной оксидной пленкой, предохраняющей металл от дальнейшего окисления, т. е. кислота пассивирует их. Поэтому азотную кислоту, как и серную, можно перевозить в стальных и алюминиевых цистернах.<br><br>Азотная кислота окисляет многие органические вещества, обесцвечивает красители. При этом обычно выделяется много теплоты и вещество воспламеняется. Так, если к азотной кислоте прилить каплю скипидара, то происходит яркая вспышка, а тлеющая лучинка в ней загорается (рис. 33).<br><br>Азотная кислота широко применяется в химической промышленности для производства азотных удобрений, пластмасс, искусственных волокон, органических красителей и лаков, лекарств и взрывчатых веществ.<br><br>Соли азотной кислоты — нитраты получают при действии кислоты на металлы, их оксиды и гидроксиды. Нитраты натрия, калия, кальция и аммония называются селитрами: NaNO3 — натриевая селитра, КN03 — калийная селитра, Са(NO3)2 — кальциевая селитра, NН4О3 — аммиачная селитра. Все они применяются как азотные удобрения.<br>[[Image:ahim09-65.jpg]] | + | <u>''Оксиды.''</u> Азот образует пять [[Оксиды,_их_классификация_и_свойства|оксидов]] со степенями окисления +1, +2, +3, +4, +5.<br><br>Оксиды N20 и N0 несолеобразующие (что это означает?), а остальные оксиды — кислотные: N2O3 соответствует азотистая кислота НN02, а N205 — азотная кислота НNO3. Оксид азота(IV) N02, при растворении в воде образует одновременно две кислоты — HNO2 и НNO3.<br><br>Если же он растворяется в воде в присутствии избытка кислорода, получается только азотная кислота<br><br>4N02 + 02 + 2Н20 = 4НNO3<br><br>Оксид азота(IV) NO2 — бурый, очень ядовитый газ. Он легко получается при окислении кислородом воздуха бесцветного несолеобразующего оксида азота(П):<br><br>2NO + 02 = 2NO2<br><br>[[Азотные,_калийные_и_фосфорные_удобрения|Азотная]] кислота НN03 — бесцветная жидкость, которая «дымится» на воздухе. При хранении на свету концентрированная азотная кислота желтеет, так как частично разлагается с образованием бурого газа N02.<br><br>Азотная кислота проявляет все типичные свойства сильных кислот: взаимодействует с оксидами и гидроксидами металлов, с солями. Но вот с металлами она ведет себя по-особому — ни один из металлов не вытесняет из азотной кислоты водород, независимо от ее концентрации (для серной кислоты такое поведение характерно только в ее концентрированном состоянии). Это объясняется тем, что НNO3 является сильным окислителем, в ней азот имеет максимальную степень окисления +5. Именно он и будет восстанавливаться при взаимодействии с металлами.<br><br>Продукт восстановления зависит от положения [[Рубка_металла|металла]] в ряду напряжений, от концентрации кислоты и условий проведения реакции. Например, при взаимодействии с медью концентрированная азотная кислота восстанавливается до оксида азота(IV):<br><br>Сu + 4НN03(конц) = Сu(NO3)2 + 2NO2 + 2Н20<br><br>а разбавленная — до оксида азота(ПII):<br><br>ЗСu + 8HN03(разб) = ЗСu(HNО3)2 + 2NO + 4Н20<br><br>Железо и алюминий при действии концентрированной HN03 покрывается прочной оксидной пленкой, предохраняющей металл от дальнейшего окисления, т. е. кислота пассивирует их. Поэтому азотную кислоту, как и серную, можно перевозить в стальных и [[Конспект_уроку_з_теми:_Алюміній_як_хімічний_елемент_і_проста_речовина._Фізичні_та_хімічні_властивості_алюмінію|алюминиевых]] цистернах.<br><br>Азотная кислота окисляет многие органические вещества, обесцвечивает красители. При этом обычно выделяется много теплоты и вещество воспламеняется. Так, если к азотной кислоте прилить каплю скипидара, то происходит яркая вспышка, а тлеющая лучинка в ней загорается (рис. 33).<br><br>Азотная кислота широко применяется в химической промышленности для производства азотных удобрений, пластмасс, искусственных волокон, органических красителей и лаков, лекарств и взрывчатых веществ.<br><br>Соли азотной кислоты — нитраты получают при действии кислоты на металлы, их оксиды и гидроксиды. Нитраты натрия, калия, кальция и аммония называются селитрами: NaNO3 — натриевая селитра, КN03 — калийная селитра, Са(NO3)2 — кальциевая селитра, NН4О3 — аммиачная селитра. Все они применяются как азотные удобрения.<br>[[Image:Ahim09-65.jpg|химия 9 класс]] |
| | | | |
| - | <br>Калийная селитра используется также при изготовлении черного пороха, а из аммиачной селитры, как вы уже знаете, готовят взрывчатое вещество аммонал. Нитрат серебра, или ляпис, AgNOз применяется в медицине для прижигания ран, язв и др.<br><br>Почти все нитраты хорошо растворимы в воде. При нагревании они разлагаются с выделением кислорода. | + | <br>Калийная селитра используется также при изготовлении черного пороха, а из аммиачной селитры, как вы уже знаете, готовят взрывчатое вещество аммонал. Нитрат серебра, или ляпис, AgNOз применяется в медицине для прижигания ран, язв и др.<br><br>Почти все нитраты хорошо растворимы в [[Тема_40._Вода.|воде]]. При нагревании они разлагаются с выделением кислорода. |
| | | | |
| | <br>Поэтому если в расплавленную в пробирке калийную селитру бросить кусочек раскаленного древесного угля, то он энергично сгорит, взаимодействуя с выделяющимся из селитры кислородом (рис. 34).<br><br>1. Несолеобразующие и кислотные оксиды азота.<br><br>2. Оксид азота(IV). | | <br>Поэтому если в расплавленную в пробирке калийную селитру бросить кусочек раскаленного древесного угля, то он энергично сгорит, взаимодействуя с выделяющимся из селитры кислородом (рис. 34).<br><br>1. Несолеобразующие и кислотные оксиды азота.<br><br>2. Оксид азота(IV). |
| Строка 13: |
Строка 13: |
| | 5. Применение азотной кислоты. | | 5. Применение азотной кислоты. |
| | | | |
| - | 6. Нитраты, селитры.<br><br>Почему азотная кислота не образует кислых солей?<br><br>Напишите молекулярные и ионные уравнения реакций азотной кислоты с гидроксидом меди(II), оксидом железа(III) и карбонатом натрия.<br><br>Большинство солей азотной кислоты растворимы в воде, тем не менее предложите уравнение реакции НNO3 с солью, в результате которой образуется осадок. Напишите ионное уравнение этой реакции.<br><br>Рассмотрите уравнения реакций разбавленной и концентрированной азотной кислоты с медью с точки зрения процессов окисления-восстановления.<br><br>Предложите две цепочки превращений, приводящих к получению азотной кислоты, исходя из азота и аммиака. Опишите окислительно-восстановительные реакции, используя метод электронного баланса.<br><br>Сколько килограммов 68%-ной азотной кислоты можно получить из 134,4 м3 оксида азота(IV)?<br><br>При прокаливании 340 г натриевой селитры получили 33,6 л кислорода. Какова массовая доля примесей в селитре?<br> | + | 6. Нитраты, селитры.<br><br>Почему азотная кислота не образует кислых солей?<br><br>Напишите молекулярные и ионные уравнения реакций азотной кислоты с гидроксидом [[Век_медный,_бронзовый,_железный|меди]](II), оксидом железа(III) и карбонатом натрия.<br><br>Большинство солей азотной кислоты растворимы в воде, тем не менее предложите уравнение реакции НNO3 с солью, в результате которой образуется осадок. Напишите ионное уравнение этой реакции.<br><br>Рассмотрите уравнения реакций разбавленной и концентрированной азотной кислоты с медью с точки зрения процессов окисления-восстановления.<br><br>Предложите две цепочки превращений, приводящих к получению азотной кислоты, исходя из азота и аммиака. Опишите окислительно-восстановительные реакции, используя метод электронного баланса.<br><br>Сколько килограммов 68%-ной азотной [[Карбоновые_кислоты_(Химия_10_класс)|кислоты]] можно получить из 134,4 м3 оксида азота(IV)?<br><br>При прокаливании 340 г натриевой селитры получили 33,6 л кислорода. Какова массовая доля примесей в селитре?<br> |
| | | | |
| - | <br> <sub>схемы и таблицы к [[Химия|уроку химии]], презентация урока [[Химия_9_класс|9 класса]], [[Гипермаркет_знаний_-_первый_в_мире!|интерактивные технологии]]</sub> | + | <br> <sub>схемы и таблицы к [[Химия|уроку химии]], презентация урока [[Химия 9 класс|9 класса]], [[Гипермаркет знаний - первый в мире!|интерактивные технологии]]</sub> |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Текущая версия на 12:38, 1 июля 2012
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Кислородные соединения азота
Оксиды. Азот образует пять оксидов со степенями окисления +1, +2, +3, +4, +5.
Оксиды N20 и N0 несолеобразующие (что это означает?), а остальные оксиды — кислотные: N2O3 соответствует азотистая кислота НN02, а N205 — азотная кислота НNO3. Оксид азота(IV) N02, при растворении в воде образует одновременно две кислоты — HNO2 и НNO3.
Если же он растворяется в воде в присутствии избытка кислорода, получается только азотная кислота
4N02 + 02 + 2Н20 = 4НNO3
Оксид азота(IV) NO2 — бурый, очень ядовитый газ. Он легко получается при окислении кислородом воздуха бесцветного несолеобразующего оксида азота(П):
2NO + 02 = 2NO2
Азотная кислота НN03 — бесцветная жидкость, которая «дымится» на воздухе. При хранении на свету концентрированная азотная кислота желтеет, так как частично разлагается с образованием бурого газа N02.
Азотная кислота проявляет все типичные свойства сильных кислот: взаимодействует с оксидами и гидроксидами металлов, с солями. Но вот с металлами она ведет себя по-особому — ни один из металлов не вытесняет из азотной кислоты водород, независимо от ее концентрации (для серной кислоты такое поведение характерно только в ее концентрированном состоянии). Это объясняется тем, что НNO3 является сильным окислителем, в ней азот имеет максимальную степень окисления +5. Именно он и будет восстанавливаться при взаимодействии с металлами.
Продукт восстановления зависит от положения металла в ряду напряжений, от концентрации кислоты и условий проведения реакции. Например, при взаимодействии с медью концентрированная азотная кислота восстанавливается до оксида азота(IV):
Сu + 4НN03(конц) = Сu(NO3)2 + 2NO2 + 2Н20
а разбавленная — до оксида азота(ПII):
ЗСu + 8HN03(разб) = ЗСu(HNО3)2 + 2NO + 4Н20
Железо и алюминий при действии концентрированной HN03 покрывается прочной оксидной пленкой, предохраняющей металл от дальнейшего окисления, т. е. кислота пассивирует их. Поэтому азотную кислоту, как и серную, можно перевозить в стальных и алюминиевых цистернах.
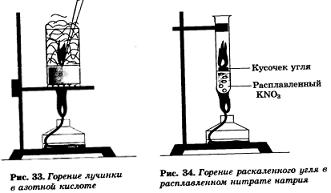
Азотная кислота окисляет многие органические вещества, обесцвечивает красители. При этом обычно выделяется много теплоты и вещество воспламеняется. Так, если к азотной кислоте прилить каплю скипидара, то происходит яркая вспышка, а тлеющая лучинка в ней загорается (рис. 33).
Азотная кислота широко применяется в химической промышленности для производства азотных удобрений, пластмасс, искусственных волокон, органических красителей и лаков, лекарств и взрывчатых веществ.
Соли азотной кислоты — нитраты получают при действии кислоты на металлы, их оксиды и гидроксиды. Нитраты натрия, калия, кальция и аммония называются селитрами: NaNO3 — натриевая селитра, КN03 — калийная селитра, Са(NO3)2 — кальциевая селитра, NН4О3 — аммиачная селитра. Все они применяются как азотные удобрения.
Калийная селитра используется также при изготовлении черного пороха, а из аммиачной селитры, как вы уже знаете, готовят взрывчатое вещество аммонал. Нитрат серебра, или ляпис, AgNOз применяется в медицине для прижигания ран, язв и др.
Почти все нитраты хорошо растворимы в воде. При нагревании они разлагаются с выделением кислорода.
Поэтому если в расплавленную в пробирке калийную селитру бросить кусочек раскаленного древесного угля, то он энергично сгорит, взаимодействуя с выделяющимся из селитры кислородом (рис. 34).
1. Несолеобразующие и кислотные оксиды азота.
2. Оксид азота(IV).
3. Свойства азотной кислоты как электролита и как окислителя.
4. Взаимодействие концентрированной и разбавленной азотной кислоты с медью.
5. Применение азотной кислоты.
6. Нитраты, селитры.
Почему азотная кислота не образует кислых солей?
Напишите молекулярные и ионные уравнения реакций азотной кислоты с гидроксидом меди(II), оксидом железа(III) и карбонатом натрия.
Большинство солей азотной кислоты растворимы в воде, тем не менее предложите уравнение реакции НNO3 с солью, в результате которой образуется осадок. Напишите ионное уравнение этой реакции.
Рассмотрите уравнения реакций разбавленной и концентрированной азотной кислоты с медью с точки зрения процессов окисления-восстановления.
Предложите две цепочки превращений, приводящих к получению азотной кислоты, исходя из азота и аммиака. Опишите окислительно-восстановительные реакции, используя метод электронного баланса.
Сколько килограммов 68%-ной азотной кислоты можно получить из 134,4 м3 оксида азота(IV)?
При прокаливании 340 г натриевой селитры получили 33,6 л кислорода. Какова массовая доля примесей в селитре?
схемы и таблицы к уроку химии, презентация урока 9 класса, интерактивные технологии
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|











