|
|
|
| Строка 64: |
Строка 64: |
| | | | |
| | 1. Метод С.В.Лебедева. С его помощью в промышленности было налажено производство бутадиена из этилового спирта. В основе этого метода, который разработал Лебедев, лежит реакция:<br> | | 1. Метод С.В.Лебедева. С его помощью в промышленности было налажено производство бутадиена из этилового спирта. В основе этого метода, который разработал Лебедев, лежит реакция:<br> |
| - | 425 °С, Аl2O3, ZnO
| + | <br> <sub>425 °С, Аl2O3, ZnO</sub><br>2СН3—СН2—ОН -----------------> СН9=СН-СН=СН9 + 2Н2O + Н2<br><br> |
| - | 2СН3—СН2—ОН -----------------> СН9=СН-СН=СН9 + 2Н2O + Н2 | + | |
| | | | |
| | <br>[[Image:HimR10-27.jpg|лебедев]]<br> | | <br>[[Image:HimR10-27.jpg|лебедев]]<br> |
| Строка 151: |
Строка 150: |
| | [[Image:10kl_Alkadieny0001.jpg|500x500px|акдиены]] | | [[Image:10kl_Alkadieny0001.jpg|500x500px|акдиены]] |
| | <br> | | <br> |
| - |
| |
| - |
| |
| - | В зависимости от взаимного расположения двойных связей различают ''три вида диенов:''<br><br>• алкадиены с кумулированным расположением двойных связей<br><br>СН2=С=СН2<br><br>• алкадиены с сопряженными двойными связями<br><br>CH2=CH—CH=CH2<br><br>• алкадиены с изолированными двойными связями<br><br>CH2=CH—CH2—CH=CH2<br><br>Эти три вида алкадиенов существенно отличаются друг от друга по строению и свойствам. Центральный атом углерода (атом, образующий две двойные связи) в алкадиенах с кумулированными связями находится в состоянии ер-гибридизации. Он образует две Þ-связи, лежащие на одной прямой и направленные в противоположные стороны, и две я-связи, лежащие в перпендикулярных плоскостях.''п''-Связи образуются за счет негибридизованных р-орбиталей каждого атома [[Строение_атома_углерода|углерода]].<br><br>Свойства алкадиенов с изолированными двойными связями практически ничем не отличаются от свойств алкенов, разве что алкадиены вступают в соответствующие реакции в две ступени. Атомы углерода, образующие двойные связи, находятся в sр<sup>2</sup>-гибридизации.<br><br>Свойства алкадиенов с сопряженными связями весьма специфичны, так как сопряженные л-связи существенно влияют друг на друга.<br><br>р-Орбитали, образующие сопряженные ''п''-связи, фактически составляют единую систему (ее называют ''п''-системой), так как р-орбитали соседних л-связей частично перекрываются.<br><br>Длины двойных связей (1 и 3) составляют 0,137 нм (двойная связь в алкенах — 0,132 нм), а одинарной (2) — 0,146 нм (0,154 нм у алканов). Таким образом, можно считать, что кратность связей 1 и 3 несколько меньше двух, а связи 2 больше единицы.<br><br>Иногда алкадиены с сопряженными связями изображают следующим образом:<br><br>СН2—СН—СН—СН2<br><br>
| |
| - |
| |
| - | [[Image:HimR10-25.jpg|Алкадиены]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | ''Изомерия и номенклатура''<br><br>Для алкадиенов характерна как структурная изомерия, так и цис-транс-изомерия. Структурная [[Явище_ізомерії._Структурна_ізомерія,_номенклатура_насичених_вуглеводнів|изомерия]]:<br><br>• изомерия углеродного скелета:<br><br>
| |
| - |
| |
| - | [[Image:HimR10-26.jpg|Алкадиены]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Алкадиены изомерны соединениям классов алкинов и цик-лоалкенов (см. «Алкины»).<br><br>При формировании названия алкадиена указывают номера двойных связей. Главная цепь должна обязательно содержать обе кратные связи.
| |
| - |
| |
| - | <br>''Получение''<br><br>1. Метод Лебедева. В 1932 г. в нашей стране было налажено производство бутадиена из этилового спирта методом, разработанным С. В. Лебедевым. В основе метода лежит реакция<br><br> <sub>425 °С, Аl2O3, ZnO</sub><br>2СН3—СН2—ОН -----------------> СН9=СН-СН=СН9 + 2Н2O + Н2<br><br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Серге́й Васи́льевич Ле́бедев<br>
| |
| - |
| |
| - | (1874-1934)<br>
| |
| - |
| |
| - | [[Image:HimR10-27.jpg|лебедев]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Советский химик, академик. Основные научные исследования посвящены полимеризации, изомеризации и гидрогенизации непредельных углеводородов. Получил (1928) синтетический каучук полимеризацией 1,3-бутадиена под действием натрия.<br><br>
| |
| - |
| |
| - | Этиловый спирт одновременно претерпевает и дегидратацию, и дегидрирование.<br><br>2. Способ дегидрирования. Одним из самых распространенных способов получения бутадиена-1,3 является двухстадий-ное каталитическое дегидрирование ''н''-бутана:<br><br>СН3—СН2—СН2—СН3 —> CH2=CH—СН=СН2 + 2Н2<br><br>На первой стадии этого процесса образуется как бутен-1, так и бутен-2.<br><br>[[Image:HimR10-28.jpg|Алкадиены]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Не менее важное, чем бутадиен-1,3, другое соединение — изопрен (2-метилбутадиен-1,3) получают аналогичным способом — дегидрированием 2-метилбутана.<br>
| |
| - |
| |
| - | 3. Способ дегидрогалогенирования. Для получения алкадиенов можно применять стандартный способ создания кратных связей — дегидрогалогенирование, известное вам еще по теме «[[Алкены|Алкены]]».<br><br>При действии на дибромалканы спиртового раствора щелочи происходит отщепление двух молекул галогеноводорода и образование двух двойных связей:<br>[[Image:HimR10-29.jpg|Алкадиены]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Существенным является расположение галогенов в молекуле дига-логенида. Так, например, в случае 2,3-дибромбутана или 2,2-ди-бромпропана образуются соответствующие алкины (см. § 13 «Алкины»).<br><br>''Физические свойства''<br><br>В обычных условиях пропадиен-1,2, бутадиен-1,3 — газы, 2-метилбутадиен-1,3 — летучая жидкость. Алкадиены с изолированными двойными связями (простейший из них — пен-тадиен-1,4) — жидкости. Высшие диены — твердые вещества.<br><br>''Химические свойства''<br><br>Напомним, что свойства алкадиенов с изолированными двойными связями мало отличаются от свойств алкенов. Алкадиены с сопряженными связями обладают некоторыми особенностями.<br><br>1. Реакции присоединения. Алкадиены способны присоединять водород, галогены, галогеноводороды.<br><br>Особенностью присоединения к алкадиенам с сопряженными двойными связями является способность присоединять молекулы как в положения 1 и 2 (1,2-присоединение), так и в положения 1 и 4 (1,4-присоединение):<br><br> Вr Вr<br> | |<br>СН2=СН—СН=СН2 + Вг2 —> CH2—CH—CH=CH2<br> 1,2-присоединение
| |
| - |
| |
| - | <br> Вг Вг<br> | l<br>CH2=CH—СН=СН2 + Вг2 —> CH2—CH=CH—CH2<br> 1,4-присоединение<br><br>Соотношение продуктов зависит от условий и способа проведения соответствующих реакций.<br><br>2. Реакции полимеризации. Важнейшим свойством диенов является способность полимеризоваться под воздействием катионов или свободных радикалов. Полимеризация этих соединений является основой получения синтетических каучуков. Обратите внимание на то, что полимеризация сопряженных диенов протекает как 1,4-присоединение.<br><br>В этом случае двойная связь оказывается центральной в элементарном звене, а элементарное звено, в свою очередь, может принимать как цис-, так и тракс-конфигурацию:<br>[[Image:HimR10-30.jpg|Алкадиены]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Рассмотрим причины, по которым в случае алкадиенов с сопряженными двойными связями возможно 1,4-присоединение на примере реакции гидробромирования (присоединения НВr).<br><br>Эта реакция протекает по механизму электрофильного присоединения и начинается с присоединения электрофильной частицы, катиона [[Квантовые_постулаты_Бора._Модель_атома_водорода_по_Бору|водорода]], к молекуле алкадиена:<br><br>СН2=СН—СН=СН2 + H+ —> СН3—СН+—СН=СН2<br><br>Присоединение к этому карбокатиону иона Вr<sup>-</sup> приведет к продукту 1,2-присоединения:<br><br>СН3—СН+—СН=СН2 + Вr<sup>-</sup> —> СН3—СНВг—СН=СН2<br><br>
| |
| - |
| |
| - | Положительный заряд на атоме углерода означает наличие незаполненной р-орбитали, которая может перекрываться с л-связью, перетягивая к себе электронную плотность. В результате этого происходит перемещение двойной связи в центр молекулы, а положительный заряд оказывается на крайнем атоме углерода:<br><br>СН<sub>3</sub>—СН+—СН=СН<sub>2</sub> —> CH<sub>3</sub>- СН=СН—СН<sub>2</sub><sup>+</sup><br><br>Обратите внимание на то, что мы встретились со случаем, когда одна и та же частица описывается двумя различными структурами, отличающимися друг от друга распределением электронной плотности. Присоединение аниона брома ко второму карбокатиону приведет к продукту 1,4-присоединения:<br><br>СН<sub>3</sub>—СН=СН—СН+ + Вг<sup>-</sup> —> СН3—СН=СН—СН<sub>2</sub>Вr<br>''<br>Натуральный и синтетический каучуки. Резина''<br><br>До конца 1930-х гг. в промышленности использовали натуральный каучук, выделяемый из млечного сока (латекса) некоторых растений-каучуконосов. Наиболее ценным каучуконосом является гевея, растущая в [[Общая_характеристика_Латинской_Америки|Латинской Америке]]. Исследования показали, что натуральный каучук представляет собой цис-полиизопрен, т. е. полимер, элементарные звенья которого соответствуют изопрену (2-метилбутадиену-1,3) и находятся в цис-конфигурации.<br>
| |
| - |
| |
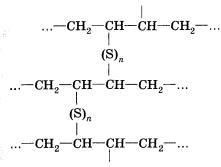
| - | Каучук, в котором все элементарные звенья находятся или в цис-, или в транс-конфигурации, называется стереорегулярным.<br><br>В середине прошлого века (Гудьир, 1839 г.) было обнаружено, что при нагревании каучука с серой (до 8%) образуется резина — эластичный материал, технические свойства которого гораздо лучше, чем у каучука. При нагревании с серой (вулканизации) происходит сшивание полимерных цепей за счет сульфидных мостиков, что приводит к увеличению прочности, устойчивости к истиранию, к действию органических растворителей и других веществ.<br><br>[[Image:HimR10-31.jpg|Алкадиены]]<br>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | В связи с бурным ростом промышленного производства в начале XX в. возросла потребность в каучуке. И это заставило химиков искать пути получения синтетического каучука. Первые попытки были неудачными, так как при полимеризации диенов образовывались нестереорегулярные цепи (т. е. цепи, в которых элементарные звенья находились как в цис-, так и в траке-конфигурации). Получаемый каучук был похож на смолу, вулканизация его давала резину очень плохого качества.<br><br>Впервые технологически удобный способ синтеза полибутадиенового каучука был разработан русским химиком С. В. Лебедевым. В его основе лежала полимеризация бутадиена-1,3 с использованием катализатора — металлического натрия.<br><br>Это позволило получить полибутадиен с хорошими технологическими свойствами. Однако этот полимер был нестерео-регулярным, и поэтому резина, полученная на его основе, была менее эластичной, чем резина природного каучука. Стерео-регулярные полимеры (в том числе и изопреновые) научились получать лишь в 50-е гг. XX в.<br><br>Современная химическая промышленность вырабатывает несколько видов синтетического каучука. В качестве мономеров используют изопрен, бутадиен, хлоропрен (2-хлорбутадиен-1,3), стирол (винилбензол) и т. д. Большое распространение получили резины, произведенные на основе сополимеров алкадиенов с сопряженными двойными связями и производных алкенов.<br>
| |
| - |
| |
| - | Такие резины характеризуются высокой морозоустойчивостью, прочностью и эластичностью (бутадиен-стирольный), масло-бензостойкостью (бутадиен-нитрильный (нитрил — СН2=СН—СH)), пониженной газопроницаемостью, устойчивостью к действию ультрафиолетового излучения, окислителей (бутилкаучук — сополимер изопрена и изобутилена).<br><br>1. Какие виды алкадиенов вы знаете? Приведите примеры.<br><br>2. Напишите формулы изомеров углеводорода С6Н10, относящегося к классу алкадиенов.<br><br>3. Какие виды изомерии характерны для алкадиенов с сопряженными двойными связями? Приведите примеры.<br><br>4. При взаимодействии бутадиена-1,3 с бромом возможно образование разных соединений. Что это за соединения? Напишите уравнения соответствующих реакций.<br><br>5. Расшифруйте следующую цепочку превращений. Назовите соединения А, Б, В, Г.<br>[[Image:HimR10-32.jpg|Алкадиены]]
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | 6*. При полном сжигании 0,1 моль ациклического углеводорода образуется 5,4 г воды и выделяется 8,96 л (н. у.) углекислого газа. При взаимодействии этого углеводорода с эквимолярным количеством брома при 40 °С образуется преимущественно дибромалкен симметричного строения с атомами брома на концах цепи. Определите строение исходного углеводорода.<br>
| |
| - |
| |
| - | <br> <sub>квесты по [[Химия 10 класс|химии для 10 класса]], шпаргалки [[Гипермаркет знаний - первый в мире!|для учеников]], рефераты [[Химия|по химии]]</sub>
| |
| - |
| |
| - | '''<u>Содержание урока</u>'''
| |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока '''
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии
| |
| - |
| |
| - | '''<u>Практика</u>'''
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников
| |
| - |
| |
| - | '''<u>Иллюстрации</u>'''
| |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа '''
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты
| |
| - |
| |
| - | '''<u>Дополнения</u>'''
| |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты'''
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие
| |
| - | '''<u></u>'''
| |
| - | <u>Совершенствование учебников и уроков
| |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике'''
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми
| |
| - |
| |
| - | '''<u>Только для учителей</u>'''
| |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки '''
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы
| |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения
| |
| - |
| |
| - |
| |
| - | '''<u>Интегрированные уроки</u>'''<u>
| |
| - | </u>
| |
| - |
| |
| - | <br>
| |
| - |
| |
| - | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам].
| |
| - |
| |
| - | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум].
| |
Версия 09:24, 31 августа 2015
Гипермаркет знаний>>Химия>>Химия 10 класс>> Химия: Алкадиены
Строение алкадиенов
Алкадиены — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода и соответствующие общей формуле СnН2n-2.
Строение алкадиенов
Общая характеристика алкадиенов
Алкадиены являются представителями ненасыщенных углеводородов, которые содержат в своем углеродном скелете две двойные связи, поэтому их еще называют диеновыми углеводородами.
А вот что собой представляет общая формула гомологического ряда алкадиенов:
СnН2n-2.
Но, эта формула также соответствует и гомологическому ряду алкинов, а также циклоалкенов.
О наличии двух двойных связей в молекуле нам говорит название класса, где «ди» обозначает два, а «ен» переводится, как связь, то есть двойная связь.
Классификация диенов
Также следует отметить, что в зависимости от взаимного расположения двойных связей, диены можно разделить на такие группы, как:
Первая группа
• Кумулированные диены. Это такие соединения, молекулы которых имеют две двойные связи расположены у одного и того же атома углерода (1,2-диены)
СН2=С=СН2
Вторая группа
• Сопряженные диены. К ним относятся алкадиены, в молекулах, которых имеются две двойные связи, разделенные одинарной или одной простой связью:
CH2=CH—CH=CH2
Вот какой вид иногда могут иметь алкадиены, которые имеют сопряженные связи:
СН2—СН—СН—СН2
Третья группа
• Изолированные диены. К ним относятся такие соединения, у которых молекулы имеют две двойные связи и притом эти двойные связи разделены несколькими одинарными
CH2=CH—CH2—CH=CH2
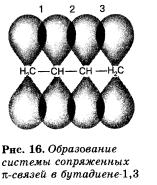
Изомерия и номенклатура
Если рассматривать изометрию алкадиенов, то здесь следует сказать, что для них характерна, как структурная изометрия, так и пространственная.
На рисунке внизу мы видим примеры структурной и пространственной изометрии:
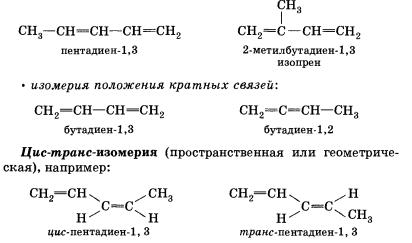
Что же касательно составления названий алкадиенов, то здесь существуют следующие правила:
• Во-первых, основная цепь в обязательном порядке должна содержать две двойные связи;
• Во-вторых, нумерацию, как правило начинают с того конца, с которого ближе расположена кратная связь;
• В-третьих, дают названия заменителям и указывают атомы углерода, от которого они отходят;
• В-четвертых, атомы углерода дают название алкадиена, как правило, от тех атомов, от которых была образована двойная связь.
Получение алкадиенов
Если рассматривать вопрос получения диенов, то, как правило, используют:
1. Метод С.В.Лебедева. С его помощью в промышленности было налажено производство бутадиена из этилового спирта. В основе этого метода, который разработал Лебедев, лежит реакция:
425 °С, Аl2O3, ZnO
2СН3—СН2—ОН -----------------> СН9=СН-СН=СН9 + 2Н2O + Н2

Сергей Васильевич Лебедев был известным химиком, который посвятил свои научные исследования полимеризации, изомеризации и гидрогенизации непредельных углеводородов. С помощью полимеризации 1,3-бутадиена под действием натрия, ему удалось получить синтетический каучук.
2. Способ дегидрирования. Одним из распространенных промышленных методов получения бутадиена-1,3 является каталитическое дегидрирование н-бутана, которые выделяют из частей нефтеперегонки:
СН3—СН2—СН2—СН3 —> CH2=CH—СН=СН2 + 2Н2
При рассмотрении этого процесса, на его первой стадии может образовываться как бутен-1, так и бутен-2.

Изопрен (2-метилбутадиен-1,3) получают методом дегидрирования 2-метилбутана.
3. Способ дегидрогалогенирования. Для получения алкадиенов можно применять стандартный лабораторный, которым является способ реакции отщепления.
При воздействии спиртового раствора щелочи на дибромалканы, мы можем наблюдать процесс отщепления двух молекул галогеноводорода и образование двух двойных связей:
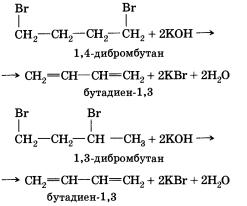
Физические свойства
Что касается физических свойств алкадиенов, то при изолированной двойной связи, они имеют такие же свойства, как и обычные алкены.
При обычных условиях, бутадиен-1,3 представляет собой легко сжижающийся газ, который имеет довольно неприятный запах. А изопрен и другие низшие диены, являются
бесцветными легкокипящими жидкостями. Что касается высших диенов, то они представлены в виде твердых веществ.
Химические свойства
Как вам уже известно, химические и физические свойства алкадиенов имеют много общего с алкенами, хотя алкадиены с сопряженными связями имеют свои нюансы и являются более активными.
1. Для алкадиенов свойственна реакции присоединения, и они способны присоединять, как водород, так и галогены, и галогеноводороды.
Главной особенность диенов является то, что они обладают способностью присоединения не только молекулы 1,2, но и продукт присоединения 1,4:
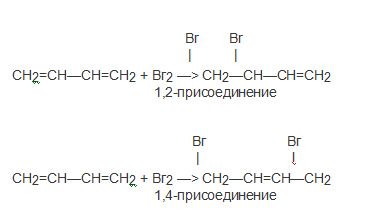
Предпочтительное протекание реакции, как правило, зависимо от условий и способа проведения.
2. Следующим химическим свойством диенов является реакции полимеризации. Она может происходить под воздействием катионов или свободных радикалов. Как правило, такая полимеризация этих соединений приводит к образованию полимеров, которые обладают свойствами, напоминающими природный каучук. Поэтому можно сказать, что основной областью применения бутадиена и изопрена, является получение синтетического каучука.

Натуральный и синтетический каучуки. Резина
Пока человек не научился производить синтетический каучук, до тех пор в промышленности использовали натуральный каучук. Получали такой каучук с помощью каучуконосных растений, методом выделения млечного сока, то есть так называемого латекса. Наиболее ценным растением по выделению природного каучука считалась произрастающая в Латинской Америке гевея.
В этой области было проведено огромное количество исследований, которые выявили, что
натуральный каучук имеет в своем составе цис-полиизопрен, то есть, это такой полимер, который по своему строению соответствует изопрену (2-метилбутадиену-1,3).
Но благодаря проведению различных опытов и исследований, американский изобретатель Чарльз Нельсон Гудьир сумел провести вулканизацию каучука. Им было обнаружено, что
что при нагревании каучука с серой в итоге получается довольно таки эластичный материал, который даже по техническим характеристикам превосходит каучук. Вот таким методом Гудьиру удалось получить резину.
Чарльз Нельсон проведя вулканизацию, заметил, что за счет сульфидных мостиков происходит сшивание полимерных цепей и в итоге увеличивается прочность и устойчивость к различным органическим веществам и растворителям.
А так как в двадцатом веке начался стремительный рост промышленности, то и потребность в каучуке также возросла. Но использование в промышленных масштабах природного каучука было не рентабельно и довольно таки дорого, то ученым пришлось искать пути получения синтетического каучука.
Но, первоначально не все так просто складывалось в этой области, и первый полученный каучук отдаленно напоминал смолу, которая к тому же, при ее вулканизации имела очень плохое качество.
Как вам уже известно, из сегодняшнего урока, синтетический каучук был получен по методу химика С.В.Лебедева только в 1932 году, тогда же его производство и приобрело промышленные масштабы.
В основе такого технологически удобного способа получения каучука, лежала полимеризация бутадиена-1,3 с использованием такого катализатора, как металлический натрий.
Благодаря этой технологии удалось получить полибутадиен, который обладал довольно неплохими технологическими свойствами. Но и здесь не все было так гладко, как хотелось, потому что, полученный полимер был нестерео-регулярным и соответственно, произведенная на его основе резина не отличалась особой эластичностью и уступала качеству резины, полученной из природного каучука.
А вот изопреновые и стерео-регулярные полимеры ученым удалось получить только в пятидесятых годах двадцатого века.
Конечно же, в настоящее время, современные технологии в химической промышленности позволяют производить не один, а несколько видов синтетического каучука. Широкое использование в качестве мономеров получили такие типы синтетических каучуков, как изопреновый, бутадиеновый, хлоропреновый, стирольный и т.д.
Также, большой популярностью пользуется резина, которая произведена на основе сополимеров алкадиенов, сочлененными двойными связями, а также производные алкенов.
Для таких видов резины характерны: хорошая эластичность, прочность и морозоустойчивость. Кроме того, эти виды резины обладают пониженной газопроницаемостью, а также устойчивы к действию ультрафиолета и различных окислителей.
Домашнее задание
Ответьте на поставленные вопросы и решите данные задания.

|




















