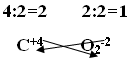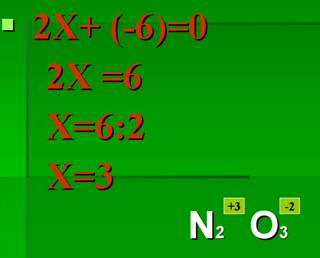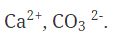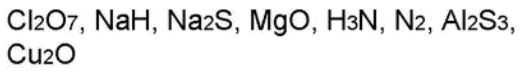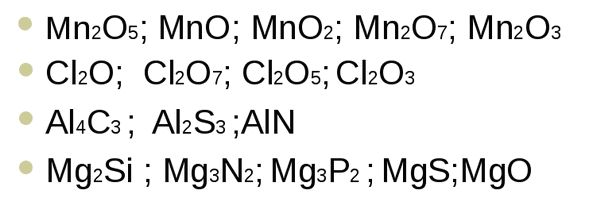|
Гипермаркет знаний>>Химия>>Химия 8 класс. Полные уроки>>Химия: Степень окисления. Полные уроки
Цели урока
Задачи урока• обучающие: продолжить изучение валентности, узнать, что такое степень окисления, рассмотреть ее виды, а также научиться правильно определять степени окисления атома в соединении; • развивающие: научить приемам обобщения и сравнения, развить навыки самостоятельной работы, способствовать развитию логического мышления; • воспитательные: сформировать чувство толерантности. Основные термины
Проверка домашнего задания1. В каких молекулах существует неполярная ковалентная связь? • А) J2 • Б)СО2 • В) О2 • Г) Н2О • Д) К2О 2)У какой молекулы при образовании ковалентно - неполярной связи образуется тройная связь? • А) СI2 • Б)N2 • В)О2 • Г)S2 3)Как называется положительно заряженные ионы? • А) катионы • Б)молекулы • В)анионы • Г) кристаллы 4)В каком ряду располагаются вещества ионного соединения? • А)СН4, NН3, Мg • Б)СI2, МgО, NаСI • В) МgF2, NаСI, СаСI2 • Г)Н2S, НСI, Н2О 5)Валентность определяются по: • А)по номеру группы • Б)по числу неспаренных электронов • В)по типу химической связи • Г) по номеру периода.
Степень окисленияСначала давайте вспомним, что такое валентность:
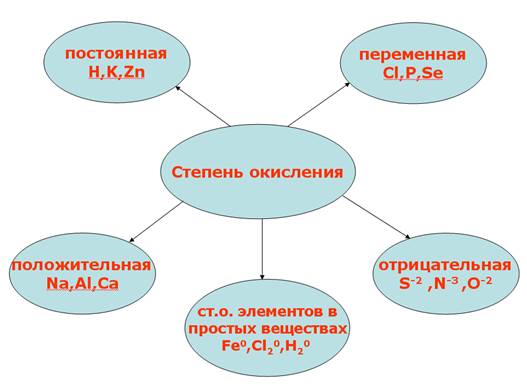
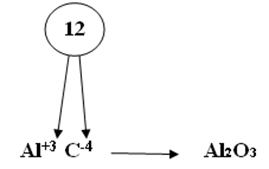
Степень окисления у молекул с различными химическими связями образуется следующим образом: 1. В соединениях с ионной связью степени окисления элементов равно зарядам ионов. Пример этого можно посмотреть на рисунке 1. Рис.1. Иллюстрация степени окисления элементов в соединениях с ионной связью. 2. В соединениях с ковалентной неполярной связью (в молекулах простых веществ) степень окисления элементов равно 0. Н20, СI20, F20, S0, AI0 3. Степень окисления у молекул с ковалентно-полярной связью определяется подобно молекулам с ионной химической связью. Степень окисления элемента – это условный заряд его атома, в молекуле, если считать, что молекула состоит из ионов. Степень окисления атома в отличие от валентности имеет знак. Она может быть положительной, отрицательной и нулевой. На рисунке 2 представлены виды степени окисления. Рис. 2. Степени окисления. Валентность обозначатся римскими цифрами сверху символа элемента, а степень окисления обозначается арабскими цифрами с зарядом над символом элемента (рисунок 3). Рис. 3. Обозначение валентности и степени окисления. У одного и того же элемента могут быть разные степени окисления. Так, на рисунке 4 представлены степени окисления серы. Рис. 4. Степени окисления серы. Теперь давайте посмотрим на определение степени окисления оксидов:
Положительная степень окисления равна числу электронов, которые отданы данным атомом. Атом может отдать все валентные электрон, соответствующие номеру группы, в котором элемент находится, при этом проявляя высшую степень окисления (исключение ОF2). Отрицательная степень окисления равна числу электронов, которые приняты данным атомом (проявляется только у неметаллов). Атомы неметаллов присоединяют то количество электронов, которое им до завершения внешнего уровня не достает, при этом проявляя отрицательную степень. На рисунке 5 представлены примеры высших и низших степеней окисления. Рис. 5. Высшие и низшие степени окисления. Значение степени окисления между высшим и низшим степенями окислений называется промежуточными (рисунок 6): Рис. 6. Промежуточная степень окисления. В соединениях с ковалентной неполярной связью (в молекулах простых веществ) степень окисления элементов равно 0: Н20, СI20, F20, S0, AI0 Для определения степени окисления атома в соединении следует учитывать ряд положений (рисунок 7). Рис. 7. Положения, которые следует учитывать для определения степени окисления атома в соединении. Очень скоро вы познакомитесь с окислительно-восстановительными реакциями:
Составление формулы веществаСуществует несколько способов составления формул вещества по степени окисления, однако сначала запомните алгоритм и правило их составления (рисунок 8): Рис.8. Алгоритм составления химических формул по степени окисления. Давайте посмотрим, как составлять формулы оксидов:
Первый способ составления формул:1. На первом месте пишется элемент с меньшей электроотрицательностью, на втором с большей электроотрицательностью. 2. Элемент, написанный на первом месте имеет положительный заряд «+», а на втором с отрицательным зарядом «-». 3. Указать для каждого элемента степень окисления. 4. Найти общее кратное значение степеней окисления. 5. Разделить наименьшее общее кратное на значение степеней окисления и полученные индексы приписать внизу справа после символа соответствующего элемента. На рисунке 9 представлен пример этого пункта: Рис. 9. Пример пункта 5 составления формул. 6. Если степень окисления четное – нечетное, то они становятся рядом с символом справа внизу крест – накрест без знака «+» и «-». Пример того, как оформлять этот пункт, представлен на рисунке 10. Рис. 10. Пример пункта 6 составления формул. 7. Если степень окисления имеет четное значение, то их сначала нужно сократить на наименьшее значение степени окисления и поставить крест – накрест без знака «+» и «-»: С+4 О-2. Пример того, как оформлять такое соединений, представлен на рисунке 11. Рис. 11. Пример пункта 7 составления формул. Второй способ составления формул:1. Обозначим степень окисления N через Х, указать степень окисления О: N2x O3-2 2. Определить сумму отрицательных зарядов, для этого степень окисления кислорода умножаем на индекс кислорода: 3• (-2)= -6 3.Чтобы молекула была электронейтральной нужно определить сумму положительных зарядов: Х2 = 2Х 4.Составить алгебраическое уравнение (рисунок 12). Рис.12. Составление алгебраического уравнения.
Выводы1. Степень окисления —условный заряд атомов химического элемента в соединении, который вычислен на основе предположения, что все соединения состоят только из ионов. Контролирующий блок1. Что такое степень окисления? Домашнее заданиеДайте названия следующих бинарных соединений: Cl2O7, Cl2O, ClO2, FeCl2, FeCl3, MnS, MnO2, MnO, MnCl4, Cu2O, Mg2Si, Na3N, FeS. Написать формулы веществ состоящих из следующих элементов: 1. Р и О Правила определения степени окисленияЗаданием данного урока является ознакомление с такой темой, как степень окисления. Давайте с вами подытожим, и еще раз вспомним определение степени окисления. Нам уже известно, что степенью окисления называют такой условный и вспомогательный заряд атомов химического элемента в соединении, который вычисляется из такого предложения, в котором все ионные и ковалентно - полярные соединения состоят только из ионов. Суждение о степени окисления различных элементов могут быть полезны: • во-первых, при компоновке классификации химических веществ; В большинстве случаев, степень окисления атомов в веществах со сложным строением вначале обозначаются знаком, затем цифрой. Обозначение цифр может быть такой: +1, +2, -2 и другими. Если гипотетически представить, что в соединении существует заряд иона, то в этом случае следует вначале указывать цифру, а потом уже знак. Приведем пример: Но для нахождения степени окисления существуют определенные правила. Давайте более подробно остановимся на этих правилах. Итак, при определении степени окисления атомов нужно придерживаться следующих правил: • Во-первых, в простых веществах степень окисления атомов равняется нулю; • Во-вторых, алгебраическая сумма степеней окисления в нейтральных молекулах также равна нулю. А вот для ионов алгебраическая сумма равняется заряду иона. • В-третьих, практически во всех соединениях водород будет иметь степень окисления, которая равняется +1, исключением являются гидриды активных металлов. В них СО будет равняться -1. • В-четвертых, если рассматривать атомы кислорода, то в его соединениях СО = -2. Тогда исключением будут OF2 и пероксиды металлов и соответственно в этом случае СО кислорода будет равно +2 и -1. • Следующим правилом будет СО щелочных металлов. Если брать элементы первой группы из главной подгруппы, то СО = +1. А вот элементы второй группы, к которым относятся щелочно-земельные металлы в соединении будут иметь степень окисления равную +2. Для алюминия СО = +3, а для фтора = -1. • Если рассматривать ковалентные соединения, то в нем более электроотрицательный атом всегда показывает степень окисления со знаком «-». А вот в соединениях с менее электроотрицательным атомом СО имеет знак «+». • Если же рассматривать простые ионные соединения, то их степень окисления будет равной и по величине и по тому знаку, который имеет его электрический заряд. А теперь более подробно рассмотрим правила для промежуточных степеней окисления: Но следует отметить, что всех этих правил следует придерживаться тогда, когда мы имеем дело с постоянной степенью окисления. В случае же, когда в химических элементах СО переменная, то она, как правило, зависит от порядка, а также от типов атомов в этом соединении. Практическое задание1. Вам даны формулы химических элементов. Определите степень окисления по этим формулам. 2. В этом задании следует определить степени окисления представленных перед вами химических элементов по формуле бинарного соединения. 3. Перед вами представлены формулы. Назовите их соединения: 4. По названию этих веществ нужно составить формулы: |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: