|
Гипермаркет знаний>>Химия>>Химия 7 класс>> Атомы. Ионы. Химические элементы. Для любознательных. Химические элементы в живой природе
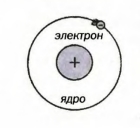
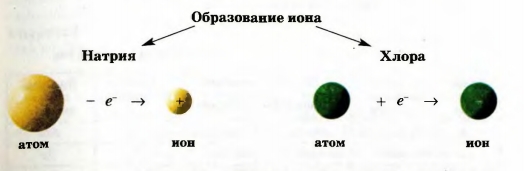
> выяснить, какое строение имеет атом; О веществах, их строении размышляли еще древнегреческие философы. Они утверждали, что вещества состоят из атомов — невидимых и неделимых частиц, а в результате их соединения образовался и существует окружающий мир. В переводе с греческого слово «атом» означает «неделимый». Доказать существование атомов удалось лишь в XIX в. с помощью сложных физических экспериментов. Одновременно было установлено, что атом не является сплошной, монолитной частицей. Он состоит из ядра и электронов. В 1911 г. была предложена одна из первых моделей атома — планетарная. Согласно этой модели, ядро находится в центре атома и занимает незначительную часть его объема, а электроны движутся вокруг ядра по определенным орбитам, как планеты — вокруг Солнца (рис. 32). Электрон в тысячи раз меньше атомного ядра. Это отрицательно заряженная частица. Ее заряд — наименьший из существующих в природе. Поэтому величину заряда электрона физики приняли за единицу измерения зарядов мельчайших частиц (кроме электронов, существуют и другие частицы). Таким образом, заряд электрона равен - 1 . Эту частицу обозначают так: Ядро атома заряжено положительно. Заряд ядра и суммарный заряд всех электронов атома одинаковы по величине, но противоположны по знаку. Поэтому атом электронейтралъный. Если заряд ядра атома составляет +1, то в таком атоме находится один электрон, если +2 — два электрона и т. д. Атом в определенных условиях может потерять либо присоединить один или несколько электронов. При этом он становится положительно или отрицательно заряженной частицей — ионом1. Ион — заряженная частица, образовавшаяся в результате потери атомом или присоединения к нему одного или нескольких электронов. 1 Слово «ион» в переводе с греческого означает «идущий». В отличие от электронейтрального атома ион способен перемещаться в эл ектри ч еском поле. Если атом теряет один электрон, то образуется ион с зарядом +1, а если присоединяет электрон, то заряд иона будет равен - I (схема 5). В случае потери атомом или присоединения к нему двух Атомов во Вселенной — бесконечное множество. Их различают по зарядам ядер. Вид атомов с определенным зарядом ядра называют химическим элементом. Атомы с зарядом ядра +1 принадлежат одному химическому элементу, с зарядом +2 — другому элементу и т. д. Понятие «химический элемент» используют для классификации атомов. С аналогичной целью, например, введены сорта фруктов, овощей, цветов и т. п. Следует помнить: химический элемент — не частица и не вещество (так же как название сорта яблок — это не яблоко). Он не имеет агрегатного состояния, плотности, температуры плавления, других физических свойств. Сейчас известны 115 химических элементов. Заряды ядер их атомов составляют от +1 до +112, а также +114, +116 и +118. Почти 90 элементов существуют в природе, а остальные (как правило, с наибольшими зарядами атомных ядер) — искусственные элементы. Их получают ученые на уникальном исследовательском оборудовании. Ядра атомов искусственных элементов неустойчивы и быстро распадаются.
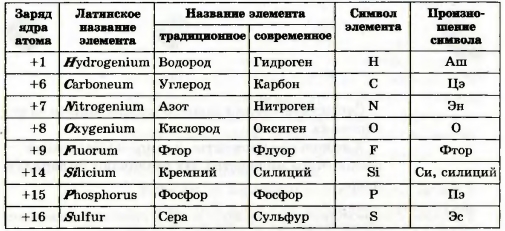
Названия химических элементов, атомов и ионов. У каждого химического элемента есть название. Современные названия элементов происходят от латинских названий (табл. I). Их всегда пишут с большой буквы. Названия элементов используют и для соответствующих частиц: атом Гидрогена (водорода), ион Гидрогена (водорода). С названиями ионов, образовавшихся из нескольких атомов, вы ознакомитесь позже. Названия химических элементов имеют разное происхождение. Одни связаны с названиями или свойствами (цветом, запахом) веществ, другие — с названиями планет, стран и т. п. Есть элементы, названные в честь выдающихся ученых. Происхождение некоторых названий неизвестно, поскольку они возникли очень давно. Современное название одного из элементов — Меркурий. Оно отличается от латинского названия (Hydrargyrum), но близкое к английскому (Mercury) и французкому (Mercure). ► Что вы думаете о происхождении названий таких элементов: Европий, Франций, Нептуний, Прометий, Менделевий? Символы элементов во всех странах одни и те же. Каждый элемент, кроме названия, имеет еще и сокращенное обозначение — символ, или знак. В наше время используют символы элементов, предложенные почти 200 лет назад известным шведским химиком Й. Я. Берцелиусом (1779—1848). Они состоят из одной латинской буквы (первой в латинских названиях элементов) или двух1. В таблице I такие буквы выделены в названиях элементов курсивом.
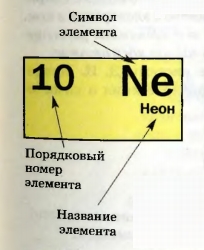
В некоторых случаях используют общее обозначение химического элемента — E. Символы и названия химических элементов содержатся в периодической системе Д. И. Менделеева. В 1869 г. русский химик Дмитрий Иванович Менделеев предложил таблицу, в которой разместил известные к тому времени 63 элемента. Эту таблицу назвали периодической системой химических элементов. В периодической системе есть горизонтальные строки, которые называют периодами, и вертикальные столбцы — группы. Пересекаясь, они образуют клетки, в которых содержится важнейшая информация о химических элементах. Каждая клетка пронумерована. В ней записан символ элемента, а под ним — название (рис. 33). 1 Символы четырех элементов, открытых в последнее время, состоят из трex букв. Номер клетки называют порядковым номером размещенного в ней элемента. Его общее обозначение — Z. Выражение «порядковый номер элемента Неона — 10» сокращенно записывают так: Z(Ne) = 10. Порядковый номер элемента совпадает с зарядом ядра его атома и количеством электронов в нем. В периодической системе все элементы размещены в порядке возрастания заряда ядер атомов. Итак, из периодической системы Д. И. Менделеева можно получить такие сведения о химическом элементе: • символ; ► Найдите в периодической системе элемент с порядковым номером 5 и выпишите в тетрадь сведения о нем. Одни элементы встречаются в природе «на каждой шагу», другие — чрезвычайно редко. Распростриненность элемента в воздухе, воде, почве и т. п. оценивают, сравнивая количество его атомов с количеством атомов других элементов. Распределение элементов в разных частях нашей планеты изучает наука геохимия. Значительный вклад в ее развитие внес выдающийся отечественный ученый В. И. Вернадский. Атмосфера почти полностью состоит из двух газов — азота и кислорода. Молекул азота Гидросфера — это реки, озера, моря, океаны, в которых растворены небольшие количества твердых веществ и газов. Приняв во внимание состав молекулы воды Литосфера, или земная кора, — это твердый поверхностный слой Земли. В нем содержится много элементов. Наиболее распространенными являются Оксиген (58 % всех атомов), Силиций (19,6 % ) и Алюминий (6,4 % ). Во Вселенной существуют те же элементы, что и на нашей планете. Первое и второе места по распространенности в ней занимают Гидроген (92 % всех атомов) и Гелий (7 % ) — элементы, атомы которых имеют простейшее строение. Атом — мельчайшая электронейтральная частица вещества, которая состоит из положительно заряженного ядра и отрицательно заряженных электронов. Ион — положительно или отрицательно заряженная частица, образовавшаяся вследствие потери атомом или присоединения к нему одного или нескольких электронов. Вид атомов с определенным зарядом ядра называют химическим элементом. Каждый элемент имеет название и символ. Важнейшие сведения о химических элементах содержатся в периодической системе, созданной русским ученым Д. И. Менделеевым. Почти 90 химических элементов существуют в природе; они различаются по распространенности.
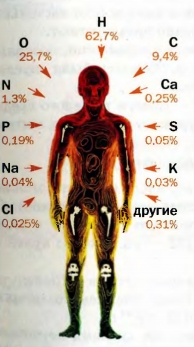
Химические элементы в живой природе Подсчитано, что в среднем 80 % массы растений приходится на воду. В организмах животных и человека это вещество также преобладает. Следовательно, наиболее распространенным элементом в живой природе, как и в гидросфере, является Гидроген.
Растениям нужно немного меньше элементов — Карбон, Оксиген, Гидроген, Нитроген, Фосфор, Калий, Магний, Сульфур. Они поступают в растения из воздуха и почвы вместе с углекислым газом, водой, растворенными в ней веществами.
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. — К.: ВЦ «Академія», 2008. — 136 с.: іл. Содержание урока Если у вас есть исправления или предложения к данному уроку, напишите нам. Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|
||||||||||||||||||||||||||||||
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: