|
Гіпермаркет Знань>>Фізика і астрономія>>Фізика 11 клас>> Фізика: Неперервний і лінійчастий спектри. Спектри поглинання і випромінювання. Спектральний аналіз та його застосування
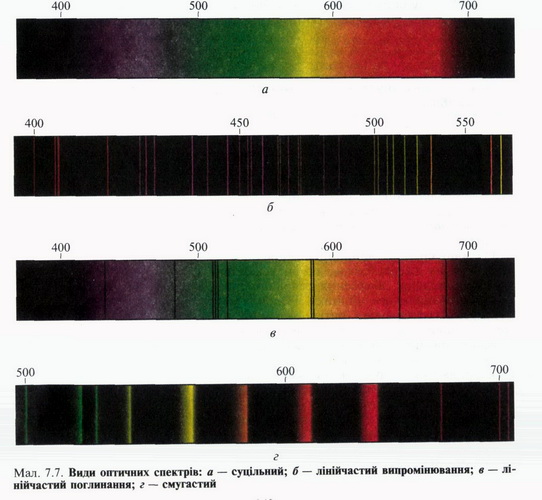
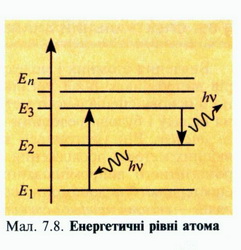
ОПТИЧНІ СПЕКТРИ. ПОГЛИНАННЯ І ВИПРОМІНЮВАННЯ СВІТЛА АТОМОМ Електромагнітне випромінювання будь-якої природи може характеризуватися спектром коливань, на які можна розкласти його за довжиною хвилі або частотою. Залежно від характеру поширення електромагнітних хвиль оптичні спектри поділяють на спектри випромінювання, поглинання, розсіювання і відбиття. Оптичні спектри випромінювання спостерігаються у джерел світла, які випускають фотони внаслідок збудження речовини під впливом зовнішнього чинника. Наприклад, розжарена вольфрамова нитка електричної лампи випромінює світло внаслідок її нагрівання при проходженні по ній електричного струму. Останні три види спектрів спостерігаються в разі проходження випромінювання крізь речовину, внаслідок чого відбувається його поглинання, розсіювання і відбивання залежно від властивостей і довжини хвилі Оптичні спектри поглинання, розсіювання і відбивання характеризують властивості речовини Оптичні спектри спостерігають візуально за допомогою спектральних приладів і фіксують, як правило, фотографічним способом або за допомогою фотоелементів. Спектри можуть бути (мал. 7.7): а) суцільними, що охоплюють широкий діапазон довжин хвиль; Суцільний оптичний спектр спостерігається за умови термодинамічної рівноваги речовини і випромінювання за даної температури. Проте в реальних умовах досягти такого стану практично неможливо, тому найчастіше одночасно спостерігають різні види спектрів. Так, за звичайних умов сонячне світло бачать у спектроскопі у вигляді суцільного спектра з темними лініями поглинання. Механізм утворення суцільних оптичних спектрів пояснює класична електродинаміка. За її тлумаченням поглинуте електромагнітне випромінювання збуджує в речовині хвилі, частота яких відповідає частоті падаючого світла. Проте класична фізика виявилася безпорадною у поясненні лінійчастих і смугастих спектрів випромінювання і поглинання світла атомами і молекулами. їхню природу можна зрозуміти лише на основі квантових постулатів Бора та інтерпретації квантових переходів між рівнями енергії в атомах і молекулах. За класичною теорією монохроматичне світло збуджуватиме хвилі певної частоти, а природне світло утворюватиме суцільний спектр випромінювання Для наочного ілюстрування станів атома використовують енергетичні діаграми, на яких рівні енергії позначають горизонтальними лініями (мал. 7.8). Доволі довго атом може перебувати лише в основному стаціонарному стані, що характеризується мінімальною енергією Е1. Решта станів атома чи молекули (E2, Е3, ..., Еn) є стаціонарними лише умовно, і тому їх називають збудженими станами. Наприклад, якщо незбуджений атом поглине квант hv, то він може перейти в умовно стабільний, збуджений стан Е3, але згодом, випромінивши квант частотою
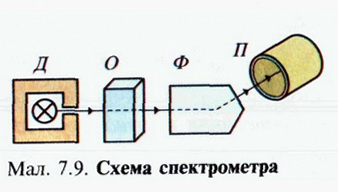
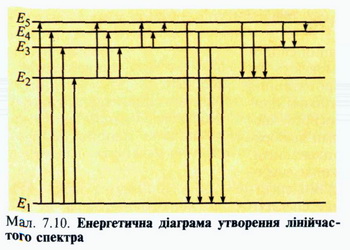
СПЕКТРАЛЬНИЙ АНАЛІЗ ТА ЙОГО ЗАСТОСУВАННЯ Вивчення атомних і молекулярних спектрів випромінювання і поглинання покладено в основу спеціального методу дослідження складу і будови речовини — спектрального аналізу. Він грунтується на кількісних і якісних методах дослідження спектрів електромагнітного випромінювання речовин, які спостерігають за допомогою спеціальних приладів — спектрографів і спектрометрів. Принцип дії цих приладів грунтується на їх здатності виокремлювати в просторі і часі з усього світлового потоку певні ділянки випромінювання. їх можна фіксувати фотографічним способом або вимірювати різні їхні характеристики — зміну світлового потоку, довжину хвилі спектральної лінії тощо (мал. 7.9). Тому головним елементом спектрометрів є селективний пристрій Ф (дисперсійна призма, дифракційна ґратка, інтерферометр тощо), за допомогою якого вдається виділити частину спектра в певному інтервалі довжин хвиль. Метод визначення в тілах якісного складу і кількісного вмісту речовини за її спектром називають спектральним аналізом Селективність (від лат. selectus — вибраний) — вибірковість, ступінь здатності до вибірковості Для вивчення спектрів поглинання світловий потік від джерела Д спрямовують на досліджуваний об'єкт О, після проходження крізь який він потрапляє на селективний пристрій Ф. Відокремлена певним способом частина спектра фіксується пристроями відображення Я (сканувальні екрани, фотоелементи, фотоплівки тощо). Далі характеристики випромінювання порівнюються з одержаним спектром і залежно від обраного методу спектроскопії на підставі їх аналізу роблять висновки щодо досліджуваних спектрів поглинання. За допомогою атомного спектрального аналізу визначають елементний склад зразка, зіставляючи його спектр зі спектральними лініями хімічних елементів, що наводяться у спеціальних таблицях і атласах. Для одержання спектра випромінювання досліджувану речовину потрібно перевести в газоподібний стан і активізувати, тобто перевести її атоми у збуджений стан. Найпростіше це можна зробити за допомогою нагрівання досліджуваного зразка, наприклад помістити його в полум'я. Кожен хімічний елемент має власний набір спектральнихліній, притаманний лише йому одному Для одержання спектра випромінювання атоми речовини слід перевести у збуджений стан, наприклад нагріти тіло до високої температури За високих температур атоми переходять у збуджений стан Е2, E3, Е4, Е5, в якому можуть перебувати недовго (мал. 7.10). З часом вони повертаються у свій основний, стабільний стан E1, випромінюючи при цьому світловий квает пеевної частини: Кожний хімічний елемент має свій, властивий лише йому набір спектральних ліній — атомний спектр. За лініями атомного спектра речовини за допомогою спеціальних таблиць, в яких наведено серії довжин хвиль спектрів випромінювання різних речовин, визначають хімічний склад зразка. В основу молекулярного спектрального аналізу покладено порівняння виміряного спектра зразка зі спектрами окремих речовин. Молекулярні спектри подібні до атомних — вони також лінійчасті, проте мають свої особливості — спектральних ліній більше, тому вони утворюють доволі широкі смуги. Це пояснюють тим, що внаслідок взаємодії атомів, які складають молекулу, енергетичні рівні атомів розщеплюються, адже їх енергія зумовлена двома чинника¬ми — власними коливаннями атомів у молекулі та іншими її рухами. Лінійчастий атомний і смугастий молекулярний спектри відтворюють можливі електронні переходи з одного енергетичного рівня на інші У гірничодобувній промисловості за допомогою спектрального аналізу визначають хімічний склад зразків корисних копалин Спектр молекули є її однозначною характеристикою, за якою ідентифікують речовини. Кількісний вміст речовини визначається за інтенсивністю випромінювання смугастого спектра. Зокрема, застосування сучасних фотоелектричних приладів сумісно з обчислювальною технікою дає змогу виз-начати склад речовин за досить малих їх мас — до 1 мкг і менше. Тому цей метод знайшов широке застосування в науці і техніці. Зокрема, у металургійному виробництві за його допомогою контролюють вміст домішок у сплавах, щоб отримувати матеріали із заданими властивостями. Застосування спектрального аналізу в астрофізиці дає змогу визначати хімічний склад і рух небесних тіл, які знаходяться далеко за межами нашої галактики. ЗАПИТАННЯ
Зміст уроку
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум. |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: